一種在富鋰錳基正極材料表層構造尖晶石結構的方法與流程
本發明涉及一種富鋰錳基正極材料的制備方法,特別涉及一種在富鋰錳基正極材料表層構造尖晶石結構的方法,屬于化學儲能電池領域。
背景技術:
一方面,移動電子設備的飛速發展迫切需要開發更高容量的鋰二次電池;另一方面,歷次的能源危機和嚴峻的環境問題迫使各國政府加大力度推動新能源電動汽車產業的發展,而電動汽車的快速發展也要依靠更高容量和更快充放電速率的鋰二次電池。為滿足這一需求,首先需要發展新一代高容量電極材料。目前,商品化鋰二次電池用正極材料主要采用鈷酸鋰、磷酸鐵鋰和鎳鈷錳(或鎳鈷鋁)三元材料,其實際比容量均小于220mah/g。因此,開發高容量的新型正極材料已成為鋰二次電池研究的重點。
美國阿貢國家實驗室的thackeray小組報到的xli2mno3·(1-x)limo2(m=ni,co,mn或者它們的組合)類鋰離子電池正極材料(簡稱為富鋰錳基正極材料),因為擁有遠超過當前商業化正極材料的放電比容量而受到鋰電行業的廣泛關注(m.m.thackeray,s.-h.kang,c.s.johnson,j.t.vaughey,r.benedek,s.a.hackney,j.mater.chem.2007,17,3112)。富鋰錳基正極材料經過首周活化后,放電比容量能超過250mah/g(qiu,m.zhang,l.wu,j.wang,y.xia,d.qian,h.liu,s.hy,y.chen,k.an,y.zhu,z.liu,y.s.meng,natcommun2016,7,12108),而且也有較好的熱穩定性,其初始熱分解溫度被推遲到250℃以上(h.deng,i.belharouak,y.-k.sun,k.amine,j.mater.chem.2009,19,4510)。然而,富鋰錳基正極材料也存在著首周庫倫效率低、倍率性能差等缺點。研究表明,通過在富鋰錳基正極材料表面包覆嵌鋰氧化物可以提高首周庫倫效率;通過構造分級結構并有序暴露{010}優勢晶面可以顯著提高倍率性能。
尖晶石結構擁有三維的鋰離子擴散通道,用作包覆介質包覆在富鋰錳基正極材料表面可以有效地改善其倍率性能。然而,已有的報道均是通過在電極材料的表面附著具有尖晶石層結構的材料,這種包覆層不僅難以控制其均勻性和厚度,而且在充放電循環過程中可能會脫落、失效,另外。表面包覆的工藝復雜,難以大規模應用于生產。
技術實現要素:
針對現有技術中尚無一種廉價、高效且與本體材料無縫銜接的制備具有尖晶石結構的包覆層的方法,本發明的目的在于提供一種在富鋰錳基正極材料表層構造尖晶石結構的方法,該方法通過將本體材料的表層結構轉變成尖晶石結構,不僅保證鋰離子傳輸通道的暢通,而且避免表層尖晶石結構因為結構應力使材料在充放電循環過程中脫落,解決了富鋰錳基正極材料首周庫倫效率低的問題,并改善了電極材料在反復的充放電循環中的結構穩定性。
本發明的目的是通過以下技術方案實現的。
一種在富鋰錳基正極材料表層構造尖晶石結構的方法,所述方法步驟如下:
將富鋰錳基正極材料加入到弱酸水溶液中,攪拌至ph的變化率小于0.01min-1時,進行固液分離,并將分離得到的固體進行洗滌、干燥;再將干燥后的固體置于250℃以上的溫度下熱處理30min以上,得到表層具有尖晶石結構的富鋰錳基正極材料。
所述富鋰錳基正極材料的化學式如下:xli2mno3·(1-x)limo2,0<x<1,m為ni、co和mn中的一種以上。
所述弱酸水溶液的ph值大于2且小于7。
所述弱酸水溶液中弱酸優選碳酸、乙酸、丙酸、磷酸二氫銨、磷酸二氫鈉、磷酸二氫鉀以及其他磷酸二氫鹽。
所述磷酸二氫銨的質量與富鋰錳基正極材料的質量比為0.01~50:1,磷酸二氫銨水溶液的濃度優選0.01mol/l~1.3mol/l。
優選地,在300℃~500℃下熱處理2h~10h。
有益效果:
(1)本發明所述方法是將富鋰錳基正極材料的本體材料表層結構轉變成尖晶石結構,即所構造的表層尖晶石結構是富鋰錳基正極材料自身的一部分,有效減小了兩種不同結構的界面張力,從而提高了電極材料在反復的充放電循環中的結構穩定性。
(2)采用本發明所述方法制備的富鋰錳基正極材料表面的尖晶石結構具有三維鋰離子擴散通道,這些表層的通道與本體材料原本晶體結構中的鋰離子擴散通道相互連接,保證了在充放電過程中鋰離子擴散通道的暢通。這種結構顯著改善了富鋰錳基正極材料的倍率性能,不僅使其在大的充放電流下(如5c、10c)具有較高的放電比容量,而且首周活化速率也得到顯著提高,其1c速率活化的放電比容量與0.1c速率活化的比容量相當,而且首周庫倫效率也提升到88%以上。
(3)本發明選用弱酸水溶液進行改性,原料成本低廉,工藝及設備簡單,易于擴大生產;而且選用酸性適中的弱酸如磷酸二氫銨,可避免損害電極材料的主體結構;并且通過調節弱酸水溶液的濃度并配合調整處理時間,可以有效調節構造的尖晶石層的深度,從而調節電極材料的電化學性能,這種調控方式簡便、易行,不必要求嚴格控制反應時間,重復可靠性高。
(4)本發明所用原始電極材料為富鋰錳基正極材料,所改造的表層尖晶石結構的主要成分為li-mn-o,所以該方法適用于所有含錳氧化物的改性。
附圖說明
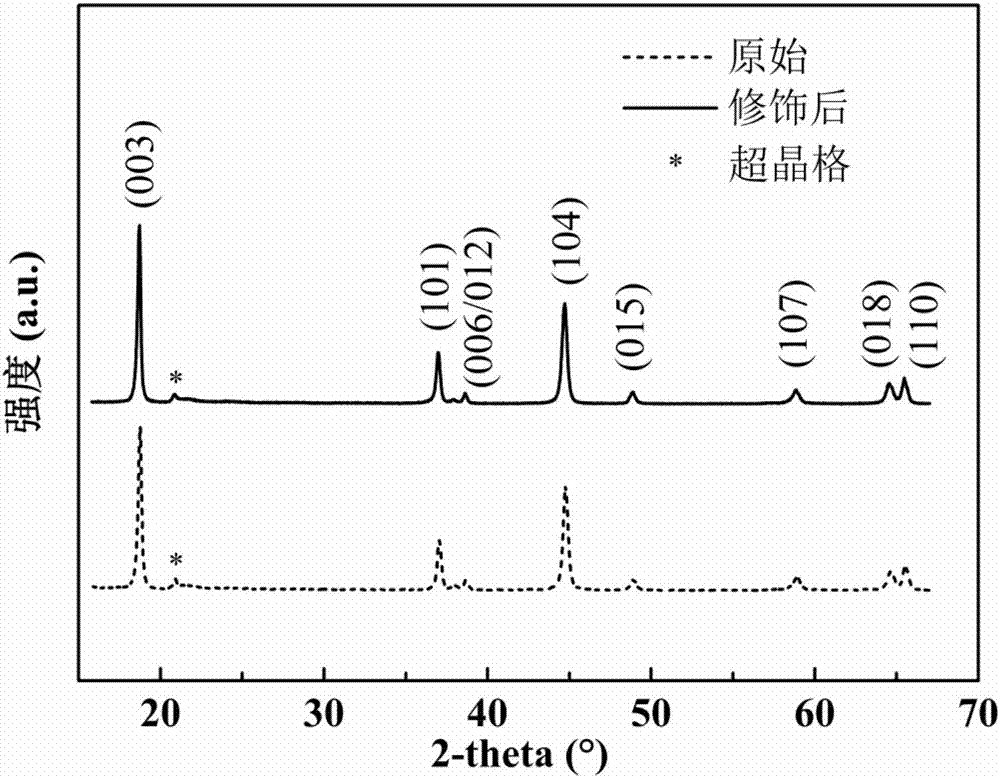
圖1為實施例1修飾后的表層具有尖晶石結構的富鋰錳基正極材料與對比例1制備的原始富鋰錳基正極材料的x射線衍射(xrd)對比圖。
圖2為實施例1修飾后的表層具有尖晶石結構的富鋰錳基正極材料的高分辨透射電子顯微鏡(hrtem)圖。
圖3為采用實施例1修飾后的表層具有尖晶石結構的富鋰錳基正極材料組裝的cr2025鈕扣電池的循環伏安(cv)曲線圖。
圖4為采用對比例1制備的原始富鋰錳基正極材料組裝的cr2025鈕扣電池的循環伏安曲線圖。
圖5為采用實施例1修飾后的表層具有尖晶石結構的富鋰錳基正極材料組裝的cr2025鈕扣電池的倍率性能測試圖。
圖6為采用對比例1制備的原始富鋰錳基正極材料組裝的cr2025鈕扣電池的倍率性能測試圖。
具體實施方式
為更好理解本發明,下面結合具體實施例對本發明做進一步詳細描述。應當理解的是,此處所描述的具體實施方式僅用于說明和解釋本發明,并不用于限制本發明。另外,在本文中所披露的范圍的端點和任何值都不限于該精確的范圍或值,這些范圍或值應當理解為包含接近這些范圍或值的值。對于數值范圍來說,各個范圍的端點值之間、各個范圍的端點值和單獨的點值之間,以及單獨的點值之間可以彼此組合而得到一個或多個新的數值范圍,這些數值范圍應被視為在本文中具體公開。
以下實施例中:
ph計:儀器型號:梅特勒-托利多fe20,中國;
高分辨透射電子顯微鏡(hrtem):儀器型號:hitachih-800,日本;
x射線衍射儀:儀器型號:rigakuultimaiv,日本;
循環伏安(cv)測試:chi660e電化學工作站,中國;測試電壓區間為2v~4.8v,掃描速率0.1mv/s;
電感耦合等離子體質譜(icp)儀:儀器型號:agilent7500ce,美國。
cr2025鈕扣電池的組裝及測試:將正極材料、乙炔黑、pvdf(聚偏氟乙烯)按照8:1:1的質量比制成漿料并涂覆在鋁箔上,用裁片機將烘干的負載漿料的鋁箔裁成直徑約為1cm的小圓片用作正極,以金屬鋰片作為負極、celgard2300為隔膜、1m的碳酸酯溶液為電解液(其中,溶劑是體積比為1:1的碳酸乙烯酯和碳酸二甲酯的混合溶液,溶質為lipf6),在氬氣手套箱內組裝成cr2025紐扣電池;采用ct2001aland電池測試儀對所組裝的cr2025紐扣電池在不同的電流密度下進行恒流充放電測試,定義1c電流密度為250ma/g,充放電電壓區間為2v~4.6v,測試溫度為30℃;其中,所述正極材料為實施例中制備的具有尖晶石結構的富鋰錳基正極材料、對比例1中制備的原始富鋰錳基正極材料或對比例2中制備的硝酸改性的富鋰錳基正極材料。
實施例1~8以及對比例2中所述的富鋰錳基正極材料為對比例1中所制備的原始富鋰錳基正極材料。
實施例1
將5g富鋰錳基正極材料加入到100ml濃度為0.25mol/l磷酸二氫銨水溶液后,進行磁力攪拌使電極材料在酸性溶液中發生li+—h+離子交換,并用ph計測量磷酸二氫銨水溶液的ph值,直至ph值的變化率小于0.01min-1時,進行真空抽濾,并將抽濾得到的固體用去離子水洗滌3次,再置于80℃烘箱干燥6h;再將干燥后的固體置于馬弗爐中,在450℃下燒結5h使表層欠鋰結構轉變成尖晶石結構,隨爐冷卻,得到表層具有尖晶石結構的富鋰錳基正極材料。
圖1為修飾后的表層具有尖晶石結構的富鋰錳基正極材料與原始富鋰錳基正極材料的xrd對比圖,從圖中可知,修飾后的正極材料沒有改變原始富鋰錳基正極材料的主體晶體結構,兩者都是典型的α-nafeo2結構,屬r-3m空間群,(006)/(012)和(018)/(110)峰分裂明顯,在θ=20~22°之間呈現li2mno3的超晶格峰。但是從θ=18~20°以及θ=44~46°兩處的局部放大圖中可知,修飾后的正極材料的(003)峰和(104)峰相對原始富鋰錳基正極材料均微向低角度偏移,說明修飾后的正極材料的層間距相比于原始富鋰錳基正極材料增大了,這將有利于鋰離子的嵌入和脫出。
圖2為修飾后的正極材料的hrtem圖,從圖中可以看到修飾后的正極材料的表層原子與內部原子的排列表現出明顯的差異,內部原子呈典型的層狀結構排布,過渡金屬層的原子排布連續緊密,而表層原子與原子間有明顯的間距。修飾后的正極材料的表層原子排列對應于一種類似limn2o4的尖晶石結構。從hrtem圖中就可以看出,富鋰錳基正極材料表層的這種尖晶石結構比內部的層狀結構有更通暢的li離子擴散途徑;而且,表層的尖晶石結構與內部的層狀結構是連續拼接的,既保證了鋰離子擴散的連續性,又避免了相與相之間由于較大的晶格應變而使結構脫落的問題。
將修飾后的正極材料組裝成cr2025鈕扣電池進行電化學性能測試。為了證實改造的表層結構是尖晶石相,將新組裝的電池進行cv測試;另外,為了排除首周充電活化產生的尖晶石相的影響,cv測試從開路態首先向低電壓方向掃描,測試結果如圖3所示。圖3中的segment1表示的是從開路態向負掃的第一段,與圖4中原始富鋰錳基正極材料的cv曲線相比可知,修飾后的正極材料在2.8v左右處多出一個小峰,在隨后的cv測試中也出現位于該處的氧化峰和還原峰,該特征峰被認為是由尖晶石結構的氧化或還原產生的,證明了修飾后的正極材料中存在著可以辨別的且能夠貢獻容量的尖晶石結構。將cr2025鈕扣電池依次在1c、2c、5c、10c、1c下進行倍率性能測試,結果如圖5所示。根據倍率性能測試結果可知,修飾后的正極材料在1c下的首次放電比容量為259.2mah/g,首次庫倫效率為90.5%,5c放電比容量為222.3mah/g,10c放電比容量為201.9mah/g。
實施例2
將5g富鋰錳基正極材料加入到100ml濃度為0.25mol/l磷酸二氫銨水溶液后,進行磁力攪拌使電極材料在酸性溶液中發生li+—h+離子交換,并用ph計測量磷酸二氫銨水溶液的ph值,直至ph值的變化率小于0.01min-1時,進行真空抽濾,并將抽濾得到的固體用去離子水洗滌3次,再置于80℃烘箱干燥6h;再將干燥后的固體置于馬弗爐中,在300℃下燒結5h使表層欠鋰結構轉變成尖晶石結構,隨爐冷卻,得到表層具有尖晶石結構的富鋰錳基正極材料。
與原始富鋰錳基正極材料的xrd圖譜相比,修飾后的正極材料沒有改變原始富鋰錳基正極材料的主體晶體結構,也是典型的α-nafeo2結構,屬r-3m空間群,(006)/(012)和(018)/(110)峰分裂明顯,在θ=20~22°之間呈現li2mno3的超晶格峰。而且在θ=18~20°以及θ=44~46°處可以看到,修飾后的正極材料的(003)峰和(104)峰相對原始富鋰錳基正極材料均微向低角度偏移,說明修飾后的正極材料的層間距相比于原始富鋰錳基正極材料增大了,這將有利于鋰離子的嵌入和脫出。
從hrtem圖中可以得知,修飾后的正極材料的表層原子與內部原子的排列表現出明顯的差異,內部原子呈典型的層狀結構排布,過渡金屬層的原子排布連續緊密,而表層原子與原子間有明顯的間距。修飾后的正極材料的表層結構對應于一種類似limn2o4的尖晶石結構,這種尖晶石結構比內部的層狀結構有更通暢的li離子擴散途徑。而且,表層的尖晶石結構與內部的層狀結構是連續拼接的,既保證了鋰離子擴散的連續性,又避免了相與相之間由于較大的晶格應變而使結構脫落的問題。
將修飾后的正極材料組裝成cr2025鈕扣電池進行電化學性能測試。與原始富鋰錳基正極材料的cv曲線相比可知,修飾后的正極材料的cv曲線中多出一個位于2.8v左右的還原峰,證明存在尖晶石結構。將cr2025鈕扣電池依次在1c、2c、5c、10c、1c下進行倍率性能測試,根據測試結果可知,修飾后的正極材料在1c下的首次放電比容量為274.8mah/g,首次庫倫效率為95.0%,5c放電比容量為232.8mah/g,10c放電比容量為206.9mah/g。
實施例3
將5g富鋰錳基正極材料加入到100ml濃度為0.25mol/l磷酸二氫銨水溶液后,進行磁力攪拌使電極材料在酸性溶液中發生li+—h+離子交換,并用ph計測量磷酸二氫銨水溶液的ph值,直至ph值的變化率小于0.01min-1時,進行真空抽濾,并將抽濾得到的固體用去離子水洗滌3次,再置于80℃烘箱干燥6h;再將干燥后的固體置于馬弗爐中,在600℃下燒結5h使表層欠鋰結構轉變成尖晶石結構,隨爐冷卻,得到表層具有尖晶石結構的富鋰錳基正極材料。
與原始富鋰錳基正極材料的xrd圖譜相比,修飾后的正極材料沒有改變原始富鋰錳基正極材料的主體晶體結構,也是典型的α-nafeo2結構,屬r-3m空間群,(006)/(012)和(018)/(110)峰分裂明顯,在θ=20~22°之間呈現li2mno3的超晶格峰。而且在θ=18~20°以及θ=44~46°處可以看到,修飾后的正極材料的(003)峰和(104)峰相對原始富鋰錳基正極材料均微向低角度偏移,說明修飾后的正極材料的層間距相比于原始富鋰錳基正極材料增大了,這將有利于鋰離子的嵌入和脫出。
從hrtem圖中可以得知,修飾后的正極材料的表層原子與內部原子的排列表現出明顯的差異,內部原子呈典型的層狀結構排布,過渡金屬層的原子排布連續緊密,而表層原子與原子間有明顯的間距。修飾后的正極材料的表層結構對應于一種類似limn2o4的尖晶石結構,這種尖晶石結構比內部的層狀結構有更通暢的li離子擴散途徑。而且,表層的尖晶石結構與內部的層狀結構是連續拼接的,既保證了鋰離子擴散的連續性,又避免了相與相之間由于較大的晶格應變而使結構脫落的問題。
將修飾后的正極材料組裝成cr2025鈕扣電池進行電化學性能測試。與原始富鋰錳基正極材料的cv曲線相比可知,修飾后的正極材料的cv曲線中多出一個位于2.8v左右的還原峰,證明存在尖晶石結構。將cr2025鈕扣電池依次在1c、2c、5c、10c、1c下進行倍率性能測試,根據測試結果可知,修飾后的正極材料在1c下的首次放電比容量為257.5mah/g,首次庫倫效率為93.2%,5c放電比容量為218.3mah/g,10c放電比容量為197.3mah/g。
實施例4
將5g富鋰錳基正極材料加入到100ml濃度為0.25mol/l磷酸二氫銨水溶液后,進行磁力攪拌使電極材料在酸性溶液中發生li+—h+離子交換,并用ph計測量磷酸二氫銨水溶液的ph值,直至ph值的變化率小于0.01min-1時,進行真空抽濾,并將抽濾得到的固體用去離子水洗滌3次,再置于80℃烘箱干燥6h;再將干燥后的固體置于馬弗爐中,在450℃下燒結2h使表層欠鋰結構轉變成尖晶石結構,隨爐冷卻,得到表層具有尖晶石結構的富鋰錳基正極材料。
與原始富鋰錳基正極材料的xrd圖譜相比,修飾后的正極材料沒有改變原始富鋰錳基正極材料的主體晶體結構,也是典型的α-nafeo2結構,屬r-3m空間群,(006)/(012)和(018)/(110)峰分裂明顯,在θ=20~22°之間呈現li2mno3的超晶格峰。而且在θ=18~20°以及θ=44~46°處可以看到,修飾后的正極材料的(003)峰和(104)峰相對原始富鋰錳基正極材料均微向低角度偏移,說明修飾后的正極材料的層間距相比于原始富鋰錳基正極材料增大了,這將有利于鋰離子的嵌入和脫出。
從hrtem圖中可以得知,修飾后的正極材料的表層原子與內部原子的排列表現出明顯的差異,內部原子呈典型的層狀結構排布,過渡金屬層的原子排布連續緊密,而表層原子與原子間有明顯的間距。修飾后的正極材料的表層結構對應于一種類似limn2o4的尖晶石結構,這種尖晶石結構比內部的層狀結構有更通暢的li離子擴散途徑。而且,表層的尖晶石結構與內部的層狀結構是連續拼接的,既保證了鋰離子擴散的連續性,又避免了相與相之間由于較大的晶格應變而使結構脫落的問題。
將修飾后的正極材料組裝成cr2025鈕扣電池進行電化學性能測試。與原始富鋰錳基正極材料的cv曲線相比可知,修飾后的正極材料的cv曲線中多出一個位于2.8v左右的還原峰,證明存在尖晶石結構。將cr2025鈕扣電池依次在1c、2c、5c、10c、1c下進行倍率性能測試,根據測試結果可知,修飾后的正極材料在1c下的首次放電比容量為270.5mah/g,首次庫倫效率為95.19%,5c放電比容量為224.1mah/g,10c放電比容量為205.5mah/g。
實施例5
將5g富鋰錳基正極材料加入到100ml濃度為0.25mol/l磷酸二氫銨水溶液后,進行磁力攪拌使電極材料在酸性溶液中發生li+—h+離子交換,并用ph計測量磷酸二氫銨水溶液的ph值,直至ph值的變化率小于0.01min-1時,進行真空抽濾,并將抽濾得到的固體用去離子水洗滌3次,再置于80℃烘箱干燥6h;再將干燥后的固體置于馬弗爐中,在450℃下燒結10h使表層欠鋰結構轉變成尖晶石結構,隨爐冷卻,得到表層具有尖晶石結構的富鋰錳基正極材料。
與原始富鋰錳基正極材料的xrd圖譜相比,修飾后的正極材料沒有改變原始富鋰錳基正極材料的主體晶體結構,也是典型的α-nafeo2結構,屬r-3m空間群,(006)/(012)和(018)/(110)峰分裂明顯,在θ=20~22°之間呈現li2mno3的超晶格峰。而且在θ=18~20°以及θ=44~46°處可以看到,修飾后的正極材料的(003)峰和(104)峰相對原始富鋰錳基正極材料均微向低角度偏移,說明修飾后的正極材料的層間距相比于原始富鋰錳基正極材料增大了,這將有利于鋰離子的嵌入和脫出。
從hrtem圖中可以看到,修飾后的正極材料的表層原子與內部原子的排列表現出明顯的差異,內部原子呈典型的層狀結構排布,過渡金屬層的原子排布連續緊密,而表層原子與原子間有明顯的間距。修飾后的正極材料的表層結構對應于一種類似limn2o4的尖晶石結構,這種尖晶石結構比內部的層狀結構有更通暢的li離子擴散途徑。而且,表層的尖晶石結構與內部的層狀結構是連續拼接的,既保證了鋰離子擴散的連續性,又避免了相與相之間由于較大的晶格應變而使結構脫落的問題。
將修飾后的正極材料組裝成cr2025鈕扣電池進行電化學性能測試。與原始富鋰錳基正極材料的cv曲線相比可知,修飾后的正極材料的cv曲線中多出一個位于2.8v左右的還原峰,證明存在尖晶石結構。將cr2025鈕扣電池依次在1c、2c、5c、10c、1c下進行倍率性能測試,根據測試結果可知,修飾后的正極材料在1c下的首次放電比容量為256.1mah/g,首次庫倫效率為92.37%,5c放電比容量為215.4mah/g,10c放電比容量為199.9mah/g。
實施例6
將5g富鋰錳基正極材料加入到100ml濃度為0.01mol/l磷酸二氫銨水溶液后,進行磁力攪拌使電極材料在酸性溶液中發生li+—h+離子交換,并用ph計測量磷酸二氫銨水溶液的ph值,直至ph值的變化率小于0.01min-1時,進行真空抽濾,并將抽濾得到的固體用去離子水洗滌3次,再置于80℃烘箱干燥6h;再將干燥后的固體置于馬弗爐中,在450℃下燒結5h使表層欠鋰結構轉變成尖晶石結構,隨爐冷卻,得到表層具有尖晶石結構的富鋰錳基正極材料。
與原始富鋰錳基正極材料的xrd圖譜相比,修飾后的正極材料沒有改變原始富鋰錳基正極材料的主體晶體結構,也是典型的α-nafeo2結構,屬r-3m空間群,(006)/(012)和(018)/(110)峰分裂明顯,在θ=20~22°之間呈現li2mno3的超晶格峰。而且在θ=18~20°以及θ=44~46°處可以看到,修飾后的正極材料的(003)峰和(104)峰相對原始富鋰錳基正極材料均微向低角度偏移,說明修飾后的正極材料的層間距相比于原始富鋰錳基正極材料增大了,這將有利于鋰離子的嵌入和脫出。
從hrtem圖中可以看到,修飾后的正極材料的表層原子與內部原子的排列表現出明顯的差異,內部原子呈典型的層狀結構排布,過渡金屬層的原子排布連續緊密,而表層原子與原子間有明顯的間距。修飾后的正極材料的表層結構對應于一種類似limn2o4的尖晶石結構,這種尖晶石結構比內部的層狀結構有更通暢的li離子擴散途徑。而且,表層的尖晶石結構與內部的層狀結構是連續拼接的,既保證了鋰離子擴散的連續性,又避免了相與相之間由于較大的晶格應變而使結構脫落的問題。
將修飾后的正極材料組裝成cr2025鈕扣電池進行電化學性能測試。與原始富鋰錳基正極材料的cv曲線相比可知,修飾后的正極材料的cv曲線中多出一個位于2.8v左右的還原峰,證明存在尖晶石結構。將cr2025鈕扣電池依次在1c、2c、5c、10c、1c下進行倍率性能測試,根據測試結果可知,修飾后的正極材料在1c下的首次放電比容量為268.3mah/g,首次庫倫效率為88.2%,5c放電比容量為220.2mah/g,10c放電比容量為192.2mah/g。
實施例7
將5g富鋰錳基正極材料加入到100ml濃度為0.05mol/l磷酸二氫銨水溶液后,進行磁力攪拌使電極材料在酸性溶液中發生li+—h+離子交換,并用ph計測量磷酸二氫銨水溶液的ph值,直至ph值的變化率小于0.01min-1時,進行真空抽濾,并將抽濾得到的固體用去離子水洗滌3次,再置于80℃烘箱干燥6h;再將干燥后的固體置于馬弗爐中,在450℃下燒結5h使表層欠鋰結構轉變成尖晶石結構,隨爐冷卻,得到表層具有尖晶石結構的富鋰錳基正極材料。
與原始富鋰錳基正極材料的xrd圖譜相比,修飾后的正極材料沒有改變原始富鋰錳基正極材料的主體晶體結構,也是典型的α-nafeo2結構,屬r-3m空間群,(006)/(012)和(018)/(110)峰分裂明顯,在θ=20~22°之間呈現li2mno3的超晶格峰。而且在θ=18~20°以及θ=44~46°處可以看到,修飾后的正極材料的(003)峰和(104)峰相對原始富鋰錳基正極材料均微向低角度偏移,說明修飾后的正極材料的層間距相比于原始富鋰錳基正極材料增大了,這將有利于鋰離子的嵌入和脫出。
從hrtem圖中可以看到修,飾后的正極材料的表層原子與內部原子的排列表現出明顯的差異,內部原子呈典型的層狀結構排布,過渡金屬層的原子排布連續緊密,而表層原子與原子間有明顯的間距。修飾后的正極材料的表層結構對應于一種類似limn2o4的尖晶石結構,這種尖晶石結構比內部的層狀結構有更通暢的li離子擴散途徑。而且,表層尖晶石結構與內部的層狀結構是連續拼接的,既保證了鋰離子擴散的連續性,又避免了相與相之間由于較大的晶格應變而使結構脫落的問題。
將修飾后的正極材料組裝成cr2025鈕扣電池進行電化學性能測試。與原始富鋰錳基正極材料的cv曲線相比可知,修飾后的正極材料的cv曲線中多出一個位于2.8v左右的還原峰,證明存在尖晶石結構。將cr2025鈕扣電池依次在1c、2c、5c、10c、1c下進行倍率性能測試,根據測試結果可知,修飾后的正極材料在1c下的首次放電比容量為257.5mah/g,首次庫倫效率為89.8%,5c放電比容量為222.3mah/g,10c放電比容量為193.1mah/g。
實施例8
將5g富鋰錳基正極材料加入到100ml濃度為1.25mol/l磷酸二氫銨水溶液后,進行磁力攪拌使電極材料在酸性溶液中發生li+—h+離子交換,并用ph計測量磷酸二氫銨水溶液的ph值,直至ph值的變化率小于0.01min-1時,進行真空抽濾,并將抽濾得到的固體用去離子水洗滌3次,再置于80℃烘箱干燥6h;再將干燥后的固體置于馬弗爐中,在450℃下燒結5h使表層欠鋰結構轉變成尖晶石結構,隨爐冷卻,得到表層具有尖晶石結構的富鋰錳基正極材料。
與原始富鋰錳基正極材料的xrd圖譜相比,修飾后的正極材料沒有改變原始富鋰錳基正極材料的主體晶體結構,也是典型的α-nafeo2結構,屬r-3m空間群,(006)/(012)和(018)/(110)峰分裂明顯,在θ=20~22°之間呈現li2mno3的超晶格峰。而且在θ=18~20°以及θ=44~46°處可以看到,修飾后的正極材料的(003)峰和(104)峰相對原始富鋰錳基正極材料均微向低角度偏移,說明修飾后的正極材料的層間距相比于原始富鋰錳基正極材料增大了,這將有利于鋰離子的嵌入和脫出。
從hrtem圖中可以看到,修飾后的正極材料的表層原子與內部原子的排列表現出明顯的差異,內部原子呈典型的層狀結構排布,過渡金屬層的原子排布連續緊密,而表層原子與原子間有明顯的間距。修飾后的正極材料的表層結構對應于一種類似limn2o4的尖晶石結構,這種尖晶石結構比內部的層狀結構有更通暢的li離子擴散途徑。而且,表層尖晶石結構與內部的層狀結構是連續拼接的,這既保證了鋰離子擴散的連續性,又避免了相與相之間由于較大的晶格應變而使結構脫落的問題。
將修飾后的正極材料組裝成cr2025鈕扣電池進行電化學性能測試。與原始富鋰錳基正極材料的cv曲線相比可知,修飾后的正極材料的cv曲線中多出一個位于2.8v左右的還原峰,證明存在尖晶石結構。將cr2025鈕扣電池依次在1c、2c、5c、10c、1c下進行倍率性能測試,根據測試結果可知,修飾后的正極材料在1c下的首次放電比容量為266.4mah/g,首次庫倫效率為93.9%,5c放電比容量為223.4mah/g,10c放電比容量為207mah/g。
通過對實施例1、6、7、8中修飾后的表層具有尖晶石結構的富鋰錳基正極材料進行icp測試可知,表層具有尖晶石結構的富鋰錳基正極材料中所含的li量隨磷酸二氫銨濃度的增大而減少,說明離子交換程度隨磷酸二氫銨濃度增大而加深。
對比例1
原始富鋰錳基正極材料用碳酸鹽共沉淀法合成,具體方法如下:按照mn:ni:co=4:1:1的摩爾比將硫酸錳、硫酸鎳和硫酸鈷溶于去離子水中,得到2mol/l的硫酸鹽水溶液;配置含有2mol/l碳酸鈉以及0.02mol/l氨水的堿性水溶液;且碳酸鈉的摩爾數與硫酸鹽的總摩爾數比為1.05:1;將上述硫酸鹽水溶液和堿性水溶液分別用蠕動泵連續加入到帶有攪拌器且通氮氣的反應釜中,且通過調節硫酸鹽水溶液或堿性水溶液的加入速率控制ph值,在氮氣保護氣氛下,控制反應溫度為55℃,ph穩定為8,反應6h后,將得到的沉淀前驅體反復洗滌過濾,再置于80℃下真空干燥12h;將干燥后的沉淀前驅體與li2co3按照li/mn=2的摩爾比研磨混合,將混合均勻的粉末先在500℃下預燒5h,再升溫到900℃煅燒12h,隨爐冷卻,得到層狀富鋰錳基正極材料。
從圖2中的xrd譜圖可知,所制備的原始富鋰錳基正極材料是典型的α-nafeo2結構,屬r-3m空間群,(006)/(012)和(018)/(110)峰分裂明顯,在θ=20~22°之間呈現li2mno3的超晶格峰。
將本對比例所制備的原始富鋰錳基正極材料組裝成cr2025鈕扣電池。cv測試結果如圖4所示,在第一段的掃描中,未出現明顯的還原峰;在隨后的兩段測試中,在4v和4.5v處有兩個明顯的氧化峰,分別對應著ni2+/co3+的氧化和li2mno3的活化,該原始富鋰錳基正極材料的還原峰均在2.8v以上,在2.8v左右沒有可辨別的還原峰。依次在1c、2c、5c、10c、1c下進行倍率性能測試,測試結果如圖6所示。根據測試結果可知,本對比例所制備的原始富鋰錳基正極材料在1c下的首次放電比容量為233.2mah/g,首次庫倫效率為82.4%,5c放電比容量為180.8mah/g,10c放電比容量為153.4mah/g。
對比例2
將0.5g富鋰錳基正極材料加入到100ml濃度為0.05mol/l硝酸水溶液后,進行磁力攪拌使電極材料在酸性溶液中發生li+—h+離子交換,并用ph計測量硝酸水溶液的ph值,直至ph值的變化率小于0.01min-1時,進行真空抽濾,并將抽濾得到的固體用去離子水洗滌3次,再置于80℃烘箱干燥6h;再將干燥后的固體置于馬弗爐中,在450℃下燒結5h,隨爐冷卻,得到硝酸改性的富鋰錳基正極材料。
將所制備的硝酸改性的富鋰錳基正極材料組裝成cr2025鈕扣電池,依次在1c、2c、5c、10c、1c下進行倍率性能測試,根據測試結果可知,本對比例所制備的正極材料在1c下的首次放電比容量為217.2mah/g,首次庫倫效率為88.1%,5c放電比容量為172.6mah/g,10c放電比容量為141.2mah/g。
通過上述實施例以及對比例的測試結果可知,本發明提供的在富鋰錳基正極材料表層構造尖晶石結構的方法,不僅效果卓著,可以顯著改善電極材料的倍率性能以及首周庫倫效率,而且所用原料成本低廉、無毒環保,整個工藝流程簡單、高效、環保,實驗條件寬泛、可靠性高,具有良好的工業應用前景。
- 還沒有人留言評論。精彩留言會獲得點贊!