一種以硅酸鹽玻璃為原料制備三維多孔硅的方法與流程
本發明屬于納米材料領域,更具體地,涉及一種以硅酸鹽玻璃為原料制備三維多孔硅的方法。
背景技術:
硅是地殼中第二大含量(約為26.4%)的元素。它作為一種常見的半導體材料,已經成為現代高科技社會不可或缺的重要技術基礎,單質硅在能源、半導體、有機硅以及冶金工業等方面有著廣泛而重要的應用。目前成熟商業鋰離子電池的負極材料主要為石墨類碳材料,但碳材料的理論儲鋰容量僅為372mah/g,無法滿足人們對高能量密度材料的需求,硅作為鋰離子電池負極材料具有很高的理論容量(約4200mah/g),十倍于商業用石墨烯的容量,在能量存儲方面具有非常大的前景,但是硅負極材料脫嵌鋰過程中體積膨脹較大(>300%),高的體積變化效應導致其較差的循環穩定性,使其距離實用化有一定的距離。
超細多孔納米硅,包括多孔納米硅和多孔微米硅,小尺寸效應可以有效的減弱體積膨脹的應力,還避免一定的容量衰減,多孔結構也可以留下空間緩解膨脹,具有一定的應用前景。目前硅納米材料的制備方法主要有物理法和化學法,物理法主要包括粉碎法、機械合金化法、蒸發冷凝法等;化學法主要包括氣相沉淀法、鎂熱還原法、濕化學還原氣溶膠法等。但是目前這些制備硅納米材料的方法,不僅條件苛刻、成本昂貴,步驟復雜,而且污染嚴重、涉及很多有毒物質、對人危害性較大。例如文獻“carbon-coatedporoussiliconcompositesashighperformanceli-ionbatteryanodematerials:cantheproductionprocessbecheaperandgreener”(j.mater.chem.a,2016,4,552-560)中用銅基催化劑和硅顆粒在無水乙醇中在200℃的條件下水熱,水熱產物用硝酸處理得到多孔硅,這種方法步驟繁瑣,而且無水乙醇在200℃水熱危險系數相當大,不適合廣泛應用。
通過鎂熱還原并加入氯化鈉熔鹽來制備納米硅,由于石英玻璃中的主要成分是二氧化硅,石英玻璃中二氧化硅結晶性較好,熔點高達1400℃以上,反應所需能量更大,反應時間較長,得到的納米硅沒有特殊的三維結構,副產物硅化鎂有較多,導致產率不高,顆粒堆積明顯大小不均,作為負極材料嵌鋰過程中體積膨脹仍得不到有效緩解,電化學性能也不是很理想。因為這些原料與鎂反應是一種“固-液”反應,制備出來硅的形貌跟原料形貌相似僅僅是納米顆粒堆積出來的多孔結構,納米硅并沒有形成一個整體,當體積膨脹時會導致顆粒間的分離失去良好的電接觸,最終導致電子無法有效的傳輸,容量減弱加速,倍率性能較差。
值得注意的是,由于鎂熱還原過程中會放出大量的熱,使材料局部溫度達到1700℃以上,進而使得前驅物納米顆粒團聚成塊體,難以保持原始形貌,最終得到的產物也是團聚在一起的大塊材料。例如專利“用稻殼生產納米硅的方法”(cn104030290a)中在沒有熔鹽存在的情況下制備得到的納米硅就存在嚴重的團聚現象。熔鹽法可有效解決團聚問題,目前熔鹽主要采用nacl、kcl等非鎂的熔鹽體系,然而這些熔鹽并不能很好的促進鎂熱反應,反應過程中熔融態的還原劑金屬鎂無法與這些熔鹽很好的浸潤互溶,導致鎂與反應物無法充分的接觸反應,因而需要更長的反應時間和更多鎂的量,而且產物純度不高。
然而,盡管納米硅可以解決體積膨脹問題,但是大部分納米硅的多孔主要是由很多納米硅顆粒堆積而成,納米硅并沒有形成一個整體,當體積膨脹時會導致顆粒間的分離失去良好的電接觸,最終導致電子無法有效的傳輸,容量減弱會加速,倍率性能較差,都需要復雜的碳包裹納米硅來解決這個問題,增加成本跟工序,無法廣泛推廣。另外,相對于多孔微米顆粒,由于納米顆粒表面活化能很高導致電極材料振實密度低,從而使得單位體積的電極材料能量較低,因此導致電池體積過大,影響廣泛使用。
技術實現要素:
針對現有技術的以上缺陷或改進需求,本發明提供了一種三維多孔硅及其制備方法和應用,其目的在于通過以硅酸鹽玻璃為原料,以鎂的鹵化物為熔鹽,采用低溫鎂熱還原反應制備得到納米多孔硅,由此解決現有技術納米硅制備方法條件苛刻、成本昂貴、步驟復雜、污染嚴重,同時制備得到的納米硅團聚現象嚴重、副產物多、多孔結構僅存在于硅顆粒之間以及體積能量密度低不能滿足電池負極材料的應用要求等技術問題。
為實現上述目的,按照本發明的一個方面,提供了一種多孔硅顆粒,所述多孔硅顆粒的粒徑范圍為1~5微米,所述多孔硅顆粒內部具有三維貫通的孔結構,所述孔結構中大孔結構尺寸為50~200納米,介孔結構的尺寸為2~6納米。
優選地,所述多孔硅顆粒的比表面積為270~380m2g-1。
優選地,所述多孔硅顆粒的振實密度為0.76~0.835g/cm3。
按照本發明的另一個方面,提供了一種三維多孔微米硅的制備方法,將粉末狀硅酸鹽基玻璃、鎂粉與熔鹽按照質量比1:(0.5~0.8):(5~8)混合均勻后,以1~10℃/min的升溫速度加熱到605~750℃保溫1~12h,然后酸洗得到多孔微米硅。
優選地,所述硅酸鹽玻璃為硅酸鈉玻璃或硅酸鈣玻璃。
優選地,所述熔鹽為鹵化鎂。
優選地,所述熔鹽為氯化鎂、溴化鎂或碘化鎂。
優選地,所述熔鹽為氯化鎂。
優選地,所述的制備方法,包括如下步驟:
(1)將硅酸鹽玻璃清洗后機械球磨成玻璃粉末,得到粉末狀的硅酸鹽玻璃;
(2)將步驟(1)得到的粉末狀的硅酸鹽玻璃、鎂粉與鹵化鎂按照質量比為1:(0.5~0.8):(5~8)混合均勻得到混合物;
(3)將步驟(2)得到的混合物以1~10℃/min的升溫速度加熱到605~750℃保溫1~12h,得到反應后的混合物;
(4)將步驟(3)得到的反應后的混合物進行酸洗,酸洗后得到多孔硅顆粒。
優選地,所述酸洗步驟具體為:在1mol/l的鹽酸中攪拌條件下清洗1~8h,然后在0.1mol/l的氫氟酸中清洗,干燥得到多孔微米硅顆粒。
按照本發明的另一個方面,提供了一種所述的多孔硅顆粒的應用,應用于鋰離子電池負極材料。
總體而言,通過本發明所構思的以上技術方案與現有技術相比,能夠取得下列有益效果。
(1)本發明制備多孔硅采用的原料為硅酸鹽玻璃,原料來源廣泛,合成方法簡單易行,成本低廉,產率純度高,可大規模生產,原料也可回收循環使用;
(2)原料硅酸鹽玻璃在605℃~750℃處于熔融態,此溫度也處于反應溫度范圍內且鎂粉也處于液態,是一種“液-液”鎂熱反應優于其他“固-液”鎂熱反應,便于反應充分進行并得到穩定的、分布均勻的三維多孔結構;
(3)在制備過程中用氯化鎂,溴化鎂,碘化鎂等鎂的金屬鹽作為熔鹽,由于這些熔鹽的熔點也在605-750℃之間,一方面保證反應環境穩定,并作為吸熱劑避免產物團聚燒結,另一方面由于這些鎂鹽熔融態下對鎂粉有更好的溶解性以及對反應物有更加好的潤濕性,使得整個反應更宜進行,反應更充分,反應所需能量更低,整個反應更加安全;
(4)本發明所制備出的三維多孔硅具有鋰離子電池負極材料應有的優點:多孔結構既可以有利電解液接觸又可以緩解嵌鋰過程中的體積膨脹,三維多孔結構還有利于電極材料反應是向內膨脹進而保證這個電極膜的厚度保持穩定,大大提高目前鋰離子電池的安全性;此外,這種三維貫穿結構更有利于鋰離子傳輸,應用前景廣泛。
(5)微米級別的尺寸具有大的振實密度可以達到提高電極單位體積能量密度,本發明制備的多孔微米硅的振實密度為0.81g/cm3,而市購納米硅的振實密度僅為0.15g/cm3。
(6)本發明多孔微米硅的制備方法各步驟協同合作,構成了一套獨立的技術方案,制備得到了優良的多孔微米硅。本發明選擇硅酸鹽基玻璃為原料,以鹵化鎂為熔鹽,由于二者在605-750℃之間均為熔融態,這樣才能夠實現熔融態反應,實現了良好的傳質,而硅酸鹽基玻璃本身由于含有鈉、鈣、鎂、鋁等雜質共生其中以及互熔的熔鹽骨架貫穿其中,利用這一獨特的優勢,通過酸洗反應產物,得到了三維貫通的微米硅的多孔結構。
附圖說明
圖1為本發明實施例1制備得到的三維多孔硅的掃描電鏡圖;
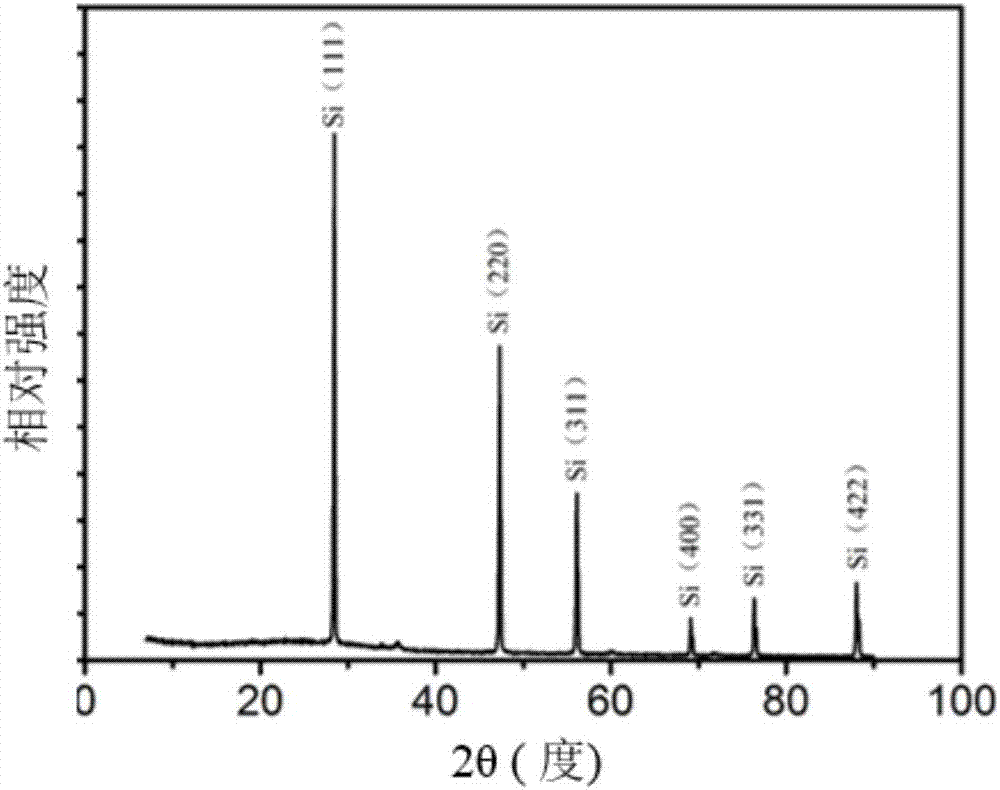
圖2為本發明實施例1制備得到的三維多孔硅的xrd圖譜;
圖3為本發明實施例1制備得到的三維多孔硅的透射電鏡圖;
圖4為本發明實施例1制備得到的三維多孔硅的電化學循環性能圖;
圖5為本發明實施例1制備得到的三維多孔硅的吸附和解吸附曲線以及孔徑分布曲線。
具體實施方式
為了使本發明的目的、技術方案及優點更加清楚明白,以下結合附圖及實施例,對本發明進行進一步詳細說明。應當理解,此處所描述的具體實施例僅僅用以解釋本發明,并不用于限定本發明。此外,下面所描述的本發明各個實施方式中所涉及到的技術特征只要彼此之間未構成沖突就可以相互組合。
本發明提供的多孔硅顆粒的粒徑范圍為1~5微米,所述多孔微米硅顆粒內部具有三維貫通的孔結構,所述孔結構中大孔結構尺寸為50~200納米,介孔結構的尺寸為2~6納米。所述多孔硅顆粒的比表面積為270~380m2g-1。所述多孔硅顆粒的振實密度為0.76~0.835g/cm3。
該三維多孔微米硅的制備方法為:將粉末狀硅酸鹽基玻璃、鎂粉與熔鹽按照質量比1:(0.5~0.8):(5~8)混合均勻后,以1~10℃/min的升溫速度加熱到605~750℃保溫1~12h,然后酸洗得到多孔微米硅。
所述硅酸鹽玻璃為硅酸鈉玻璃或硅酸鈣玻璃。所述熔鹽為鹵化鎂,包括氯化鎂、溴化鎂或碘化鎂,優選為氯化鎂。
具體地,該制備方法,包括如下步驟:
(1)將硅酸鹽玻璃清洗后機械球磨成玻璃粉末,得到粉末狀的硅酸鹽玻璃;
(2)將步驟(1)得到的粉末狀的硅酸鹽玻璃、鎂粉與鹵化鎂按照質量比為1:(0.5~0.8):(5~8)混合均勻得到混合物;
(3)將步驟(2)得到的混合物以1~10℃/min的升溫速度加熱到605~750℃保溫1~12h,得到反應后的混合物;
(4)將步驟(3)得到的反應后的混合物進行酸洗,酸洗后得到多孔硅顆粒。
作為優選的方案,將硅酸鹽玻璃粉末、鎂粉、熔鹽(mgcl2)按照質量比為1:0.6:6的量球磨混合均勻;然后將混合物放入管式爐中以5℃/min的升溫速度加熱到650℃保溫3h,待產物隨爐冷卻至室溫后取出;鎂粉與煤焦油量的選擇保證反應完全得到納米碳化硅減少副產物,mgcl2的量選擇既可保證反應有足夠的熔融介質又可以通過反應焓變計算得到恰當的吸熱效果防止顆粒燒結團聚。升溫速度優選5℃/min,既可以保證反應時間短又可以保證產物的多孔結構更穩定。反應溫度優選650℃,一方面接近鎂粉熔點(649℃)保證鎂粉熔融態反應,反應接觸更充分,另一方面此溫度下硅酸鹽玻璃也處于熔融態,更有利于多孔結構的保持。
所述酸洗步驟具體為:在1mol/l的鹽酸中清洗并攪拌1~8h然后在0.1mol/l的氫氟酸中清洗10min~30min,干燥得到多孔硅納米顆粒。
酸洗是形成多孔結構的關鍵,熔融反應后硅酸鹽基玻璃中的鈉鈣鎂鋁的氧化物、產物氧化鎂以及熔鹽骨架殘留在產物硅中,酸洗溶解掉硅顆粒內部的鈉鈣鎂鋁的氧化物、產物氧化鎂以及熔鹽,液液反應由于鈉鈣鎂鋁的氧化物、產物氧化鎂以及熔鹽在硅酸鹽基玻璃中是三維貫通存在于其中,因此經過“液-液”反應并酸洗之后,可得到硅顆粒內部的三維貫通的孔結構。
本發明制備得到的多孔硅顆粒可以應用于鋰離子電池負極材料。
本發明提供的一種以硅酸鹽基玻璃為原料制備三維多孔硅的方法,包括以下步驟:將玻璃碾磨碎,然后通過機械球磨的方法將玻璃的顆粒尺寸降低后將玻璃粉末和鎂粉、熔鹽按照一定的比例均勻球磨混合后放入在惰性氣體下反應,反應式為mxsio3+2mg=2mgo+si+mxo,其中m為na,ca,mg和al中的一種或多種,隨后將反應產物酸洗處理得到三維多孔硅。
本發明選用熔點在反應溫度附近的硅酸鹽玻璃為原料,這既可以保證反應充分進行又可以產生結構穩定的三維多孔結構。普通的硅酸鹽基玻璃在605~750℃處于熔化狀態的特征,反應時鎂粉也是熔融態,保證一種優異的“液-液”反應發生,有利于原料與液態mg的充分接觸和快速傳質過程,液液反應相對于固液或固固反應,體系溫度和成分更均勻,多孔結構更穩定,普通玻璃反應后存在的堿性氧化物na2o,cao,反應產物mgo以及熔鹽等骨架結構會以三維貫通的形式殘留在產物硅的顆粒中,通過酸洗后去掉骨架結構能得到硅顆粒內部的具有三維貫通的孔結構的多孔微米硅。
本發明采用氯化鎂(mgcl2)、溴化鎂(mgbr2)和碘化鎂(mgi2)等作為熔鹽通過熔化吸熱將反應溫度控制在800℃以下,使整個反應在相對溫和的條件下充分進行,使反應所需要的能量更低并能解決納米顆粒團聚燒結。在熔鹽的選擇上有別于上述傳統的熔鹽體系(nacl、kcl體系)是一種創新的熔鹽體系方案。
本發明中用到的工業和生活中廢棄的硅酸鹽基玻璃相對于其他含硅礦物質來說來源豐富且簡單易得,利用現有的廢物,采用低溫鎂熱還原反應得到納米硅使其有了更大的利用價值,制備的三維多孔硅具有純度較高、比表面積大、顆粒均勻且存在介孔等特點,可以應用于鋰離子電池負極材料領域。
以下為實施例:
實施例1
(1)將5g硅酸鈉玻璃先簡單的用去離子水反復清洗后干燥;將清洗后的普通玻璃研磨成粉末,進一步通過機械球磨的方法將其加工到微米級;
(2)將球磨好的硅酸鹽玻璃粉末、鎂粉、熔鹽(mgcl2)按照質量比為1:0.6:8的量球磨混合均勻;
(3)然后將混合物放入管式爐中以5℃/min的升溫速度加熱到650℃保溫3h,待產物隨爐冷卻至室溫后取出;
(4)將所得產物先在1mol/l鹽酸中清洗1小時。然后在0.1mol/l的氫氟酸中清洗0.5小時,抽濾后干燥得到多孔硅顆粒。
由圖1的掃描電鏡圖可知,本實施例制備得到的硅屬于1~5微米級別的三維多孔結構的硅,放大圖可以看見在硅顆粒內部具有明顯的三維貫通的多孔結構。
由圖2的xrd衍射圖譜可知,在28.4°、47.3°和56.1°的三強峰與硅(jcpdsno.27-1402)的三強峰相對應,并基本無雜相。
由圖3的透射電鏡圖可知,本實施例制備得到的三維多孔硅,具有優異的孔道結構且整體結構沒有破壞,且其中大孔孔徑為50~200納米。
圖4所示多孔硅優異的電化學循環性能,循環100次仍有較高的容量,循環穩定性好,因此本發明可在工業上大規模生產和應用。
如圖5所示,多孔硅的比表面積為380m2g-1,其中介孔孔徑為2~6納米。經測試該多孔微米硅的振實密度為0.81g/cm3,此方法合成的多孔硅具有超高的比表面積和優異的孔結構,適合用于鋰電池負極材料。
實施例2
將5g硅酸鈣玻璃先簡單的用去離子水反復清洗后干燥;將清洗后的廢棄玻璃研磨成粉末,進一步通過機械球磨的方法將其加工到微米級;
(2)將球磨好的硅酸鹽玻璃粉末、鎂粉、熔鹽(mgcl2)按照質量比為1:0.8:7的量球磨混合均勻;
(3)然后將混合物放入管式爐中以1℃/min的升溫速度加熱到605℃保溫12h,待產物隨爐冷卻至室溫后取出;
(4)將所得產物分別在1mol/l的鹽酸中清洗并攪拌2h然后在0.1mol/l的氫氟酸中清洗0.5小時,反復清洗抽濾后干燥得到多孔硅顆粒。
實施例3
將5g硅酸鈉玻璃先簡單的用去離子水反復清洗后干燥;將清洗后的廢棄玻璃研磨成粉末,進一步通過機械球磨的方法將其加工到微米級;
(2)將球磨好的硅酸鹽玻璃粉末、鎂粉、熔鹽(mgbr2)按照質量比為1:0.5:7的量球磨混合均勻;
(3)然后將混合物放入管式爐中以2℃/min的升溫速度加熱到605℃保溫12h,待產物隨爐冷卻至室溫后取出;
(4)將所得產物分別在1mol/l的硝酸中清洗并攪拌然后在0.1mol/l的氫氟酸中清洗0.5小時,反復清洗抽濾后干燥得到多孔硅顆粒。
實施例4
(1)將5g硅酸鈣玻璃先簡單的用去離子水反復清洗后干燥;將清洗后的廢棄玻璃研磨成粉末,進一步通過機械球磨的方法將其加工到微米級;
(2)將球磨好的硅酸鹽玻璃粉末、鎂粉、熔鹽(mgi2)按照質量比為1:0.7:6的量球磨混合均勻;
(3)然后將混合物放入管式爐中以3℃/min的升溫速度加熱到700℃保溫3h,待產物隨爐冷卻至室溫后取出;
(4)將所得產物分別在1mol/l的鹽酸中清洗并攪拌4h然后在0.1mol/l的氫氟酸中清洗0.5小時,反復清洗抽濾后干燥得到多孔硅顆粒。
實施例5
(1)將5g硅酸鈣玻璃先簡單的用去離子水反復清洗后干燥;將清洗后的廢棄玻璃
研磨成粉末,進一步通過機械球磨的方法將其加工到微米級;
(2)將球磨好的硅酸鹽玻璃粉末、鎂粉、熔鹽(mgcl2)按照質量比為1:0.65:5的量球磨混合均勻;
(3)然后將混合物放入管式爐中以10℃/min的升溫速度加熱到750℃保溫3h,待產物隨爐冷卻至室溫后取出;
(4)將所得產物分別在1mol/l的鹽酸中清洗并攪拌1h然后在0.1mol/l氟酸中清洗0.5小時,反復清洗抽濾后干燥得到多孔硅顆粒。
本領域的技術人員容易理解,以上所述僅為本發明的較佳實施例而已,并不用以限制本發明,凡在本發明的精神和原則之內所作的任何修改、等同替換和改進等,均應包含在本發明的保護范圍之內。
- 還沒有人留言評論。精彩留言會獲得點贊!