二硼化鈦材料的再循環方法與流程
本專利申請是優先權日為2012年6月6日、發明名稱為“二硼化鈦材料的再循環方法”的中國發明專利申請第201380036979.1號(國際專利申請號為pct/us2013/044283)的分案申請。
相關申請的交叉引用
本申請要求2012年6月6日提交的美國臨時申請號61/656,357、2012年9月10日提交的美國臨時申請號61/698,897和2013年3月15日提交的美國臨時申請號61/787,127的優先權。通過引用將美國臨時申請號61/656,357、61/698,897和61/787,127的公開內容以其整體并入本文用于所有目的。
美國政府權利
n/a
版權通告
本申請包括受到著作權保護的材料。著作權所有人不反對任何人對該專利公開內容的臨摹復制,如其出現在專利和商標局的文件或記錄中,然而在其它方面保留所有的著作權權利。
發明背景
1.發明領域
本發明涉及廢的或用過的硼化鈦(“tib2”)制品(包括玷污的tib2制品)的再循環。更具體地,本發明涉及通過氯化tib2制品、提純并使其反應以產生新的tib2制品的tib2制品再循環。在一些實施方案中,二硼化鈦制品是用于再循環工藝的100%的tib2原料。在一些實施方案中,二硼化鈦制品是用于再循環工藝的一定百分比的tib2原料。
在一些實施方案中,氯化tib2原料以使廢tib2制品再循環。在一些實施方案中,tib2制品(例如包括添加劑和/或雜質)能夠被氯化并加工成一種或多種形式(tio2、bcl2、tib2等)。在一些實施方案中,鈦原料包括二硼化鈦制品以及被加工以形成tio2(例如顏料級tio2)的鈦礦石和/或渣(slag)。在一些實施方案中,能夠以特定重量百分比使二硼化鈦制品與鈦原料(例如鈦礦石和/或鈦渣)結合以便由氯化工藝產生tio2和/或產生一種或多種產品。
發明概述
本發明涉及tib2再循環方法,并且特別地,涉及通過氯化再循環tib2原料的方法。
本發明的另外目標和優點將在附圖描述、發明詳述、以及權利要求中變得更加明顯。
本發明前述和/或其它方面及效用可以通過提供產生鈦產品的方法來實現,該方法包括制備tib2原料;并氯化該制備的tib2原料以產生氯化鈦產品。
在另一實施方案中,tib2原料包括tib2制品,并且該tib2原料的制備包括將該tib2制品破碎成預定的平均tib2顆粒尺寸或tib2顆粒尺寸分布。
在另一實施方案中,tib2制品包括tib2裝甲產品、tib2工具產品、tib2涂層、tib2電極和tib2粉末中的至少一種。
在另一實施方案中,tib2原料基本上由破碎的tib2制品組成。
在另一實施方案中,破碎的tib2制品包括鈉和氟的殘留物中的至少一種。
在另一實施方案中,破碎的tib2制品包括不超過2%的鈉和氟的殘留物。
在另一實施方案中,tib2原料的制備還包括將tib2制品與含ti礦石和ti渣中的至少一種組合。
在另一實施方案中,tib2原料的制備還包括將tib2制品與含ti礦石和ti渣中的至少一種的組合破碎成預定的平均顆粒尺寸或顆粒尺寸分布以制備tib2原料。
在另一實施方案中,所述含ti礦石包括鈦鐵礦。
在另一實施方案中,含ti礦石具有以重量計至少80%的tio2含量。
在另一實施方案中,ti渣包括被加工以降低其鐵含量的鈦鐵礦礦石的熔煉產品。
在另一實施方案中,ti渣具有至少85%的tio2含量。
在另一實施方案中,tib2原料包括不超過10%的tib2制品。
在另一實施方案中,tib2原料包括雜質。
在另一實施方案中,所述雜質包括fe、ni、co、w、na、f、al、li、mg、ca、cl、鹵化物鹽、硼酸鹽中的至少一種,以及它們的組合。
在另一實施方案中,所述雜質包括殘留鹽、殘留電解浴、含鈉材料、含鈣材料和含氟化物材料。
在另一實施方案中,該制備的tib2原料的氯化包括在還原氣氛下用氯氣和焦炭氯化該制備的tib2原料。
在另一實施方案中,該制備的tib2原料的氯化包括在高于700℃用氯氣和焦炭氯化該制備的tib2原料。
在另一實施方案中,該制備的tib2原料的氯化包括在低于900℃用氯氣和焦炭氯化該制備的tib2原料。
在另一實施方案中,該制備的tib2原料的氯化包括通過流化床氯化器在900℃和1000℃之間氯化該制備的tib2原料。
在另一實施方案中,該制備的tib2原料的氯化包括在低于900℃用氯氣和焦炭氯化該制備的tib2原料。
在另一實施方案中,該制備的tib2原料的氯化包括在低于800℃用氯氣和焦炭氯化該制備的tib2原料。
在另一實施方案中,制備的tib2原料的氯化包括在低于700℃用氯氣和焦炭氯化該制備的tib2原料。
在另一實施方案中,該制備的tib2原料的氯化產生氯化鈦產品和氯化硼產品。
在另一實施方案中,該制備的tib2原料通過氯化被消耗并且基本上轉變成氯化鈦蒸氣。
在另一實施方案中,該方法還包括提純該氯化的tib2原料以除去副產品。
在另一實施方案中,該氯化的tib2原料的提純包括經由分餾分離出低沸點、中沸點和高沸點的氯化物。
在另一實施方案中,該氯化的tib2原料的提純還包括非氯化物化合物或渣的分離。
在另一實施方案中,該方法還包括使氯化鈦產品反應以產生tib2產品。
在另一實施方案中,使氯化鈦產品反應包括:使氯化鈦產品氧化以產生氧化鈦產品;并且經由碳熱反應使氧化鈦產品反應以產生tib2產品。
在另一實施方案中,氧化鈦產品經由碳熱反應以產生tib2產品的反應包括將氧化硼產品添加至該碳熱反應。
在另一實施方案中,氯化鈦產品的氧化包括在氯化期間將另外的氯化鈦添加至制備的tib2原料以產生氯化鈦產品。
在另一實施方案中,該方法還包括從氯化鈦產品的氧化中回收氯,并且引導該回收的氯以在制備的tib2原料的氯化期間使用從而產生氯化鈦產品。
在另一實施方案中,氯化鈦產品的反應包括:用h2氣體還原氯化鈦產品以產生tib2產品。
在另一實施方案中,該方法還包括使氯化鈦產品和氯化硼產品反應以產生tib2產品。
在另一實施方案中,氯化鈦產品的反應包括:使氯化鈦產品和氯化硼產品氧化以產生氧化鈦產品和氧化硼產品;以及經由碳熱反應使氧化鈦產品和氧化硼產品反應以產生tib2產品。
在另一實施方案中,不添加顯著量的氯化鈦產品或氯化硼產品。
在另一實施方案中,氧化鈦產品經由碳熱反應以產生tib2產品的反應不需要將氧化硼產品添加至碳熱反應。
在另一實施方案中,氯化鈦產品的反應包括:用h2氣體還原氯化鈦產品和氯化硼產品以產生tib2產品。
在另一實施方案中,不添加顯著量的氯化鈦產品或氯化硼產品。
附圖說明
從與附圖結合的各種實施方案的下述說明,本發明的這些和/或其他方面及優點將變得清楚和更易于理解,其中:
圖1示出了根據本發明的實施方案的tib2再循環方法;
圖2示出了根據本發明的實施方案的tib2再循環方法;
圖3示出了根據本發明的實施方案的tib2再循環方法;
圖4示出了對于在200℃下tib2原料的氯化的熱力學模型;
圖5示出了對于在500℃下tib2原料的氯化的熱力學模型;
圖6示出了對于在1000℃下tib2原料的氯化的熱力學模型;
圖7示出了根據本發明一種實施方案的流化柱;和
圖8示出了根據本發明一種實施方案的實驗室級的氯化裝置。
具體實施方式
現在將詳細介紹本發明的各種實施方案。下面描述實施方案以提供本發明的組分、工藝和設備的更全面理解。所給出的任何實施例意圖是示例性的,而不是限制性的。在整個說明書和權利要求書中,下面的術語采用在本文中明確相關的含義,除非上下文另外清楚地指出。本文中所使用的短語“在一些實施方案中”和“在一種實施方案中”并不一定指相同的實施方案,盡管它們可以指相同的實施方案。此外,本文中所使用的短語“在另一實施方案中”和“在一些實施方案中”并不一定指不同的實施方案,盡管它們可以指不同的實施方案。如下所述,可以容易地將本發明的各種實施方案組合而不偏離本發明的范圍或精神。
當本文中提到任何數字范圍時,這種范圍應被理解為包括在所述范圍的最小值和最大值之間的每一個數值和/或部分。例如,約0.5-6%的范圍將清楚地包括約0.6%、0.7%和0.9%的所有中間值,一直向上并且包括5.95%、5.97%和5.99%。相同的理解適用于本文所述的每個其它數字性能和/或元素范圍,除非文中另外清楚地指出。
如本文中所使用的,術語“或”是包括性的操作符,并且等同于術語“和/或”,除非文中另外清楚地指出。術語“基于”不是排他性的并允許基于未描述的另外因素,除非文中另外清楚地指出。另外,在整個說明書中,“一種”(“a”、“an”)和“該”(“the”)的含義包括復數引用。“在…中”的含義包括“在…中”(“in”)和“在…上”(“on”)。
如本文中所使用的,術語“氯化”是指使用氯對材料進行化學處理。例如,在一種實施方案中,使用氯氣和焦炭氯化tib2原料以形成各種氯化物產品。在一種實施方案中,氯化反應是放熱的并且在另一實施方案中,氯化反應在還原氣氛中于約900℃進行。
如本文中所使用的,術語“破碎”是指將材料物理地按壓、變形或擠壓成更小的碎片。在一種實施方案中,破碎材料以增加其表面積。例如,可通過錘磨、顎式破碎、濕磨、球磨(例如超細球磨)等破碎材料。
如本文中所使用的,術語“微晶尺寸”是指結晶形式的材料晶體的平均尺寸。
如本文中所使用的,術語“研磨”是指將材料物理地減小至更小的顆粒,例如通過搗碎、破碎或磨碎。
如本文中所使用的,術語“雜質”是指材料中存在的污染物。例如,在一些實施方案中,tib2制品可包括基于tib2制品的制造方法或用途的雜質,包括殘留鹽(例如氯化物鹽);金屬生產的雜質(例如鋁熔煉);殘留電解浴(例如包括但不限于al、li、na、k、鹵化物鹽、mg、ca及其組合的組分);含鋁材料(例如al、al2o3、alcl3);含鈉材料(例如nacl);和含鈣材料(例如cacl2),僅舉幾例。在一些實施方案中,二硼化鈦材料或制品中存在的雜質還可以包括殘留氯化物鹽和/或含氟化物的材料(例如caf2、naf和alf3)。
如本文中所使用的,術語“顆粒尺寸”是指材料的平均顆粒尺寸。
如本文中所使用的,術語“提純”是指從材料中除去污染物和/或雜質。在一些實施方案中,提純包括蒸餾步驟,例如蒸發以及隨后濃縮的工藝。例如,在本發明的一些實施方案中,在氯化操作期間利用氯化硼產品和氯化鈦產品的沸點將它們與污染物和/或雜質分離。
如本文中所使用的,“反應”是指使組分或材料化學反應以形成另外的組分或材料。例如,在一個實施方案中,氯化鈦產品與氯化硼產品反應從而產生二硼化鈦。
如本文中所使用的,術語“還原”是指將電子添加至原子或離子的過程(例如通過去除氧或添加氫)。例如,在一些實施方案中,還原包括進行氣相還原(例如使用h2氣體)。在其它實施方案中,還原包括通過用于還原反應的等離子相炬供給混合的氯化物產品與氫氣。
如本文中所使用的,術語“表面積”是指材料的平均表面積。
如本文中所使用的,“鈦進料”或“tib2原料”是指在工藝中用作進料的含鈦材料。例如,在一些實施方案中,tib2原料可包括tib2;具有添加劑和/或雜質的破碎tib2制品;和/或具有tib2、ti礦石和/或ti渣的共混材料。
如本文中所使用的,“tib2材料”或“tib2制品”是指二硼化鈦源材料,該二硼化鈦源材料包括其中具有二硼化鈦的材料。在一些實施方案中,二硼化鈦材料包括添加劑和/或雜質。二硼化鈦產品中的添加劑和/或雜質的一些非限制性實例包括:fe、ni、co、w、na、f、al、li、mg、ca、cl、鹵化物鹽、硼酸鹽及其組合。二硼化鈦材料或制品的一些非限制性實例包括:裝甲、切削工具、坩堝、耐磨涂層、蒸發皿、電極、粉末以及用于二硼化鈦材料的機械和/或電子應用中的其他任何制品。
圖1示出了根據本發明實施方案的tib2再循環方法。如圖1所示,用于tib2再循環的方法包括制備tib2原料(100);使該tib2原料氯化(200);提純該氯化物產品(300);使該氯化物產品反應(400);和制造tib2制品(500)。
在本發明的一個實施方案中,操作(100)中的制備tib2原料包括將tib2制品破碎或研磨至期望的平均顆粒尺寸或表面積。例如,tib2原料可被破碎成至5微米至40mm之間的平均顆粒尺寸,或者不超過0.6mm。在另一實施方案中,tib2原料的平均顆粒尺寸足夠小以使得具有足夠的表面積用于發生表面反應/溶解(例如消耗速率)。在一些實施方案中,平均顆粒尺寸至少為約5微米;至少為約10微米;至少為約50微米;至少為約100微米;至少為約500微米;至少為約1mm;至少為約2mm;至少為約3mm;至少為約5mm;至少為約10mm;至少為約15mm;至少為約20mm;至少為約30mm;或至少為約40mm。
在其它實施方案中,二硼化鈦材料(用于氯化步驟)的平均顆粒尺寸是:不大于約5微米;不大于約10微米;不大于約50微米;不大于約100微米;不大于約500微米;不大于約1mm;不大于約2mm;不大于約3mm;不大于約5mm;不大于約10mm;不大于約15mm;不大于約20mm;不大于約30mm;或不大于約40mm。
在一些實施方案中,在氯化之前制備tib2制品。在其它實施方案中,分別從ti礦石和/或渣制備tib2制品,并在破碎或研磨后合并。在另一實施方案中,將tib2制品與ti礦石和/或ti渣合并隨后研磨至預定的平均顆粒尺寸。在一種實施方案中,tib2原料的平均顆粒尺寸在100-500微米之間。在另一實施方案中,tib2原料具有d50平均顆粒尺寸。在又一種實施方案中,tib2原料具有100微米或不超過100微米的最大顆粒尺寸。
在一種實施方案中,tib2原料由破碎的tib2制品構成。在另一實施方案中,tib2原料包括破碎的tib2制品和ti礦石和/或ti渣。例如,tib2原料可包括tib2制品與如下的組合:鈦鐵礦渣(例如50.9wt.%ti);合成金紅石(例如55.2wt.%ti);天然金紅石(例如56.9wt.%ti);氧化鈦渣;及其組合。在一種實施方案中,tib2原料包括基于tib2原料總重量在1%-10%之間的tib2制品。在一些實施方案中,tib2原料包括:不大于約25wt.%的tib2制品;不大于約20wt.%的tib2制品;不大于約15wt.%的tib2制品;不大于約10wt.%的tib2制品;或不大于約5wt.%的tib2制品。在其它實施方案中,tib2原料包括:不大于約5wt.%的tib2制品;不大于約4wt.%的tib2制品;不大于約3wt.%的tib2制品;不大于約2wt.%的tib2制品;不大于約1wt.%的tib2制品;或不大于約0.5wt.%的tib2制品。
在一些實施方案中,tib2原料包括:至少約25wt.%的tib2制品;至少約20wt.%的tib2制品;至少約15wt.%的tib2制品;至少約10wt.%的tib2制品;或至少約5wt.%的tib2制品。在一些實施方案中,共混物包括:至少約5wt.%的tib2制品;至少約4wt.%的tib2制品;至少約3wt.%的tib2制品;至少約2wt.%的tib2制品;至少約1wt.%的tib2制品;或至少約0.5wt.%的tib2制品。
在本發明的一種實施方案中,在操作(200)中使tib2原料氯化包括使tib2原料暴露于氯氣以產生氯化物產品。例如,在一種實施方案中,tib2原料包括tib2制品和具有高百分比tio2的ti礦石(例如鈦鐵礦渣為約85%tio2;合成金紅石為約92%tio2;并且天然金紅石為約95%tio2)。在該實施方案中,氯化鈦產品的產生可通過下面的反應進行:
2c+o2=2co(方程式1)
tio2+2cl2+2co=ticl4+2co2(方程式2)
tio2+2c12+c=ticl4+co2(方程式3)
tib2+5cl2=ticl4+2bcl3(方程式4)
如上面的方程式所示,在一種實施方案中,用氯氣處理tib2原料以形成鈦氯化物和硼(含硼)氯化物。在一些實施方案中,所述氯化包括在氯氣(例如cl2)存在下使tib2原料反應。在一些實施方案中,氯化的溶劑和/或鹽可用于氯化操作200。在一個非限制的實施方案中,氯化操作200在約900℃至1000℃范圍內的溫度在流化床氯化器中完成。在另一實施方案中,在氯化操作200期間,固體tib2原料通過氯化被完全消耗并轉變成蒸氣(例如氯化鈦)。
在一些實施方案中,氯化在如下溫度進行:不大于約室溫,不大于約50℃,不大于約100℃,不大于約150℃,不大于約200℃,不大于約250℃,不大于約300℃,不大于約400℃,不大于約500℃;不大于約600℃,不大于約700℃,不大于約800℃,不大于約900℃,不大于約1000℃,不大于約1200℃,或不大于約1500℃。
在一些實施方案中,氯化在如下溫度進行:至少約室溫,至少約50℃,至少約100℃,至少約150℃,至少約200℃,至少約250℃,至少約300℃,至少約400℃,至少約500℃,至少約600℃,至少約700℃,至少約800℃,至少約900℃,至少約1000℃,至少約1200℃,或至少約1500℃。
如上述方程式1-3所示,當tib2原料包括ti礦石和/或ti渣時,在一些實施方案中,需要將碳添加至氯化反應。在另一實施方案中,當tib2原料主要包含tib2制品時,反應依照方程式4,并且不必向氯化反應添加碳。在一些實施方案中,tib2原料基本上由tib2制品組成,并且在不存在碳的情況下完成tib2原料的氯化。
在本發明的一種實施方案中,tib2原料的氯化產生氯化鈦產品,如ticl4。在另一實施方案中,tib2原料的氯化產生氯化鈦和氯化硼產品,如ticl4和bcl3。
在本發明的一種實施方案中,使tib2制品再循環成二氧化鈦(氧化鈦)。在該實施方案中,根據下面的反應,操作200的氯化鈦產品與氧反應。
ticl4+o2=tio2+2cl2(方程式5)
在使tib2原料氯化之后,操作(200)的氯化物產品可以在操作(300)中提純。
例如,在一種實施方案中,在氯化后,通過分餾成低沸點、中沸點、和高沸點的氯化物而從期望的氯化物產品中分離揮發性物類。
在另一實施方案中,可在操作(300)中除去非氯化的殘留物。例如,在一種實施方案中,在操作(300)中氟化物化合物可蒸發并匯集成(report)凝聚相。
根據本發明的實施方案,提純操作(300)使氯化鈦產品和/或氯化硼產品與其余的氯化物材料和雜質以及污染物分離。例如,在一些實施方案中,提純操作(300)以如下量從氯化物產品(例如期望的氯化鈦和/或氯化硼產品)中除去雜質:至少約0.01wt.%;至少約0.05wt.%;至少約0.1wt.%;至少約0.2wt.%;至少約0.5wt.%;至少約1wt.%;至少約2wt.%;至少約5wt.%;至少約7wt.%;至少約10wt.%;至少約15wt.%;或更大。
在其它實施方案中,提純操作(300)以如下量從期望的氯化物產品中除去雜質:不大于約0.01wt.%;不大于約0.05wt.%;不大于約0.1wt.%;不大于約0.2wt.%;不大于約0.5wt.%;不大于約1wt.%;不大于約2wt.%;不大于約5wt.%;不大于約7wt.%;不大于約10wt.%;不大于約15wt.%;或更大。
在本發明的一種實施方案中,操作(300)的提純氯化鈦產品進一步在操作(400)中反應以產生新的tib2產品。
例如,如圖1所示,可在操作(600)中使氯化鈦產品和氯化硼產品氧化并碳熱反應以產生tib2產品。在一種實施方案中,操作(600)包括在操作(610)中使氯化鈦和氯化硼產品氧化以形成二氧化鈦和氧化硼(如硼酸)產品,隨后在操作(620)中使二氧化鈦和氧化硼碳熱反應以形成tib2產品。
在另一實施方案中,可在操作(700)中在金屬或其鹵化物的存在下通過硼鹵化物的氫還原來產生tib2產品。
在又一種實施方案中,可在1000℃或超過1000℃的溫度下通過鈦(或其氧化物/氫化物)與單質硼的直接反應來產生tib2產品。
在操作(400)中獲得新的tib2產品之后,在操作(500)中將該tib2產品加工成新的tib2制品。例如,tib2產品可通過噴霧干燥制成tib2粉末,或燒結成tib2裝甲板。
圖2和3示出了根據本發明實施方案的tib2再循環方法。
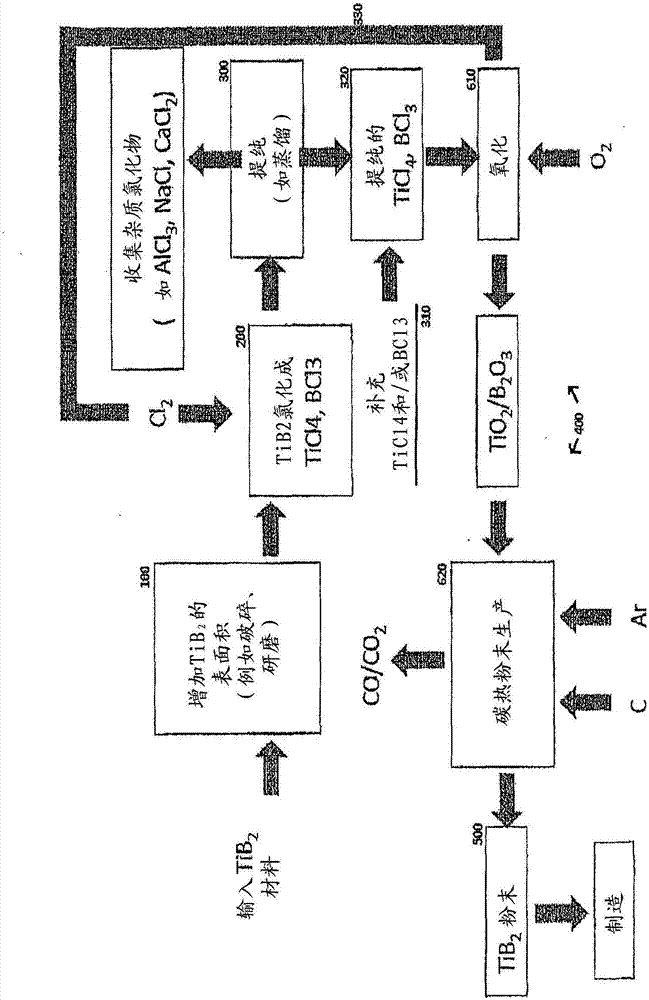
如圖2所示,tib2再循環方法包括增加輸入tib2材料的表面積(100);氯化該tib2材料以產生包括ticl4和bcl3的氯化物產品(200);提純該氯化物產品(300)并使提純的ticl4和bcl3反應(400)以產生tib2粉末(500)。
在本發明的一種實施方案中,tib2原料中的雜質在氯化操作(200)中與氯氣反應從而產生雜質氯化物,并且在提純操作(300)中通過分餾收集并除去該雜質氯化物。
在本發明的一種實施方案中,tib2原料包括ti礦石和/或渣。在該實施方案中,在操作(310)中將另外的ticl4和/或bcl3添加至提純的ticl4和/或bcl3流中。具有另外的ticl4和/或bcl3的提純的ticl4和/或bcl3隨后在操作(610)和(620)中進一步加工以產生tib2粉末。
在另一實施方案中,當tib2原料基本上主要包括tib2制品時,可不需要另外的ticl4和/或bcl3而進行反應操作(400)。例如,圖4-6示出了僅由tib2組成的tib2原料的氯化的模型。如圖4-6所示,tib2原料的氯化產生的ticl4和bcl3量足夠用于在提純操作(300)和反應操作(400)之后的tib2產品的產生并且反應不需要大量的另外ticl4和/或bcl3。
在一種實施方案中,取決于在提純操作(300)之后ticl4和/或bcl3從tib2原料的提純回收,反應操作(400)可進行而不需要大量的另外ticl4和/或bcl3。在另一實施方案中,在提純操作(300)之后氯化鈦化合物與硼氯化物化合物的配給量(ration)對于新tib2產品的產生是合適的。
如圖2所示,提純的ticl4和/或bcl3在操作(400)中反應以產生tib2粉末。在一種實施方案中,使提純的ticl4和/或bcl3在操作(610)中經歷氧化反應以產生氧化鈦和氧化硼產品;并且在操作(620)中使該氧化鈦和氧化硼產品碳熱反應以產生tib2粉末。
在一些實施方案中,將來自氧化操作(610)的氯再循環(300)到氯化器(200)中,同時在操作(620)中進一步加工所得到的二氧化鈦。
如圖3所示,tib2再循環方法包括:增加輸入tib2源材料的表面積(100);氯化該tib2源材料以產生包括ticl4和bcl3的氯化物產品(200);提純該氯化物產品(300)并使提純的ticl4和bcl3(400)反應以產生tib2粉末(500)。
在本發明的一種實施方案中,tib2源材料中的雜質在氯化操作(200)中產生雜質氯化物,并且在提純操作(300)中收集并除去該雜質氯化物。
需要時,在操作(310)中將另外的ticl4和/或bcl3添加到提純的ticl4和/或bcl3流中。隨后使提純的ticl4和/或bcl3在操作(700)中反應以產生tib2粉末。
在一種實施方案中,使提純的ticl4和/或bcl3經歷還原操作(700)以產生tib2粉末(500)。
在一些實施方案中,使來自還原反應(700)的氯再循環(330)到氯化器(200)中。
實施例1:冷流化測試
參考圖7,在tib2顆粒材料上進行冷流化測試以確定tib2顆粒材料是否可用于氯化器中。流化柱裝置包括顆粒床,用增加的空氣體積流化該顆粒床直至跨該床的壓降恒定并且通過目視觀察證實了顆粒的流化。tib2流化測試確認了在小于30篩目(例如<0.6mm)的尺寸范圍內的tib2適合于氯化器中的氯化。
實施例2:氯化實驗
氯化tib2原料以評價其作為用于ticl4產生的氯化物原料的性能。該測試在1000℃至1200℃之間操作的分批式流化床氯化器中進行。1000℃的測試確定氯化反應速率而1200℃的測試確定潛在的難熔材料的腐蝕。
參考圖8,用于實施例2的氯化器是被蛤殼式(clamshell)電阻加熱器單元圍繞的50mm的立式石英管。多孔石英玻璃料充當床支撐體和氣體分散器。從氣瓶計量供給流化氣體(n2或cl2),并且在一系列玻璃冷凝器中冷卻反應器廢氣以回收金屬氯化物反應產品。該測試運行兩個小時并且通過在冷卻后分析殘留的床料來確定反應程度。
測試1:使用100%tib2制品的tib2原料的結果
用100%裝入破碎的tib2制品來進行氯化測試并且氯化器的裝入量與用于氯化包含100%ti礦石的進料的量相似。在tib2原料的氯化測試期間沒有觀察到加工問題(床燒結、冷凝器堵塞等)。基于裝入物在反應兩個小時后的殘留重量,確定總轉化速率為0.3g/min。
測試2:使用共混的tib2制品和ti礦石的tib2原料的結果
還在(1)以重量計98/5的ti礦石:tib2和以重量計98/2的ti礦石:tib2的tib2原料共混物上完成氯化。在實驗(1)和(2)中,床料都沒有粘附于石英管側壁或形成燒結的堵塞物。因此,
共混的tib2原料的實驗室級測試顯示了tib2作為用于ticl4產生的氯化器原料、并進一步加工成tio2和/或新tib2制品的可行性。
與商業級氯化器不同的是,諸如圖8所示的實驗室級氯化器使用石英管側壁。在使用高含量tib2制品用于共混的tib2原料的測試中,例如(3)以重量計50/50的ti礦石:tib2或(2)75/25的ti礦石:tib2;觀察到床料粘附于石英管側壁以及燒結堵塞物的形成。然而25w%的tib2共混物表現出顯著更少的燒結。不受特定機制或理論的限制,一種可能的解釋是,來自tib2的硼與標準礦石中的金屬雜質(na、ca等)反應并引起導致阻塞的低溫硼硅酸鹽玻璃相的形成。然而,因為商業氯化器使用石墨(或其他類似的難熔材料)替代石英,因此本發明人預計以商業規模加工時不會有類似結果。
盡管已經示出并描述了本發明的一些實施方案,但本領域技術人員將會理解可在這些實施方案中進行改變而不脫離本發明的原則和精神,所附權利要求書和它們的等價物限定了本發明的范圍。
本申請提供了如下優選技術方案:
1.一種產生鈦產品的方法,包括:
制備tib2原料;和
氯化該制備的tib2原料以產生氯化鈦產品。
2.技術方案1的方法,其中,所述tib2原料包含tib2制品,并且所述tib2原料的制備包括將所述tib2制品破碎成預定的平均tib2顆粒尺寸或tib2顆粒尺寸分布。
3.技術方案2的方法,其中,所述tib2制品包括下列中的至少一種:tib2裝甲產品、tib2工具產品、tib2涂層、tib2電極和tib2粉末。
4.技術方案3的方法,其中,所述tib2原料基本上由破碎的tib2制品組成。
5.技術方案4的方法,其中,所述破碎的tib2制品包含鈉和氟的殘留物中的至少一種。
6.技術方案5的方法,其中,所述破碎的tib2制品包含不超過2%的鈉和氟的殘留物。
7.技術方案2的方法,其中,所述tib2原料的制備還包括將所述tib2制品與含ti礦石和ti渣中的至少一種組合。
8.技術方案3的方法,其中,所述tib2原料的制備還包括將tib2制品與含ti礦石和ti渣中的至少一種的組合破碎成預定的平均顆粒尺寸或顆粒尺寸分布以制備所述tib2原料。
9.技術方案8的方法,其中,所述含ti礦石包括鈦鐵礦。
10.技術方案9的方法,其中,所述含ti礦石具有以重量計至少80%的tio2含量。
11.技術方案10的方法,其中,所述ti渣包括經處理以降低其鐵含量的鈦鐵礦礦石的熔煉產品。
12.技術方案11的方法,其中,所述ti渣具有至少85%的tio2含量。
13.技術方案12的方法,其中,所述tib2原料包含不超過10%的tib2制品。
14.技術方案13的方法,其中,所述tib2原料包含雜質。
15.技術方案14的方法,其中,所述雜質包括fe、ni、co、w、na、f、al、li、mg、ca、cl、鹵化物鹽、硼酸鹽中的至少一種,以及它們的組合。
16.技術方案15的方法,其中,所述雜質包括殘留鹽、殘留電解浴、含鈉材料、含鈣材料和含氟化物的材料。
17.技術方案16的方法,其中,所述制備的tib2原料的氯化包括在還原氣氛下用氯氣和焦炭氯化所述制備的tib2原料。
18.技術方案17的方法,其中,所述制備的tib2原料的氯化包括在高于700℃用氯氣和焦炭氯化所述制備的tib2原料。
19.技術方案17的方法,其中,所述制備的tib2原料的氯化包括在低于900℃用氯氣和焦炭氯化所述制備的tib2原料。
20.技術方案16的方法,其中,所述制備的tib2原料的氯化包括通過流化床氯化器在900℃和1000℃之間氯化所述制備的tib2原料。
21.技術方案4的方法,其中,所述制備的tib2原料的氯化包括在低于900℃用氯氣和焦炭氯化所述制備的tib2原料。
22.技術方案4的方法,其中,所述制備的tib2原料的氯化包括在低于800℃用氯氣和焦炭氯化所述制備的tib2原料。
23.技術方案4的方法,其中,所述制備的tib2原料的氯化包括在低于700℃用氯氣和焦炭氯化所述制備的tib2原料。
24.技術方案4的方法,其中,所述制備的tib2原料的氯化產生氯化鈦產品和氯化硼產品。
25.技術方案16的方法,其中,所述制備的tib2原料通過氯化被消耗并且基本上轉變成氯化鈦蒸氣。
26.技術方案1的方法,還包括:
提純所述氯化的tib2原料以除去副產品。
27.技術方案24的方法,還包括:
提純所述氯化的tib2原料以除去副產品。
28.技術方案26的方法,其中,所述氯化的tib2原料的提純包括經由分餾來分離低沸點、中沸點和高沸點的氯化物。
29.技術方案28的方法,其中,所述氯化的tib2原料的提純還包括非氯化物的化合物或渣的分離。
30.技術方案29的方法,還包括:
使所述氯化鈦產品反應以產生tib2產品。
31.技術方案30的方法,其中,使所述氯化鈦產品反應包括:
氧化所述氯化鈦產品以產生氧化鈦產品;和
經由碳熱反應使所述氧化鈦產品反應以產生所述tib2產品。
32.技術方案31的方法,其中,所述經由碳熱反應使所述氧化鈦產品反應以產生所述tib2產品包括:將氧化硼產品添加至所述碳熱反應。
33.技術方案32的方法,其中,所述氯化鈦產品的氧化包括在所述氯化以產生氯化鈦產品期間向所述制備的tib2原料添加另外的氯化鈦。
34.技術方案33的方法,還包括由所述氯化鈦產品的氧化回收氯,并且引導回收的氯用以在所述制備的tib2原料的氯化期間使用以產生所述氯化鈦產品。
35.技術方案30的方法,其中,所述氯化鈦產品的反應包括:
用h2氣還原所述氯化鈦產品以產生tib2產品。
36.技術方案27的方法,還包括:
使所述氯化鈦產品和所述氯化硼產品反應以產生tib2產品。
37.技術方案36的方法,其中,使所述氯化鈦產品反應包括:
氧化所述氯化鈦產品和所述氯化硼產品以產生氧化鈦產品和氧化硼產品;并且
經由碳熱反應使所述氧化鈦產品和所述氧化硼產品反應以產生tib2產品。
38.技術方案37的方法,其中,不添加顯著量的氯化鈦產品或氯化硼產品。
39.技術方案38的方法,其中,所述氧化鈦產品經由碳熱反應以產生tib2產品的反應不需要向所述碳熱反應添加氧化硼產品。
40.技術方案27的方法,其中,所述氯化鈦產品的反應包括:
用h2氣還原所述氯化鈦產品和所述氯化硼產品以產生所述tib2產品。
41.技術方案40的方法,其中,不添加顯著量的氯化鈦產品或氯化硼產品。
- 還沒有人留言評論。精彩留言會獲得點贊!