多級納米金花、其制備方法及應用與流程
本發明涉及一種多級結構納米金花、其制備方法及應用,例如制備基于免疫試紙條的高靈敏檢測試劑盒中的應用,屬于材料科學及分析檢測技術領域。
背景技術:
作為納米顆粒體系中極其重要的一員,納米金顆粒本身還具有獨特的物理化學性能,如良好的生物相容性,使納米金顆粒在生物標記和生物傳感方面得到廣泛應用。目前納米金的制備方法主要有:液相還原法、光化學法、氣相蒸發法、種晶生長法、電化學還原法、相轉移法、水熱法、微波法等。但此類方法大多只能用于合成球形納米金顆粒,而不適于制備具有特殊形貌,例如具有花球狀結構的納米金顆粒等。因而,為制備這些具有特殊形貌的納米金顆粒,一般需要另行設計特殊的制備方法,但現有的此類方法大多存在工藝復雜,可控性差,成品率低等不足。另一方面,免疫層析檢測結合了色譜分析和免疫反應的特征,具有快速、簡便檢測分析的有點,廣泛應用于食品、環境和生物醫學領域的快速初級檢測。免疫層析檢測中應用最為普遍的一類是膠體金標記側向試紙條(簡稱金標試紙條),典型的金標試紙條包括PVC膠板、樣品墊、膠體金結合墊、包被膜和吸水墊。當樣品溶液流經試紙條,溶液中待檢測物與結合釋放墊上的金標抗體結合后一起流動到檢測T線固定聚集,通過讀取儀檢測T線金標抗體聚集體的光散射強度,定性檢測目標分子。結合墊中的膠體金起到識別、富集目標檢測物和提供光學檢測信號的重要作用,是決定試紙條靈敏度的關鍵材料之一。常規膠體金試紙條使用納米金球其光學信號有限,靈敏度不高,因而限制了其實際應用。
多級結構納米金花顆粒具有納米級粗糙表面和更大的比表面積,可以結合更多的抗體,更容易捕獲目標檢測物,從而提高試紙條檢測靈敏度。目前已有方法制備的納米金花比表面積相對較小,多級結構不明顯,合成步驟較多,可重復性差。
技術實現要素:
鑒于現有技術的不足,本發明的主要目的在于提供一種多級結構納米金花。
本發明的另一目的在于提供一種簡便、高產率制備所述多級納米金花的方法。
本發明的又一目的在于提供所述多極納米金花的應用。
為實現前述發明目的,本發明采用的技術方案包括:
一種多級結構納米金花的制備方法,其包括:
將氯金酸與作為穩定劑的陽離子聚電解質在水相體系中充分混合,并在溫度為20℃~40℃的條件下持續攪拌或振蕩,至形成的混合溶液呈現黃色,
向獲得的黃色混合溶液內加入還原劑,并劇烈攪拌或振蕩10s以上,優選為10s~60s,再加入作為種子的納米金球,之后將形成的混合反應體系快速攪拌或振蕩10s以上,優選為10s~30s,而后在室溫靜置2h以上,優選為2h~4h。
進一步的,所述還原劑包括抗壞血酸或硼氫化鈉等,優選為抗壞血酸,但不限于此。
進一步的,所述聚電解質包括聚二烯丙基二甲基氯化銨或殼聚糖季銨鹽等,優選為聚二烯丙基二甲基氯化銨,但不限于此。
在一實施方案之中,所述制備方法包括:采用檸檬酸鈉還原氯金酸制得所述納米金球。
在一較佳實施方案之中,所述制備方法包括:在所述混合反應體系中,穩定劑的濃度為1.8%~35wt%,氯金酸的濃度為1mmol/L~20mmol/L,還原劑的濃度為5mmol/L~0.1mmol/L,種子的濃度為2.5×10-4mmol/L~2.5×10-2mmol/L。
其中,所述納米金球的粒徑優選為10nm~30nm。
所述多級結構納米金花的粒徑為50nm~300nm,并且所述納米金花表面具有長約40nm~80nm、寬約10nm~40nm的花瓣型尖端凸起,大幅增加了納米金花的比表面積和表面粗糙度。
一種金標抗體,其包含所述的多級結構納米金花以及結合在所述納米金花上的選定抗體。
所述金標抗體的制備方法包括:將所述的多級結構納米金花與選定抗體于pH值為7~10的液相體系中充分混合,并以BSA或者酪蛋白封閉,再除去未標記的選定抗體。
一種試劑盒,其包括:
免疫層析試紙條,其檢測墊上分布有彼此不重合的檢測線和質控線,所述檢測線和質控線分別包含有第一抗體和第二抗體;
以及所述的金標抗體,其中所述選定抗體采用第三抗體;
其中,所述第一抗體僅在有目標物存在的情況下才能與目標物及第三抗體特異性結合,而所述第二抗體無論在有或無目標物存在的情況下均能與第三抗體特異性結合。
作為較佳實施方案之一,所述試劑盒一種大腸桿菌檢測試劑盒。
一種檢測方法,其包括:
提供所述的試劑盒,
將液態的待檢樣品與所述金標抗體混合后,再施加至所述試紙條的加樣孔中,
以及,以裸眼判讀和/或試紙條讀取儀檢測作為檢測手段,對樣品內的目標物進行定性和/或定量判斷。
進一步的,所述的檢測方法具體可以包括:將金標抗體與液態的待檢樣品充分混合后,再滴加到試紙條的加樣孔中,經設定時間后,以試紙條讀取儀檢測檢測線的光學強度變化,從而定性和/或定量檢測待檢樣品中目標物的含量。
與現有技術相比,本發明的有益效果至少在于:
(1)提供了一種新型的多級結構的納米金花,其具有納米級粗糙表面和更大的比表面積,在應用為試紙條的標記抗體時可以結合更多的抗體,更容易捕獲目標檢測物,從而可大幅提高檢測靈敏度;
(2)提供了一種一步法制備多級結構納米金花的新方法,其操作簡便、,納米金花產率較高,可重復性好;
(3)提供了一種基于所述多級結構納米金花的檢測試劑盒和檢測方法,其能顯著改善常規試紙條的檢測效果,例如,當應用于檢測大腸桿菌時,檢測限可降低到103CFU/mL,靈敏度有顯著提升。
附圖說明
圖1是本發明一典型實施方案之中制備的多級結構納米金花粒子的掃描電鏡圖;
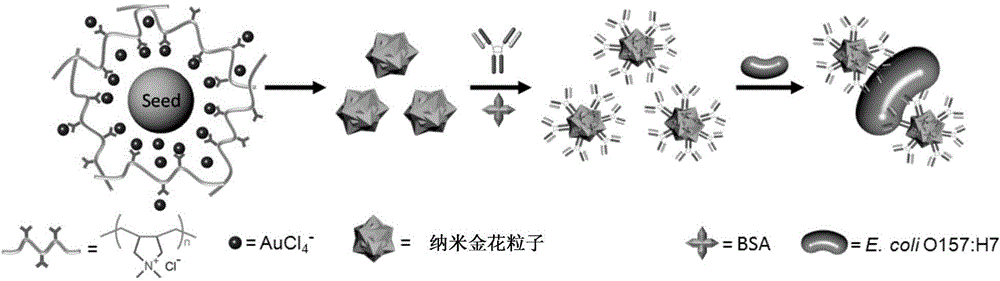
圖2a-圖2b是本發明一典型實施方案之中納米金花表面修飾抗體用于試紙條檢測大腸桿菌的示意圖;
圖3是本發明一典型實施方案之中多級結構納米金花標記抗體檢測不同濃度大腸桿菌的試紙條照片;
圖4是本發明一典型實施方案之中納米金花標記抗體檢測不同濃度大腸桿菌的檢測線光強度圖。
具體實施方式
本發明的一個方面提供了一種多級結構納米金花粒子(如下簡稱“多級結構納米金花”或“納米金花”)的制備工藝,其主要是以聚電解質作為穩定劑,利用高分子鏈段的多級構象,使得金納米粒子在多個成核中心同時生長,從而有效制得多級結構納米金花,該納米金花粒子表面具有納米級的尖端凸起,即表面具有納米級的粗糙形貌,因而具有更大比表面積。
在一較為典型的實施例之中,一種納米金花的制備方法可以包括如下步驟:
1)檸檬酸鈉還原氯金酸制備粒徑為10nm~30nm的納米金球粒子,將其作為制備納米金花粒子的種子。
2)將氯金酸加入聚二烯丙基二甲基氯化銨(PDDA)水溶液中,25℃下攪拌15分鐘以上,至溶液呈現黃色,然后將抗壞血酸水溶液快速加入上述黃色溶液中,劇烈攪拌30秒以上,加入前述的納米金球種子,快速攪拌10秒以上,室溫下靜置4小時以上。
本發明的另一方面提供了所述多級納米金花粒子的用途。例如,將其作為免疫層析試紙條的金標抗體,而應用于生物、化學檢測領域。
進一步的,作為其中的典型應用方案之一,可以在所述納米金花上連接特定的抗體而形成金標抗體,并與試紙條,例如免疫層析試紙條而組合形成試劑盒,用于檢測目標物。
其中,抗體,例如大腸桿菌的特異性單抗可以借助靜電作用力而修飾于納米金花粒子表面。其中,利用納米金花粒子的多級結構和納米級表面凸起,可以修飾更多的抗體,更容易捕獲、富集目標物,例如大腸桿菌細胞,從而提高試紙條檢測目標物的靈敏度。
在本發明中所采用的試紙條可以包括依次設置的過濾墊、樣本墊和檢測墊,所述樣本墊的邊緣部與過濾墊及檢測墊相互接觸或重合,所述檢測墊上分布有彼此不重合的檢測線和質控線,所述檢測線和質控線可分別包含有所述的第一抗體和第二抗體。
進一步,本發明的試劑盒在應用時,其中目標物與所述金標抗體以及檢測線上對應的第一抗體是利用抗原抗體之間的特異性結合的原理呈夾心模式結合,因而,所述試劑盒對于某些生物、化學物質的檢測都是適用的,特別適合于以雙抗夾心模式檢測的大分子蛋白質、細胞等物質。
進一步,所述試紙條還可包括依次分布的過濾墊、樣本墊、檢測墊和吸水墊,所述檢測墊與吸水墊的邊緣部相互接觸或重合。
如本領域技術人員所知曉的,在前述試紙條中,各組成部分的功能大致如下:
過濾墊,主要用于初步過濾樣品基質;
樣本墊,樣本墊經特定處理液處理,具有一定的pH緩沖作用,用于調節待檢物的pH以及 協助待檢物和金標抗體在試紙條上的流動;
檢測墊,檢測墊表面分布有彼此不重合的檢測線和質控線。
進一步的,所述試紙條還可包括:吸水紙,用于吸收多余的金標抗體金以及未參加反應的液體樣品等。
進一步的,所述過濾墊可采用聚酯膜,檢測墊采用硝酸纖維膜,但均不限于此。
在一實施例中,可以將聚酯墊、樣本墊、檢測墊、吸水紙依次重疊組裝成所述試紙條。
本發明的又一個方面提供了一種檢測系統,包括:
所述的試劑盒,
以及,檢測設備,用以監測在所述試紙條上施加待檢樣品與金標抗體的混合物前后,于所述試紙條的質控線和檢測線處的信號變化情況,特別是光學信號變化情況,從而實現對待檢樣品中目標物的定性和/或定量判斷。
進一步的,所述檢測設備包括試紙條讀取儀。
本發明的再一個方面提供了一種檢測方法,其包括:
提供所述的試劑盒,
將液態的待檢樣品與所述金標抗體混合后,再施加至所述試紙條上,
以及,以裸眼判讀和/或試紙條讀取儀檢測作為檢測手段,對樣品內的目標物進行定性和/或定量判斷。
進一步的,所述的檢測方法具體可包括:
將金標抗體與液態的待檢樣品充分混合后,再滴加到試紙條的樣本墊上,經設定時間后,通過裸眼觀察試紙條上檢測線和質控線的顏色變化,定性分析待檢樣品中是否存在目標物,或者以試紙條讀取儀記錄T、C值和T/C值,并與預先建立的標準曲線對照,從而定量檢測待檢樣品中目標物的含量。
進一步的,前述標準曲線可通過業界悉知的方式建立,例如,可以通過下列方法獲得,即:制備一系列不同濃度的目標物的標準樣品,依照前述檢測方法,分別獲得和記錄與不同濃度標準樣品對應的T、C值和T/C值,并探知檢測結果與樣品濃度存在的數學關系,從而建立標準曲線。
其中,T、C值分別為試紙條讀取儀測得的檢測線(T線)和和質控線(C線)的檢測值,例如吸光度值等,這應是本領域技術人員依據常識及本說明書可很容易且明確的知悉的。
即以檢測大腸桿菌為例,本發明中,可以在所述納米金花表面修飾大腸桿菌特異性抗體, 再用于試紙條高靈敏檢測大腸桿菌。
在一較為典型的實施例之中,一種多級結構納米金花標記抗體用于免疫層析試紙條高靈敏檢測大腸桿菌的方法可以包括:
1)納米金花的表面修飾過程。請參閱圖2a,可以將納米金花水溶液室溫下攪拌10分鐘,用碳酸鉀水溶液調節納米金花粒子溶液pH≈8,攪拌10分鐘。將大腸桿菌單抗(murine anti-E.coli O157:H7mAb)水溶液加入納米金花水溶液,室溫攪拌1小時,然后加入封閉劑牛血清蛋白水溶液,室溫攪拌30分鐘。將標記號的好的納米金花抗體離心分離,重新分散在磷酸鹽緩沖液中備用。
2)待檢樣本的提取。將食品待檢測樣本粉碎,分散在水溶液中,過濾后收集濾液,離心濃縮分散在磷酸鹽緩沖液中備用。
3)將納米金花標記抗體與待檢測濃縮溶液在Elisa酶標板中混合,靜置3分鐘。然后將上述混合溶液直接滴入免疫層析試紙條的加樣孔中,靜置10分鐘后,用試紙條讀取儀檢測試紙條檢測線(T線)的光學強度,以獲得檢測大腸桿菌的結果。
顯然的,在該典型實施例采用的試紙條中,亦包含檢測線和質控線,其中檢測線和質控線中可分別包含由大腸桿菌免疫獲得的多抗和能與所有單抗特異性結合的二抗等,其結構和工作原理等可參閱圖2b。
以下進一步結合一更為具體的實施例及附圖對本發明的技術方案作更為詳細的解釋說明。
實施例1:
(1)制備多級結構納米金花顆粒:納米金花的合成是根據納米晶種的再生長法,主要有如下步驟:
第一,金納米晶種的合成:將100毫升、2.5×10-4摩爾/升的氯金酸水溶液加熱到120℃,加入10毫升、1%的檸檬酸鈉水溶液,攪拌30分鐘后,溶液變為酒紅色,停止加熱冷卻到室溫,備用。
第二,多級結構納米金花生長液的配置:取0.4毫升、24毫摩爾/升的氯金酸水溶液加入35%的聚二烯丙基二甲基氯化銨(PDDA)水溶液中,室溫攪拌15分鐘。然后加入0.8毫升、0.1摩爾/升的抗壞血酸水溶液,攪拌30秒,至溶液變成無色通明。
第三,納米晶種生長成納米金花:0.1毫升的納米晶種溶液快速滴加上述第二步配置的生長液中,攪拌均勻,靜置6小時,至溶液變成橙色,表明生成了納米金花,其尺寸和形貌可 參閱圖1。
其中,通過調控PDDA和氯金酸水溶液濃度可以控制納米金花的形貌,而納米金花的微觀形貌可通過掃描電鏡等檢測。
(2)納米金花標記抗體的制備:
將2毫升前述步驟三獲得的納米金花水溶液攪拌10分鐘,加入碳酸鉀水溶液調節pH值>8,攪拌穩定10分鐘。再加入0.5毫升、4.5微克/毫升大腸桿菌單抗水溶液,攪拌1小時。之后加入0.4毫升、5%的牛血清蛋白,攪拌30分鐘。最后,將標記后的納米金花粒子(即金標抗體)離心分離,重新分散在0.4毫升磷酸鹽緩沖液(pH≈7.4)中,備用。
(3)金標抗體用于試紙條檢測大腸桿菌:
將金標抗體與不同濃度(0、103、104、105、106、107CFU/mL)的大腸桿菌樣品溶液混合,靜置3分鐘。參閱圖3,隨后直接轉移到常規免疫試紙條的加樣孔中,10分鐘后檢測樣品溶液全部流過試紙條,用試紙條讀取儀測試檢測線處納米金花聚集體的光散射強度。參閱圖4,可以看到,利用該金標抗體,可以實現對大腸桿菌的高靈敏檢測,檢測濃度下限達到103CFU/mL。
采用本發明的技術方案,可以制備新型免疫層析試紙條,用于食品安全、環境、醫學診斷等領域的簡便、高靈敏分析檢測。
應當指出,以上所述本發明的具體實施方式,并不構成對本發明保護范圍的限定。任何根據本發明的技術構思所作出的各種其他相應的改變與變形,均應包含在本發明權利要求的保護范圍內。
- 還沒有人留言評論。精彩留言會獲得點贊!