術中放療掃描路徑規劃方法和術中放療系統與流程
本申請總體上涉及術中放療領域,更特別地,涉及一種術中放療掃描路徑規劃方法和術中放療系統。
背景技術:
術中放療(intra-operativeradiationtherapy,iort)是手術中對可見腫瘤、瘤床區或易復發轉移部位,在直視下的一次大劑量放療。該技術最大的優勢是可以在手術條件下將部分臨近患者靶區(即,擬放療部位)的重要器官推離到射野外,從而降低其受照劑量。
上個世紀九十年代后期,意大利hitesyss.p.a.和美國intraopmedicalinc.先后推出名為novac7的移動式術中放療裝置(美國專利no.5,635,721)和名為mobetron的可移動電子直線加速器(美國專利no.5,321,271)。然而,這兩種裝置均未考慮術中放療影像的使用,術中放療時完全依賴于醫生的經驗水平,這樣有可能導致靶區劑量不足或重要器官超量,影響術中放療效果。
題為“手術中放射治療裝置”的中國發明專利zl200310108091.2公開了一種新型的手術中放射治療裝置。該裝置的特征是利用ct和mri的三維(3d)影像確定電子束入射病灶的方向和位置。電子直線加速器通過運動機架固定在手術室的天花板上,通過移動運動機架和手術床,可將加速器放置在預先設定的治療位置以進行術中放療。雖然該裝置采集3d影像,但卻是在手術前通過ct或mri影像輔助確定,無法在瘤床暴露狀態下獲取周圍正常組織和重要器官的關系,進而無法確定最優的治療方案。
目前iort的治療方案是放療科醫生在上手術臺后短時間內根據經驗決定的,由于缺少術中3d影像和劑量分布信息,無法評估受照組織的3d劑量,治療方案中的治療參數(例如,治療限光筒大小、角度、能量等)能否正確選擇很大程度上依賴于醫生的經驗水平。這樣有可能導致靶區劑量不足或重要器官超量,影響iort效果。
此外,在臨床治療時,需要經過放療醫生經過手工擺放、固定治療限光筒和放療物理師手工控制手柄移動加速器輻射頭對準射束中軸與限光筒中心軸等長時間的大量工作后,才開始iort,因此難以保證精度。同時,實施的放療是簡單的固定照射野單能治療,單一能量的電子線實現的是單一深度的治療,無法完全適應深度分布多樣的腫瘤形狀,進而導致無法更好地保護腫瘤周圍的正常組織。
技術實現要素:
為了克服現有技術的不足,本申請提供了一種術中放療掃描路徑規劃方法、術中放療系統及其控制裝置,其中利用所獲得的術中影像建立待放療區域的3d模型,以便于精確地確定待放療區域,并且為其分配放療劑量。本申請中還利用機械臂實現術中放療組件的高精度多自由度機械掃描,從而實現精確的調強調能放療處理。使用機械臂還可以在手術室復雜的環境下為術中放療建立統一坐標系,從而確定模擬定位和治療實施的空間位置關系。
根據本申請一示例性實施例,一種術中放療掃描路徑規劃方法可包括:透過輔助掃描組件獲得待掃描區域的多幅圖像;基于所述待掃描區域的多幅圖像建立所述待掃描區域的3d模型;基于所述3d模型確定待放療區域;以及針對所述待放療區域規劃放療組件的掃描路徑。
在一些示例中,所述輔助掃描組件可以是具有開放的上端和封閉的筒底的限光筒,所述限光筒的筒底可設置為貼合到所述待掃描區域上。
在一些示例中,透過輔助掃描組件獲得待掃描區域的多幅圖像可包括:利用超聲組件、ct裝置、x光裝置、或mri裝置來獲得所述待掃描區域的多幅圖像。
在一些示例中,透過輔助掃描組件獲得待掃描區域的多幅圖像可包括:利用機械臂操縱超聲組件在所述輔助掃描組件的內底壁上掃描,以獲得所述待掃描區域的多幅圖像。
在一些示例中,基于所述3d模型確定待放療區域可包括:由圖像識別模塊直接識別出所述3d模型中的待放療區域;或者接收用戶對所述3d模型中的待放療區域的選擇;或者由圖像識別模塊初步識別出所述3d模型中的待放療區域,然后接收用戶對圖像識別模塊初步識別的待放療區域的修改,以確定最終的待放療區域。
在一些示例中,針對所述待放療區域規劃放療組件的掃描路徑可包括:將所述待放療區域劃分成若干個子區域;確定用于每個子區域的放療劑量;以及通過調整強度和能量的方式,規劃放療組件經過每個子區域的掃描路徑和掃描方式,其中所述掃描方式包括步進式掃描和動態連續掃描。
根據本申請一示例性實施例,一種術中放療控制裝置可包括:成像控制模塊,用于控制成像組件沿預定路徑移動并且透過輔助掃描組件對待掃描區域進行掃描,以獲得所述待掃描區域的多幅圖像;建模模塊,用于基于所述多幅圖像建立所述待掃描區域的3d模型;放療區域確定模塊,用于確定所述3d模型中的待放療區域;以及放療路徑規劃模塊,用于規劃放療組件對所述待放療區域進行掃描的路徑。
在一些示例中,所述術中放療控制裝置還可包括:放療執行模塊,用于控制機械臂沿所規劃的放療路徑移動所述放療組件以執行放療處理。
在一些示例中,所述輔助掃描組件可以是具有開放的上端和封閉的筒底的限光筒,所述限光筒的筒底可設置為貼合到所述待掃描區域上。
在一些示例中,所述成像控制模塊可配置為控制超聲組件、ct裝置、x光裝置、或mri裝置對所述待掃描區域進行掃描以獲得所述待掃描區域的多幅圖像。
在一些示例中,所述成像組件可以是超聲組件,所述成像控制模塊可配置為控制機械臂操縱所述超聲組件對所述待掃描區域進行掃描,以獲得所述待掃描區域的多幅圖像。
在一些示例中,在控制機械臂操縱所述超聲組件之前,所述成像控制模塊還可配置為基于所述輔助掃描組件和所述超聲組件的信息來規劃所述預定路徑。
在一些示例中,所述放療區域確定模塊可包括:圖像識別單元,配置為識別出所述3d模型中的待放療區域;以及放療區域選擇單元,配置為接收用戶對所述3d模型中的待放療區域的選擇。
在一些示例中,所述放療路徑規劃模塊可包括:子區域劃分單元,配置為將所述待放療區域劃分成若干個子區域;放療劑量確定單元,配置為確定用于每個子區域的放療劑量;以及放療路徑規劃單元,配置為通過調整強度和能量的方式,規劃放療組件經過每個子區域的掃描路徑和掃描方式,其中所述掃描方式包括步進式掃描和動態連續掃描。
在一些示例中,所述放療執行模塊可包括:機械臂控制單元,配置為控制機械臂沿所規劃的放療路徑移動所述放療組件;以及放療組件控制單元,配置為控制所述放療組件在移動時的放療強度和能量。
根據本申請一示例性實施例,一種術中放療系統可包括輔助掃描組件、成像組件、放療組件、機械臂、以及控制組件,所述控制組件可包括存儲器和處理器,所述處理器配置為運行所述存儲器上存儲的計算機指令以:控制所述成像組件透過所述輔助掃描組件對待掃描區域進行掃描,以獲得所述待掃描區域的多幅圖像,所述輔助掃描組件設置在所述待掃描區域上;基于所述待掃描區域的多幅圖像建立所述待掃描區域的3d模型;基于所述3d模型確定待放療區域;針對所述待放療區域規劃放療組件的移動路徑;以及控制所述機械臂沿所規劃的移動路徑移動所述放療組件,以對所述待放療區域進行放療處理。
在一些示例中,所述輔助掃描組件可以是具有開放的上端和封閉的筒底的限光筒,所述限光筒的筒底設置為貼合到所述待掃描區域上。
在一些示例中,所述成像組件可以是超聲組件、ct裝置、x光裝置、或mri裝置。
在一些示例中,所述成像組件可以是超聲組件,所述處理器可配置為控制所述機械臂在所述輔助掃描組件的內底壁上移動所述超聲組件,以獲得所述待掃描區域的多幅圖像。
在一些示例中,基于所述3d模型確定待放療區域可通過如下步驟來實現:通過圖像識別來直接識別出所述3d模型中的待放療區域;或者接收用戶對所述3d模型中的待放療區域的選擇;或者通過圖像識別來初步識別出所述3d模型中的待放療區域,然后接收用戶對初步識別的待放療區域的修改,以確定最終的待放療區域。
在一些示例中,針對所述待放療區域規劃放療組件的移動路徑可通過如下步驟來實現:將所述待放療區域劃分成若干個子區域;確定用于每個子區域的放療劑量;以及通過調整強度和能量的方式,規劃放療組件經過每個子區域的掃描路徑和掃描方式,其中所述掃描方式包括步進式掃描和動態連續掃描。
根據本申請一示例性實施例,一種計算機可讀存儲介質可存儲有計算機程序指令,所述計算機程序指令在被處理器運行時可使得所述處理器執行如上所述的方法。
在一些示例中,所述計算機程序指令在被處理器運行時還使得所述處理器執行如下步驟:控制機械臂沿所規劃的掃描路徑移動所述放療組件,以對所述待放療區域進行放療處理。
本發明的有益效果是:iort機械臂掃描方法可實現多自由度和高精度的機械掃描,此外,使用機械臂可在手術室復雜的環境下為術中放療建立統一坐標系,從而確定模擬定位和治療實施的空間位置關系。裝載有超聲組件的機械臂利用自動控制技術實現術中3d超聲影像獲取,超聲成像具有無輻射、軟組織分辨率高、設備體積小和成本低等優勢,并且術中3d影像的獲取有助于精確地確定待放療區域;裝載有治療組件的機械臂利用自動控制技術實現術中3d調強調能治療,在保證靶區處方劑量的同時有效地保護正常組織,滿足iort精確放療需求。
本申請的其它特征和優點將在隨后的說明書中闡述,并且,部分地從說明書中變得顯而易見,或者通過實施本申請而了解。本申請的目的和其它優點可通過在說明書、權利要求書以及附圖中所特別指出的結構來實現和獲得。
附圖說明
附圖用來提供對本申請的進一步理解,并且構成說明書的一部分,與本申請的實施例一起用于解釋本申請,并不構成對本申請的限制。
圖1示出執行術中放療掃描路徑規劃的術中放療系統。
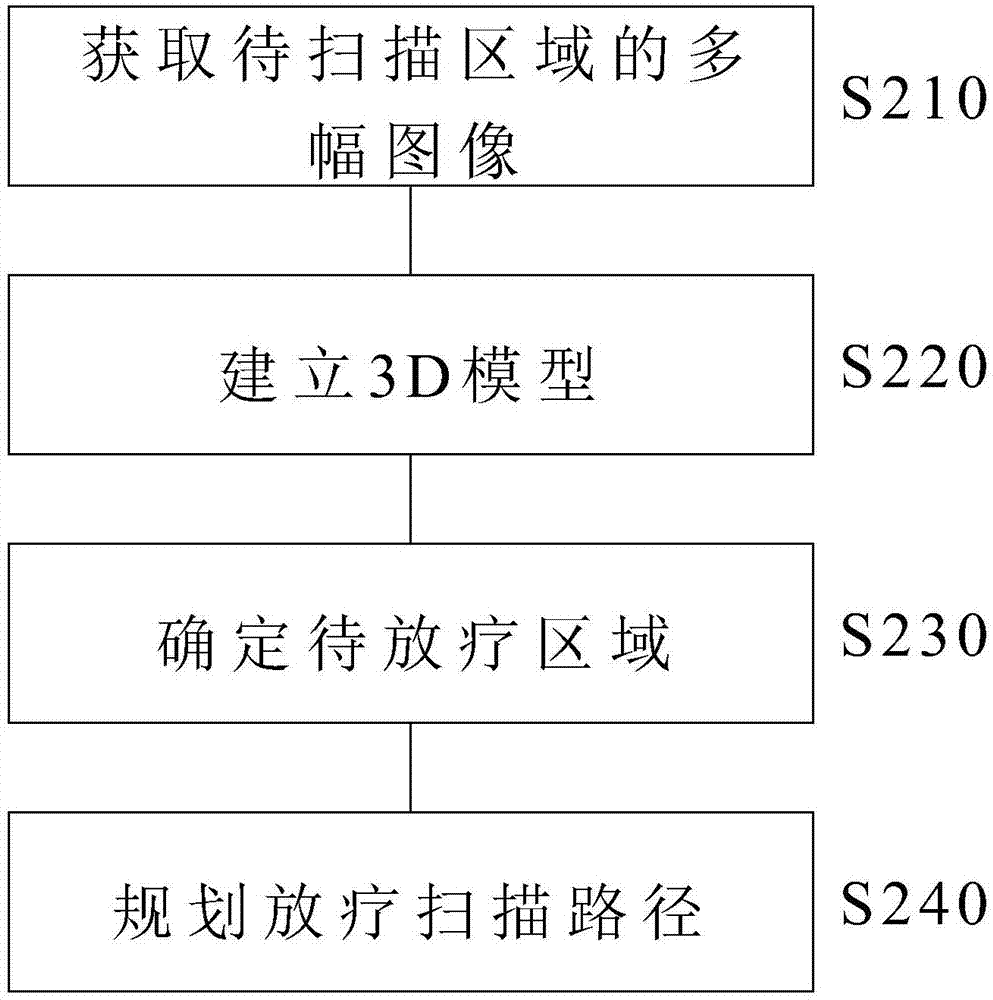
圖2示出術中放療掃描路徑規劃方法的流程圖。
圖3示出執行術中放療的術中放療系統。
圖4示出用于術中放療系統的控制裝置的框圖。
具體實施方式
下面將參照附圖詳細描述根據本申請的各個實施例。這里,需要注意的是,在附圖中,將相同的附圖標記賦予基本上具有相同或類似結構和功能的組成部分,并且將省略關于它們的重復描述。
圖1示出執行術中放療掃描路徑規劃的術中放療系統。如圖1所示,術中放療系統包括輔助掃描組件100、成像組件200、機械臂300、以及用于控制放療系統的控制組件800。此外,放療系統還可以包括放療組件600或700(如圖3所示),其將在后面再詳細地描述。
輔助掃描組件100可以是用于限定超聲掃描范圍的筒狀結構,其一般為圓筒形狀,也可以具有各種其他形狀,例如矩形或正方形等。例如,輔助掃描組件100可以為多功能限光筒,其具有開放的上端和封閉的筒底101。筒底101可以為平坦形狀,也可以為與成像組件200的成像端面相適應的弧形。筒底101優選由適于成像波束以及放療輻射束容易穿過的材料形成,其示例包括例如聚氨酯等。關于多功能限光筒的其他方面已在2016年8月24日公開的發明專利申請201610207427.8中得到了詳細的描述,所以這里不再重復描述。
如圖1所示,輔助掃描組件100(即,多功能限光筒)被擺放在患者400的待掃描區域上。應注意,輔助掃描組件100的擺放是在手術中進行的,例如在切除腫瘤之后進行,從而輔助掃描組件100的筒底101的外壁可以直接與待掃描區域(例如瘤床)緊密貼合,例如直接位于腫瘤殘余物或瘤床401的上方,這會帶來若干益處。例如,第一,由于在手術中進行,使得成像組件可以更貼近待掃描區域,從而獲得更清晰準確的圖像。第二,通過輔助掃描組件100與待掃描區域的緊密貼合,可以相對于輔助掃描組件100固定待掃描區域的位置,避免因待掃描區域的移動而對成像以及后面的放療帶來的不利影響。
在擺放輔助掃描組件100之后,術中放療系統就可以在控制組件800的控制下,執行各種功能操作,例如后面描述的術中放療掃描路徑規劃操作和術中放療操作。控制組件800可以是專用控制組件,其包括專用于控制術中放療系統的硬件,也可以是通用計算機,例如臺式計算機、筆記本計算機、平板計算機、甚至手機等,其通過運行計算機指令來控制術中放療系統的各種操作。
一般而言,控制組件800可包括存儲器810和處理器820。存儲器810可包括各種計算機可讀存儲介質,例如rom、ram、eeprom、磁盤、光盤、軟盤、閃存等。存儲器800中可存儲有計算機程序指令,處理器11可以運行這些程序指令,以實現下面將詳細描述的各種操作。存儲器800中還可以存儲有各種其他信息,例如術中放療系統的設備信息、其各種組件的參數信息、操作者信息、待放療患者信息等。
處理器820可以是中央處理單元(cpu)或者具有數據處理能力和/或指令執行能力的其他形式的處理單元,并且可以控制術中放療系統中的其他組件以執行期望的功能。雖然圖1示出了一個存儲器810和一個處理器820,但是控制組件800可包括多個存儲器810和多個處理器820,并且這些存儲器和處理器可以分布在不同的位置,例如位于機械臂300處的機械臂控制用處理器和存儲器,位于成像組件200處的成像組件控制用處理器和存儲器、以及位于放療組件600和700處的放療組件用處理器和存儲器等。就此而言,本發明無任何特殊限制,只要它們能夠實現下面將描述的各種功能即可。
雖然未示出,但是控制組件800還可具有各種接口。例如,與術中放療系統的各組件連接的接口、用于接收用戶輸入的接口(鍵盤、鼠標、音頻輸入接口等)、輸出接口(顯示器、打印機、揚聲器等)等。控制組件800還可通過例如網絡接口連接到醫院內管理系統或因特網等。為了簡單起見,下面將省略對這些接口的描述,然而應理解,本發明的許多功能可以借助于這些接口來實現,并且在本申請的教導下,對于本領域技術人員而言這些都是顯而易見的。
圖2示出術中放療掃描路徑規劃方法的流程圖。下面將參照圖1和圖2來描述根據本發明一些實施例的術中放療掃描路徑規劃方法。
首先,在步驟s210,透過輔助掃描組件100(如圖1所示,其設置在待掃描區域上)獲得待掃描區域的多幅圖像,這可利用成像組件200來進行。成像組件200可以是各種醫院內常用的成像組件,例如超聲組件、ct裝置、x光裝置、mri裝置等。由于本發明涉及術中放療,所以這些成像組件需要設置在手術室中。從便利的角度來說,超聲組件是優選的。下面將以超聲組件200為例來進行說明,但是應理解,在本發明的教導下,利用其他組件來進行成像的過程對于本領域技術人員而言也是顯而易見的。
如圖1所示,超聲組件200可安裝在機械臂300的末端,這可以由操作者手工安裝,也可以由控制組件800控制機械臂300來主動抓取位于預定位置處的超聲組件200。機械臂300的末端和超聲組件200上可以有匹配的接合特征,例如對應的凸起和凹陷,使得超聲組件200在機械臂300上的安裝位置是固定的。然后,可以將裝載有超聲組件200的機械臂300置于輔助掃描組件100的中心處,并且使超聲組件200的末端201與輔助掃描組件100的內底壁緊密貼合。如前所述,輔助掃描組件100的筒底可以具有與超聲組件200的末端相適應的弧形或平坦形狀等,以提高成像質量。
此時,可以初始化機械臂位置參數,將機械臂的當前位置設置為參考位置,即坐標系的原點,這便于之后機械臂的掃描運動。輔助掃描組件100的相關信息,例如外徑、內徑、底端材料和厚度等,以及超聲組件200的相關信息,例如超聲探頭外徑和超聲探頭初始位置等,可存儲在例如存儲器810中。因此,控制組件800可利用這些信息來規劃機械臂300的成像掃描路徑,以及超聲組件200的控制參數。
然后,控制組件800可以控制機械盤300沿所規劃的成像掃描路徑來移動超聲組件200,并且基于所確定的控制參數來控制超聲組件200,以獲得待掃描區域的多幅圖像,例如圖1所示的圖像500。超聲組件200可以是2d超聲組件或3d超聲組件,因此所獲得的多幅圖像可以是2d圖像,也可以是3d圖像。超聲組件200還可以包括多頻率探頭,例如單個多頻率超聲探頭或者多個不同頻率的單頻率超聲探頭的組合,以獲得不同頻率的圖像,這可以增加成像深度。
所獲得的多幅圖像可以存儲在例如存儲器810中,控制組件800可以基于這些圖像來建立待掃描區域的3d模型,從而完成步驟s220。
接下來,在步驟s230中,可以基于待掃描區域的3d模型來確定待放療區域。待放療區域可以是3d區域,例如立體腫瘤殘余物、組織等,也可以是基本2d的區域,例如瘤床等。可以通過多種方式來確定待放療區域,例如通過圖像識別技術來直接識別出3d模型中的腫瘤區域,將其作為待放療區域。替代地,可以由用戶例如用鼠標對3d模型中的特定區域進行選擇,將其作為待放療區域。再者,還可以采取這兩種方式的組合,即首先通過圖像識別技術來初步識別出3d模型中的待放療區域,然后由用戶對初步識別的待放療區域進行修改,以確定最終的待放療區域。這樣,可以兼顧效率和精度這兩方面。通過采用3d模型,可以適形地確定待掃描區域,例如圖1所示的區域401,而避免將區域401下方的正常組織402也確定為待掃描區域。
然后,在步驟s240中,可以針對所確定的待放療區域,規劃用于特定放療組件的放療掃描路徑。具體而言,放療掃描路徑規劃可通過下面的過程來完成。
首先,放療組件600例如限光筒或電子加速器700的相關信息已經存儲于例如存儲器810中,這些信息包括例如放療輻照束的光斑尺寸或直徑、強度范圍、強度調節精度、能量范圍、能量調節精度等。考慮到放療組件600的參數,可以將待放療區域401劃分為若干個子區域或者塊,其在附圖中由點403表示。可以理解,射束直徑越小,射束強度和能量調節精度越高,則子區域403可以越小,所劃分的子區域403的數量可以越多。
然后,可以為所確定的每個子區域分配放療劑量。此時,可以為所有的子區域403分配相同的劑量,也可以為不同的子區域403分配不同的劑量。例如,可以由用戶選取全部或一部分子區域403,并且為其指定劑量值。這樣,可以靈活地為待放療區域401的不同位置指定不同的劑量值,例如在鄰近正常組織402的區域分配較小的劑量以避免可能損失正常組織402。
最后,即可為放療組件600規劃經過每個子區域403的放療掃描路徑。此時,可以通過調整強度和能量的方式,規劃放療組件600經過每個子區域403的掃描路徑和掃描方式。可以理解,射束能量對應于放療深度,能量越高,放療深度越大。確定了強度和能量,即可確定每個子區域403的放療劑量。掃描方式可以包括步進式掃描和動態連續掃描。應注意,在確定射束強度和能量時,還應考慮輔助掃描組件100的筒底101的材料和厚度對射束的吸收或衰減作用。
雖然未示出,但是在完成了放療路徑規劃之后,還可以可選地對路徑規劃進行評估,例如評估附近的正常組織所受到的照射劑量。如果評估符合要求,例如附近正常組織受到的照射劑量較低,則路徑規劃符合要求,輸出或保存該路徑規劃;反之,如果評估不符合要求,例如附近正常組織受到的照射劑量較高,超出了規定閾值,則路徑規劃不符合要求,需要調整或重新規劃,例如減小正常組織附近區域的照射劑量等,直到評估符合要求為止。
這樣,就最終完成了放療路徑規劃。接下來,就可以利用所規劃的路徑來執行放療處理,如圖3所示。在圖3中,示出了將放療限光筒600作為放療組件安裝在機械臂300上,射束601通過限光筒600被引導至待放療區域401中的各個點403。當然,還可以采用其他放療組件,例如電子加速器700。
注意,在進行放療操作時,輔助掃描組件100仍保持為緊密貼合在待放療區域上,這可以帶來若干好處。例如,可以將待掃描區域保持在相對于輔助掃描組件100恒定的位置,由于成像組件200和放療組件600都可以相對于輔助掃描組件100定位,所以待掃描區域相對于成像組件200和放療組件600處于相同的位置。而且,輔助掃描組件100可以為成像組件200和放療組件600建立相同的坐標系。這些都有助于提高放療的精確度。
控制組件800根據所規劃的放療路徑,包括強度、能量、掃描方式等,來控制機械臂300和其上的放療組件600。這樣,可以完成對不規則放療區域401的調強調能放療操作,形成適形的劑量分布,有效地保護腫瘤或瘤床后方的正常組織402。
圖4示出可用于前述術中放療系統中以執行前述操作或實現前述功能的控制裝置10的框圖。應理解,控制裝置10可以作為軟件模塊集成到前述術中放療系統中,該軟件模塊可存儲在存儲器810中,其包括的計算機指令可以由例如處理器820運行以執行前述操作。另一方面,控制裝置10(包括其中的各個模塊和單元)也可以由專門的硬件或固件實現。控制裝置10的所有實現方式,包括軟件、硬件和固件等,都應理解為落入本發明的保護范圍內。
如圖4所示,控制裝置10可包括成像控制模塊20、建模模塊30、放療區域確定模塊40、放療路徑規劃模塊50、以及放療執行模塊60。
成像控制模塊20可用于前述成像操作。例如,成像控制模塊20可基于輔助掃描組件100和成像組件200的信息來規劃成像掃描路徑,并且可控制機械臂300來沿所規劃的路徑移動成像組件200,以透過輔助掃描組件100對待掃描區域進行成像掃描,從而獲得待掃描區域的多幅圖像500。然后,建模模塊30可基于多幅圖像500建立待掃描區域的3d模型。
放療區域確定模塊40可用于確定3d模型中的待放療區域。具體而言,放療區域確定模塊40可包括圖像識別單元42和放療區域選擇單元44。圖像識別單元42可基于圖像識別技術來自動識別出3d模型中的待放療區域,放療區域選擇單元44則可以接收用戶對放療區域的選擇,或者對圖像識別單元42所識別的待放療區域的修改。
放療路徑規劃模塊50可用于規劃放療組件對待放療區域進行掃描的路徑。具體而言,放療路徑規劃模塊50可包括子區域劃分單元52、放療劑量確定單元54和放療路徑規劃單元56。劃分單元52可以將所確定的待放療區域劃分成若干個子區域,放療劑量確定單元54可用于確定每個子區域的放療劑量,放療路徑規劃單元56可通過調整強度和能量的方式,規劃放療組件經過每個子區域的掃描路徑和掃描方式,其中所述掃描方式包括步進式掃描和動態連續掃描。
雖然未示出,但是在一些實施例中,控制裝置10還可包括評估單元,以用于對所規劃的放療路徑進行評估。如果所規劃的放療路符合要求,例如對周圍正常組織的潛在損傷可能性低,則可以將該路徑用于后面的放療處理;否則,則需要重新進行放療路徑規劃。
最后,放療執行模塊60可根據所規劃的放療路徑來控制機械臂和放療組件以執行放療處理。具體而言,放療執行模塊60可包括機械臂控制單元62和放療組件控制單元64。機械臂控制單元62可用于控制機械臂300沿所規劃的放療路徑移動放療組件600或700,放療組件控制單元64可控制放療組件在移動時的操作,例如控制其放療強度和能量等,從而實現調強調能放射治療。
上面簡要描述了控制裝置10中的各個模塊或單元的功能或操作。應理解,這些功能或操作已經在上面參照圖1-3得到了進一步的詳細描述,因此可以結合關于圖1-3的描述來理解控制裝置10中的各個模塊或單元的功能或操作的進一步細節。
除了上述方法和設備以外,本申請的實施例還可以是計算機程序產品,其包括計算機程序指令,所述計算機程序指令在被處理器運行時使得所述處理器執行上面描述的本申請各種實施例的術中放療系統執行的各種操作、步驟和功能。所述計算機程序產品可以以一種或多種程序設計語言的任意組合來編寫用于執行本申請實施例操作的程序代碼,所述程序設計語言包括面向對象的程序設計語言,諸如java、c++等,還包括常規的過程式程序設計語言,諸如“c”語言或類似的程序設計語言。程序代碼可以完全地在用戶計算設備上執行、部分地在用戶設備上執行、作為一個獨立的軟件包執行、部分在用戶計算設備上部分在遠程計算設備上執行、或者完全在遠程計算設備或服務器上執行。
此外,本申請的實施例還可以是計算機可讀存儲介質,其上存儲有計算機程序指令,所述計算機程序指令在被處理器運行時使得所述處理器執行上面描述的根據本申請各種實施例的術中放療系統執行的各種操作、步驟和功能。所述計算機可讀存儲介質可以采用一個或多個可讀介質的任意組合。可讀介質可以是可讀信號介質或者可讀存儲介質。可讀存儲介質例如可以包括但不限于電、磁、光、電磁、紅外線、或半導體的系統、裝置或器件,或者任意以上的組合。可讀存儲介質的更具體的例子(非窮舉的列表)包括:具有一個或多個導線的電連接、便攜式盤、硬盤、隨機存取存儲器(ram)、只讀存儲器(rom)、可擦式可編程只讀存儲器(eprom或閃存)、光纖、便攜式緊湊盤只讀存儲器(cd-rom)、光存儲器件、磁存儲器件、或者上述的任意合適的組合。
本發明的特征和優點還體現在下面描述的實施例中。
實施例1.一種術中放療掃描路徑規劃方法,包括:
透過輔助掃描組件獲得待掃描區域的多幅圖像;
基于所述待掃描區域的多幅圖像建立所述待掃描區域的3d模型;
基于所述3d模型確定待放療區域;以及
針對所述待放療區域規劃放療組件的掃描路徑。
實施例2.如實施例1所述的方法,其中,所述輔助掃描組件是具有開放的上端和封閉的筒底的限光筒,所述限光筒的筒底設置為貼合到所述待掃描區域上。
實施例3.如實施例1所述的方法,其中,透過輔助掃描組件獲得待掃描區域的多幅圖像包括:
利用超聲組件、ct裝置、x光裝置、或mri裝置來獲得所述待掃描區域的多幅圖像。
實施例4.如實施例1所述的方法,其中,透過輔助掃描組件獲得待掃描區域的多幅圖像包括:
利用機械臂操縱超聲組件在所述輔助掃描組件的內底壁上掃描,以獲得所述待掃描區域的多幅圖像。
實施例5.如實施例1所述的方法,其中,基于所述3d模型確定待放療區域包括:
由圖像識別模塊直接識別出所述3d模型中的待放療區域;或者
接收用戶對所述3d模型中的待放療區域的選擇;或者
由圖像識別模塊初步識別出所述3d模型中的待放療區域,然后接收用戶對圖像識別模塊初步識別的待放療區域的修改,以確定最終的待放療區域。
實施例6.如實施例1所述的方法,其中,針對所述待放療區域規劃放療組件的掃描路徑包括:
將所述待放療區域劃分成若干個子區域;
確定用于每個子區域的放療劑量;以及
通過調整強度和能量的方式,規劃放療組件經過每個子區域的掃描路徑和掃描方式,其中所述掃描方式包括步進式掃描和動態連續掃描。
實施例7.一種術中放療控制裝置,包括:
成像控制模塊,用于控制成像組件沿預定路徑移動并且透過輔助掃描組件對待掃描區域進行掃描,以獲得所述待掃描區域的多幅圖像;
建模模塊,用于基于所述多幅圖像建立所述待掃描區域的3d模型;
放療區域確定模塊,用于確定所述3d模型中的待放療區域;以及
放療路徑規劃模塊,用于規劃放療組件對所述待放療區域進行掃描的路徑。
實施例8.如實施例7所述的術中放療控制裝置,還包括:
放療執行模塊,用于控制機械臂沿所規劃的放療路徑移動所述放療組件以執行放療處理。
實施例9.如實施例7所述的術中放療控制裝置,其中,所述輔助掃描組件是具有開放的上端和封閉的筒底的限光筒,所述限光筒的筒底設置為貼合到所述待掃描區域上。
實施例10.如實施例7所述的術中放療控制裝置,其中,所述成像控制模塊配置為控制超聲組件、ct裝置、x光裝置、或mri裝置對所述待掃描區域進行掃描以獲得所述待掃描區域的多幅圖像。
實施例11.如實施例7所述的術中放療控制裝置,其中,所述成像組件是超聲組件,所述成像控制模塊配置為控制機械臂操縱所述超聲組件對所述待掃描區域進行掃描,以獲得所述待掃描區域的多幅圖像。
實施例12.如實施例11所述的術中放療控制裝置,其中,在控制機械臂操縱所述超聲組件之前,所述成像控制模塊還配置為基于所述輔助掃描組件和所述超聲組件的信息來規劃所述預定路徑。
實施例13.如實施例7所述的術中放療控制裝置,其中,所述放療區域確定模塊包括:
圖像識別單元,配置為識別出所述3d模型中的待放療區域;以及
放療區域選擇單元,配置為接收用戶對所述3d模型中的待放療區域的選擇。
實施例14.如實施例7所述的術中放療控制裝置,其中,所述放療路徑規劃模塊包括:
子區域劃分單元,配置為將所述待放療區域劃分成若干個子區域;
放療劑量確定單元,配置為確定用于每個子區域的放療劑量;以及
放療路徑規劃單元,配置為通過調整強度和能量的方式,規劃放療組件經過每個子區域的掃描路徑和掃描方式,其中所述掃描方式包括步進式掃描和動態連續掃描。
實施例15.如實施例8所述的術中放療控制裝置,其中,所述放療執行模塊包括:
機械臂控制單元,配置為控制機械臂沿所規劃的放療路徑移動所述放療組件;以及
放療組件控制單元,配置為控制所述放療組件在移動時的放療強度和能量。
實施例16.一種術中放療系統,包括輔助掃描組件、成像組件、放療組件、機械臂、以及控制組件,所述控制組件包括存儲器和處理器,所述處理器配置為運行所述存儲器上存儲的計算機指令以:
控制所述成像組件透過所述輔助掃描組件對待掃描區域進行掃描,以獲得所述待掃描區域的多幅圖像,所述輔助掃描組件設置在所述待掃描區域上;
基于所述待掃描區域的多幅圖像建立所述待掃描區域的3d模型;
基于所述3d模型確定待放療區域;
針對所述待放療區域規劃放療組件的移動路徑;以及
控制所述機械臂沿所規劃的移動路徑移動所述放療組件,以對所述待放療區域進行放療處理。
實施例17.如實施例16所述的放療系統,其中,所述輔助掃描組件是具有開放的上端和封閉的筒底的限光筒,所述限光筒的筒底設置為貼合到所述待掃描區域上。
實施例18.如實施例16所述的放療系統,其中,所述成像組件是超聲組件、ct裝置、x光裝置、或mri裝置。
實施例19.如實施例18所述的放療系統,其中,所述成像組件是超聲組件,所述處理器配置為控制所述機械臂在所述輔助掃描組件的內底壁上移動所述超聲組件,以獲得所述待掃描區域的多幅圖像。
實施例20.如實施例16所述的放療系統,其中,基于所述3d模型確定待放療區域是通過如下步驟來實現的:
通過圖像識別來直接識別出所述3d模型中的待放療區域;或者
接收用戶對所述3d模型中的待放療區域的選擇;或者
通過圖像識別來初步識別出所述3d模型中的待放療區域,然后接收用戶對初步識別的待放療區域的修改,以確定最終的待放療區域。
實施例21.如實施例16所述的放療系統,其中,針對所述待放療區域規劃放療組件的移動路徑是通過如下步驟來實現的:
將所述待放療區域劃分成若干個子區域;
確定用于每個子區域的放療劑量;以及
通過調整強度和能量的方式,規劃放療組件經過每個子區域的掃描路徑和掃描方式,其中所述掃描方式包括步進式掃描和動態連續掃描。
實施例22.一種計算機可讀存儲介質,其上存儲有計算機程序指令,所述計算機程序指令在被處理器運行時使得所述處理器執行如實施例1-6中的任一項所述的方法。
實施例23.如實施例22所述的計算機可讀存儲介質,其中,所述計算機程序指令在被處理器運行時還使得所述處理器執行如下步驟:
控制機械臂沿所規劃的掃描路徑移動所述放療組件,以對所述待放療區域進行放療處理。
在本說明書中,說明了大量的具體細節。然而,應當理解,本發明的實施方式可以在沒有這些具體細節的情況下實施。在一些實施方式中,并未詳細示出公知的方法、結構和技術,以便不使讀者混淆對本說明書的原理的理解。
本領域技術人員可以理解,可以對各實施方式中的裝置中的模塊進行自適應性地改變,并且把它們設置在與該實施方式不同的一個或多個裝置中。除了特征或處理相互排斥的情況之外,可以采用任何組合,對本說明書中公開的任何方法的所有步驟或者任何裝置的所有模塊進行組合。除非另外明確陳述,本說明書中公開的每個特征都可以由提供相同、等同或相似目的替代特征來代替。
應當注意,上述實施方式對本發明進行說明而不是對本發明進行限制,并且本領域技術人員在不偏離所附權利要求的范圍的情況下,可設計出各種替代實施方式。在權利要求書中,特征的排序并不意味著特征的任何特定順序,并且特別地,方法權利要求中各步驟的順序并不意味著這些步驟必須按照該順序來執行。相反地,這些步驟可以以任何適當的順序執行。在權利要求書中,不應將位于括號內的任何參考標記理解成對權利要求的限制。術語“包括”或“包含”不排除存在未列在權利要求中的模塊或步驟。位于模塊或步驟之前的術語“一”或“一個”不排除存在多個這樣的模塊或步驟。術語“第一”、“第二”、以及“第三”等的使用不表示任何順序,可將這些術語解釋為名稱。
- 還沒有人留言評論。精彩留言會獲得點贊!