鈦合金金標植入體及金標注射器的制作方法
本發明涉及醫療器械領域,特別涉及一種鈦合金金標植入體及金標注射器。
背景技術:
為了高精度照射軟組織中的腫瘤,需要在腫瘤內或旁植入金標,治療中通過對金標的追蹤實現對腫瘤的動態追蹤。
金標植入一周后,與腫瘤形成相對穩定的幾何關系,在治療中確定了金標位置也就確定了腫瘤的位置,金標的動度也就代表腫瘤的動度。
但是金標在植入腫瘤組織或其周圍特定軟組織后,金標物容易發生移動,若移位發生在治療前,不會帶來風險,但可能會引起照射精度的下降,可以通過再次植入金標來解決;若在治療中發生移位,可能會影響治療的安全性和準確性,并且金標移動則照射位置也發生改變,可能引起放射性損傷甚至事故。因此,無論金標移位發生在治療前,還是治療中,都要積極采取措施,避免治療的安全性和精確性受到影響。
技術實現要素:
本發明的目的在于提供一種鈦合金金標植入體及金標注射器,以解決現有技術中存在上述的技術問題。
本發明提供的鈦合金金標植入體,包括金標本體,所述金標本體由鈦合金制成,所述金標本體包括弧形連接桿,所述弧形連接桿兩端分別固設有球體,所述球體的直徑大于所述弧形連接桿的直徑。
進一步地,所述金標本體上設有凸起。
進一步地,所述凸起為十字形凸起。
進一步地,所述凸起為人字形凸起。
進一步地,所述凸起為V字形凸起。
進一步地,所述金標本體上設有納米藥物層。
進一步地,所述納米藥物層通過連接劑層粘接到所述金標本體上。
進一步地,所述連接劑層為生物粘合劑層。
進一步地,所述生物粘合劑層為纖維蛋白原層、凝血酶層、酪蛋白層、殼多糖層或殼聚糖層。
本發明提供的鈦合金金標植入體,具有如下優點:
通過弧形連接桿兩端的球體增加金標本體與植入的腫瘤組織或其周圍的特定軟組織的穩定性,使金標本體不易發生移動,提高治療的安全性和準確性,由于金標本體不易移動,降低在治療過程中因金標本體發生移動使照射位置發生改變,可能引起放射性損傷甚至事故出現的概率。
另外,本發明還提供了一種金標注射器,包括注射針體以及上述鈦合金金標植入體,所述金標本體放置在所述注射針體內。
附圖說明
為了更清楚地說明本發明具體實施方式或現有技術中的技術方案,下面將對具體實施方式或現有技術描述中所需要使用的附圖作簡單地介紹,顯而易見地,下面描述中的附圖是本發明的一些實施方式,對于本領域普通技術人員來講,在不付出創造性勞動的前提下,還可以根據這些附圖獲得其他的附圖。
圖1為本發明實施例一提供的鈦合金金標植入體的結構主視圖;
圖2為本發明實施例二提供的鈦合金金標植入體的結構主視圖;
圖3為本發明實施例三提供的鈦合金金標植入體的結構主視圖;
圖4為本發明實施例四提供的鈦合金金標植入體的結構主視圖;
圖5為本發明實施例五提供的鈦合金金標植入體的結構主視圖;
圖6為圖5的局部放大圖A;
圖7本發明實施例六提供的金標注射器的結構主視圖;
圖8為圖7的局部放大圖B。
附圖標記:
1-金標本體; 11-弧形連接桿; 12-球體;
13-凸起; 2-納米藥物層; 3-連接劑層;
4-注射針體; 41-套管; 42-中空手柄;
43-推進器; 411-尖部; 44-推送桿;
45-推拉頭。
具體實施方式
下面將結合附圖對本發明的技術方案進行清楚、完整地描述,顯然,所描述的實施例是本發明一部分實施例,而不是全部的實施例。基于本發明中的實施例,本領域普通技術人員在沒有做出創造性勞動前提下所獲得的所有其他實施例,都屬于本發明保護的范圍。
在本發明的描述中,需要說明的是,術語“中心”、“上”、“下”、“左”、“右”、“豎直”、“水平”、“內”、“外”等指示的方位或位置關系為基于附圖所示的方位或位置關系,僅是為了便于描述本發明和簡化描述,而不是指示或暗示所指的裝置或元件必須具有特定的方位、以特定的方位構造和操作,因此不能理解為對本發明的限制。此外,術語“第一”、“第二”、“第三”僅用于描述目的,而不能理解為指示或暗示相對重要性。
在本發明的描述中,需要說明的是,除非另有明確的規定和限定,術語“安裝”、“相連”、“連接”應做廣義理解,例如,可以是固定連接,也可以是可拆卸連接,或一體地連接;可以是機械連接,也可以是電連接;可以是直接相連,也可以通過中間媒介間接相連,可以是兩個元件內部的連通。對于本領域的普通技術人員而言,可以根據具體情況理解上述術語在本發明中的具體含義。
實施例一:
圖1為本發明實施例一提供的鈦合金金標植入體的結構主視圖;如圖1所示,本發明提供的鈦合金金標植入體,包括金標本體1,所述金標本體1由鈦合金制成,所述金標本體1包括弧形連接桿11,所述弧形連接桿11兩端分別固設有球體12,所述球體12的直徑大于所述連接桿11的直徑。
鈦是20世紀50年代發展起來的一種重要的結構金屬,鈦合金因具有強度高、耐蝕性好、耐熱性高等特點而被廣泛用于各個領域。世界上許多國家都認識到鈦合金材料的重要性,相繼對其進行研究開發,并得到了實際應用。20世紀50~60年代,主要是發展航空發動機用的高溫鈦合金和機體用的結構鈦合金,70年代開發出一批耐蝕鈦合金,80年代以來,耐蝕鈦合金和高強鈦合金得到進一步發展。鈦合金主要用于制作飛機發動機壓氣機部件,其次為火箭、導彈和高速飛機的結構件。
本發明提供的鈦合金金標植入體,具有如下優點:
通過弧形連接桿11兩端的球體12增加金標本體與植入的腫瘤組織或其周圍的特定軟組織的穩定性,使金標本體不易發生移動,提高治療的安全性和準確性,由于金標本體不易移動,降低在治療過程中因金標本體發生移動使照射位置發生改變,可能引起放射性損傷甚至事故出現的概率。
實施例二:
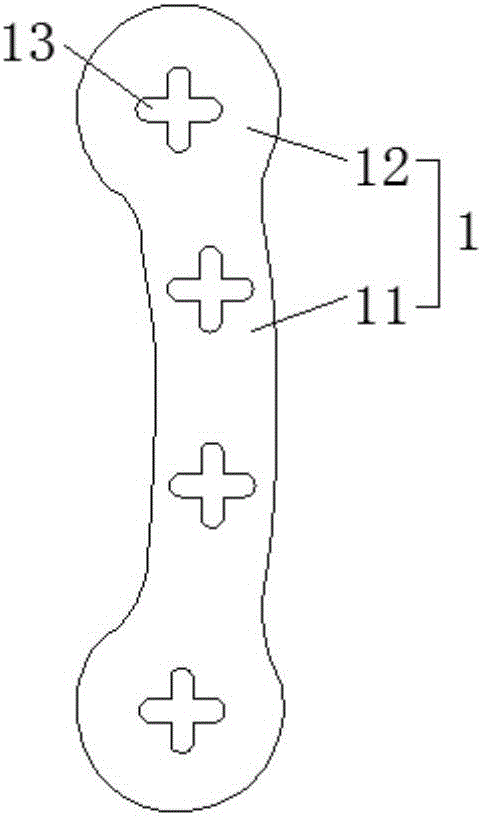
圖2為本發明實施例二提供的鈦合金金標植入體的結構主視圖;如圖2所示,本發明提供的鈦合金金標植入體,包括金標本體1,所述金標本體1由鈦合金制成,所述金標本體1包括弧形連接桿11,所述弧形連接桿11兩端分別固設有球體12,所述球體12的直徑大于所述弧形連接桿11的直徑。
金標本體1的長度為0.1mm-10mm,直徑為0.1mm-1.5mm。
所述金標本體1上設有凸起13。
所述凸起13為十字形凸起。
通過金標本體1上的凸起13進一步增加與植入的腫瘤組織或其周圍的特定軟組織的穩定性。
實施例三:
圖3為本發明實施例三提供的鈦合金金標植入體的結構主視圖;如圖3所示,本發明提供的鈦合金金標植入體,包括金標本體1,所述金標本體1由鈦合金制成,所述金標本體1包括弧形連接桿11,所述弧形連接桿11兩端分別固設有球體12,所述球體12的直徑大于所述弧形連接桿11的直徑。
所述金標本體1上設有凸起13。
所述凸起13為人字形凸起。
實施例四:
圖4為本發明實施例四提供的鈦合金金標植入體的結構主視圖;如圖4所示,本發明提供的鈦合金金標植入體,包括金標本體1,所述金標本體1由鈦合金制成,所述金標本體1包括弧形連接桿11,所述弧形連接桿11兩端分別固設有球體12,所述球體12的直徑大于所述弧形連接桿11的直徑。
所述金標本體1上設有凸起13。
所述凸起13為V字形凸起。
需要說明的是,凸起13的形狀和結構除了十字形、人字形和V字形以外,還可采用其他形狀,在此就不一一舉例。
實施例五:
圖5為本發明實施例五提供的鈦合金金標植入體的結構主視圖,圖6為圖5的局部放大圖A,如圖5-6所示,本發明提供的鈦合金金標植入體,包括金標本體1,所述金標本體1由鈦合金制成,所述金標本體1包括弧形連接桿11,所述弧形連接桿11兩端分別固設有球體12,所述球體12的直徑大于所述弧形連接桿11的直徑。
所述金標本體1上設有納米藥物層2。
所述納米藥物層2通過連接劑層3粘接到所述金標本體1上。
所述連接劑層3為生物粘合劑層。
所述生物粘合劑層為纖維蛋白原層、凝血酶層、酪蛋白層、殼多糖層或殼聚糖層。
膠原蛋白是生物高分子,動物結締組織中的主要成分,也是哺乳動物體內含量最多、分布最廣的功能性蛋白,占蛋白質總量的25%~30%,某些生物體甚至高達80%以上。
膠原蛋白種類較多,常見類型為Ⅰ型、Ⅱ型、Ⅲ型、Ⅴ型和Ⅺ型。
膠原蛋白因具有良好的生物相容性、可生物降解性以及生物活性,因此在食品、醫藥、組織工程、化妝品等領域獲得廣泛的應用。比如中國傳統的膠原保健品“阿膠”,主要是以驢皮為原料(其實就是驢皮中所含膠原蛋白),具有較高的滋補保健作用,有中藥三寶之一的美譽。
凝血酶:是一種在人體抗凝,促凝的凝血級聯反應中有著重要作用的生物活性蛋白。
酪蛋白層:酪蛋白是一種含磷鈣的結合蛋白,對酸敏感,pH較低時會沉淀。
酪蛋白是哺乳動物包括母牛,羊和人奶中的主要蛋白質,又稱:干酪素、酪朊、乳酪素。
殼多糖層:殼多糖(chitin)又稱幾丁質。為N-乙酰葡糖胺通過β連接聚合而成的結構同多糖。廣泛存在于甲殼類動物的外殼、昆蟲的甲殼和真菌的胞壁中,也存在于一些綠藻中;主要是用來作為支撐身體骨架,以及對身體起保護的作用。
殼聚糖層:殼聚糖(chitosan)又稱脫乙酰甲殼素,是由自然界廣泛存在的幾丁質(chitin)經過脫乙酰作用得到的,化學名稱為聚葡萄糖胺(1-4)-2-氨基-B-D葡萄糖。
自1859年,法國人Rouget首先得到殼聚糖后,這種天然高分子的生物官能性和相容性、血液相容性、安全性、微生物降解性等優良性能被各行各業廣泛關注,在醫藥、食品、化工、化妝品、水處理、金屬提取及回收、生化和生物醫學工程等諸多領域的應用研究取得了重大進展。針對患者,殼聚糖降血脂、降血糖的作用已有研究報告。同時,殼聚糖被作為增稠劑、被膜劑列入國家食品添加劑使用標準GB-2760。
納米藥物,指通過一定的微細加工方式直接操縱原子、分子或原子團、分子團,使其重新排列組合,形成新的具有納米尺度的物質或結構,一種具有同生物膜性質類似的磷脂雙分子層結構載體的藥物。
在藥物研究領域,由于納米技術的不斷滲透和影響,引發了藥物領域一場深遠的革命,從而出現了納米藥物這一新名詞。
納米藥物是指以納米級高分子納米粒(nano-particles,NP)、納米球(nano.spheres NS)、納米囊(nano-capsules,NC)等為載體,與藥物以一定方式結合在一起后制成的藥物,其粒徑可能超過100nm,但通常應小于500nm。納米藥物也可以是直接將原料藥物加工制成的納米粒。
納米藥物的應用不僅改善了藥物劑型的理化特性,而且提高了藥物的靶向性、緩釋性等。研究顯示納米顆粒具有將高濃度藥物直接作用于癌細胞而又避開健康組織的能力。
納米藥物的特性:
1)磁場作用下的靶向性利用納米載體與磁性物質結合,使其具有磁性。
同時,由體外附加磁場,或者通過手術植入具有磁場效應的導管、支架等材料在體內特定區域形成磁場。將靶器官暴露于磁場中,以此控制磁性納米載體在體內的分布,使其集中分布于靶器官。
有研究顯示磁性納米載體能借助磁場使其所裝載的化療藥物定向集中于靶向部位(腫瘤組織),提高靶向部位的藥物濃度、增強治療效果,同時降低其它部位的藥物濃度,減少毒副反應。
2)主動靶向性將單克隆抗體共價交聯或吸附到納米粒表面,形成具有免疫活性納米粒,并應用于抗腫瘤藥物的研究也取得了一定的結果。
2、納米藥物的控釋性
因很多化療藥物半衰期短、維持其有效抗腫瘤濃度時間較短。有些化療藥物只對處于特定增殖周期的腫瘤細胞發揮作用,而對其他增殖周期的細胞不發揮作用,然而腫瘤細胞的細胞周期通常是不同步的,因此,維持較長時間有效的血藥濃度對于腫瘤治療也非常重要。
3、納米藥物吸收率高
納米藥物有助于提高藥物的吸收率,載藥納米粒可以改變膜運轉機制,增加藥物對生物膜的透過性,有利于藥物透皮吸收及細胞內藥效的發揮。
如裝載抗腫瘤藥物阿霉素的納米粒可使其藥效較普通阿霉素增加10倍,原因在于載藥納米粒的粘附性及其小的粒徑能夠延長藥物滯留時間,增加藥物與腸壁的接觸時間和接觸面積,提高其口服吸收的生物利用率。
4、納米抗腫瘤藥物代表
目前基于納米技術的臨床抗腫瘤藥物代表為脂質體阿霉素、白蛋白結合型紫杉醇。
其中脂質體阿霉素為阿霉素與脂質納米顆粒結合起來改變了藥物的生物分布,從而減少了阿霉素的心臟毒性,白蛋白結合型紫杉醇也消除了化療藥物和有機溶劑聚氧乙烯蓖麻油的不良反應,可以不需要使用任何溶劑直接應用。
目前正在研發的藥物還有BIND-014,該藥物為靶向前列腺特異性膜抗原(PSMA)的含有多西他賽的納米顆粒藥物。
已有研究顯示該藥物在晚期實體瘤患者中取得了很好的安全性、耐受性以及有效性的結果。
另一種藥物填充金元素的納米顆粒被證實能夠殺死培養的人細胞中的Bb細胞淋巴瘤,在未化療的情況下能夠抑制小鼠體內人B細胞淋巴瘤的生長。
而正在研發的覆蓋有膀胱癌特異性配體并荷載紫杉醇的靶向性顆粒將3倍最大耐受劑量的藥物輸送至移植了患者腫瘤的小鼠,獲得了良好的疾病控制并且不良反應可耐受。
在多發性骨髓瘤的治療方面,納米顆粒也顯示出了一定的潛力,克服了應用多柔比星引起的耐藥問題,經過納米顆粒避免了其中一個耐藥受體極遲抗原-4(VLA-4)與微環境相互作用,更直接、更有效地靶向作用于腫瘤。
實施例六:
圖7為本發明實施例六提供的金標注射器的結構主視圖,圖8為圖7的局部放大圖B;如圖7-圖8所示,本發明提供的金標注射器,包括注射針體4以及上述鈦合金金標植入體,所述金標本體1放置在所述注射針體4內。
所述注射針體4包括套管41、中空手柄42、推進器43和推送桿44,套管41端部設有尖部411,套管41另一端連接中空手柄42,推進器43設置在套管41內,推進器43距套管41端部之間留有用于放置金標本體1的空隙,推送桿44一端與推進器43連接,推送桿44另一端穿過中空手柄42并安裝推拉頭45。
使用時,將金標本體1裝入套管41前端部的空隙內,將套管41穿刺到需要標記的病變器官內,推動推拉頭45帶動推送桿44從而帶動推進器43將金標本體1推出套管并注入病變器官內。
最后應說明的是:以上各實施例僅用以說明本發明的技術方案,而非對其限制;盡管參照前述各實施例對本發明進行了詳細的說明,本領域的普通技術人員應當理解:其依然可以對前述各實施例所記載的技術方案進行修改,或者對其中部分或者全部技術特征進行等同替換;而這些修改或者替換,并不使相應技術方案的本質脫離本發明各實施例技術方案的范圍。
- 還沒有人留言評論。精彩留言會獲得點贊!