一種治療糖尿病腎病的中藥丸劑及其制備方法和應用與流程
本發明屬于醫藥領域,具體是涉及一種治療糖尿病腎病的中藥丸劑及其制備方法和應用。
背景技術:
糖尿病腎病(dkd)是糖尿病(dm)最主要的微血管并發癥之一,為終末期腎病(esrd)的首要病因。糖尿病腎病中的微血管病變是指腎小球硬化,分結節性、滲出性和彌漫性三種,三者可單獨存在,也可合并存在。據統計,目前全球dm患者人數已達4.15億,預計2040年將增至6.42億,其中,20%~45%的dm患者將發生dkd。我國dm患者已經達1.1億,且發病率逐年上升。2012年我國esrd患者中19%是dkd導致,在日本、韓國、美國、澳大利亞等發達國家,這一比例高達38%~45.2%。dkd已成為威脅人類健康的重大社會問題,給社會和個人造成了巨大經濟負擔。
臨床上,糖尿病腎病主要表現為蛋白尿、高血壓及進行性腎功能損害。該病的病理體現在腎小球系膜細胞增殖、腎小球毛細血管氧化應激增加及細胞凋亡等癥狀。其中,晚期糖基化終末產物(advancedglycationendproducts,ages)參與了糖尿病腎病的發病過程,是顯著的致病因素。
dkd的治療,西醫以控制血糖、控制血壓和減少尿蛋白為主,還包括生活方式干預、糾正脂質代謝紊亂、治療腎功能不全的并發癥及透析治療等。西醫的治療方法在一定程度上解決了dkd患者血壓高及蛋白尿等臨床問題,但均不能有效阻止疾病進展,甚至導致藥源性腎病,部分藥物的應用尚存在爭議,且容易出現高鉀血癥、高肌酐血癥等副作用,使用期間需嚴格監測血鉀、血清肌酐水平,限制其臨床使用。
技術實現要素:
基于此,本發明的目的在于提供一種治療糖尿病腎病的中藥丸劑及其制備方法和應用。
實現上述目的的具體技術方案如下:
一種治療糖尿病腎病的中藥丸劑,其由活性成分、占總量質量百分比20-70%的稀釋劑、占總量質量百分比0-6%的抗黏劑以及潤濕劑制備而成;所述稀釋劑為微晶纖維素,所述抗黏劑為滑石粉,所述潤濕劑為水,所述活性成分為中藥組合物,所述中藥組合物的有效成分由以下質量份的原料制備而成,黃芪0.5-1.5份、葛根1.5-2.5份和桑白皮0.5-1.5份。
在其中一個實施例中,所述微晶纖維素占總量的質量百分比為38-60%,所述滑石粉占總量的質量百分比為2-5%。
在其中一個實施例中,所述微晶纖維素占總量的質量百分比為38-42%。
一種治療糖尿病腎病的中藥丸劑的制備方法,包括如下步驟:
s1、稱取黃芪0.5-1.5份、葛根1.5-2.5份和桑白皮0.5-1.5份,加1~15倍量溶劑回流提取,濾過,得粗濾液;
s2、將所述粗濾液通過陶瓷膜過濾,收集濾液,回收溶劑并濃縮,得浸膏;
s3、將所述浸膏、微晶纖維素、滑石粉和適量水混勻制軟材,擠出滾圓成微丸,干燥,篩分;
s4、將篩分后的微丸進行包薄膜衣,干燥,即得。
在其中一個實施例中,所述微晶纖維素占總量的質量百分比為20-70%,所述滑石粉占總量的質量百分比為0-6%。
在其中一個實施例中,所述微晶纖維素占總量的質量百分比為38-60%,所述滑石粉占總量的質量百分比為2-5%。
在其中一個實施例中,所述微晶纖維素占總量的質量百分比為38-42%。
在其中一個實施例中,在步驟s1中,所述溶劑為5~95%乙醇水溶液,所述回流提取的次數為1-5次,每次提取1-5小時;
在步驟s2中,所述陶瓷膜的孔徑為20~300nm;
在步驟s3中,所述擠出滾圓的工藝參數為擠出速度10~50rpm、滾圓時間2~10min和滾圓速度600~1500rpm,50~80℃干燥2~6小時;
在步驟s4中,所述薄膜包衣的工藝參數為進風頻率800~2000rpm、出風頻率800~2000rpm、霧化壓力0.2~0.5mpa、包衣液流速2~8rpm及物料溫度40~65℃。
在其中一個實施例中,在步驟s1中,所述乙醇水溶液的濃度為60~80%,所述回流提取的次數為2-3次,每次提取2-3小時;
在步驟s2中,所述陶瓷膜的孔徑為20~100nm;
在步驟s3中,所述擠出滾圓的工藝參數為擠出速度20~40rpm、滾圓時間5~8min和滾圓速度800~1200rpm,50~70℃干燥2~4小時;
在步驟s4中,所述薄膜包衣的工藝參數為進風頻率1000~2000rpm、出風頻率1000~2000rpm、霧化壓力0.2~0.4mpa、包衣液流速3~6rpm及物料溫度40~50℃。
上述治療糖尿病腎病的中藥丸劑在制備治療糖尿病腎病的藥物中的應用。
與現有技術相比,本發明具有以下有益效果:
本發明提供了一種治療糖尿病腎病的中藥丸劑,其由活性成分、稀釋劑、抗黏劑以及潤濕劑制備而成,所述活性成分為黃芪、葛根和桑白皮中制備的中藥組合物,選用微晶纖維素作為稀釋劑,選用滑石粉作為抗黏劑,載藥量高,產品收率高,包衣效率高。尤其當采用當微晶纖維素的用量為38-60%且滑石粉的用量在2-5%時,微丸的收率在92.1-97.5%之間,包衣效率在95.7-97.6%之間,粒徑在0.5-2mm之間,產品質量均一、穩定且可控。通過細胞試驗研究發現:在由ages即糖基化終產物制備的糖尿病腎病模型的細胞試驗中,該活性成分具有明顯的抗細胞氧化、抗細胞凋亡和抗細胞膜負電荷減少的作用,且量效關系顯著,能夠有效保護腎臟細胞的結構屏障和電荷屏障。在stz-cfa加高脂質聯合誘導的糖尿病腎病的動物模型試驗中,該中藥丸劑能夠明顯降低模型動物的尿總蛋白、尿微白蛋白、尿肌苷、尿素氮水平和肌酐清除率,能夠明顯降低模型動物血清中的mda、chol、ldl、ages、il-6、tnf-α水平,升高血清中sod、血肌酐水平,能夠降低糖尿病腎病的動物模型中腎臟he染色病理評分,明顯改善pas染色陽性百分率,具有明顯的保護腎臟的作用。
本發明提供的中藥丸劑的制備方法采用超濾技術能夠富集有效成分,所得中藥組合物的浸膏直接與微晶纖維素和滑石粉配合進行擠出滾圓制粒并包薄膜衣,載藥量高,產品收率高,包衣效率高。該制備方法具有操作簡單和工藝穩定的優點。
附圖說明
圖1為組合物對ages誘導huvec細胞氧化應激的影響,其中,a:陽性染色百分率;b:細胞照片(dihydroethidium染色,20倍物鏡)a:空白組,b:模型組,c:陽性藥組,d-h:組合物組(濃度分別為10、1、0.1、0.01、1x10-3g/l);
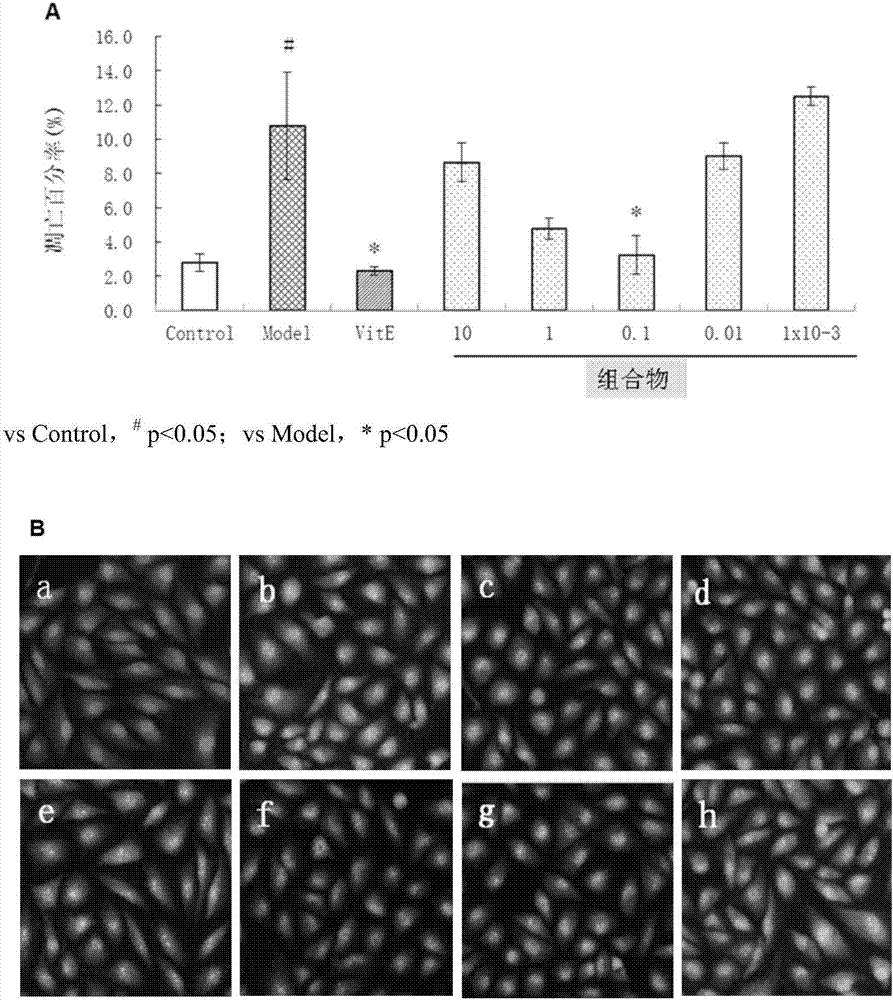
圖2為組合物對ages誘導huvec細胞凋亡的影響,其中,a:陽性染色百分率;b:細胞照片(ao-eb染色,20倍物鏡)a:空白組,b:模型組,c:陽性藥組,d-h:組合物組(濃度分別為10、1、0.1、0.01、1x10-3g/l);
圖3為組合物對ages誘導huvec細胞膜負電荷減少的影響,其中,a:陽性染色百分率;b:細胞照片(ab染色,20倍物鏡)a:空白組,b:模型組,c:陽性藥組,d-h:組合物組(濃度分別為10、1、0.1、0.01、1x10-3g/l);
圖4為stz-cfa聯合誘導的糖尿病腎病模型大鼠腎臟病理學的影響的照片(he染色,200倍),其中,a:正常組,b:模型組,c:厄貝沙坦組,d-e:組合物組;
圖5為stz-cfa聯合誘導的糖尿病腎病模型大鼠腎臟病理學的影響的照片(pas染色,200倍),其中,a:正常組,b:模型組,c:厄貝沙坦組,d-e:組合物組。
具體實施方式
以下結合具體實施例對本發明做進一步的闡述。
(一)中藥丸劑的制備
1試驗材料
1.1儀器
中藥多功能提取回流濃縮機組(湖南金一帆制藥設備實業有限公司,rzz湘-082-06)。
多功能制丸包衣機(深圳市信宜特科技有限公司,mini-250)。
1.2原輔料
黃芪(亳州市惠康中藥飲片有限公司);
葛根(亳州市惠康中藥飲片有限公司);
桑白皮(亳州市惠康中藥飲片有限公司);
乙醇(廣東順冠氣體溶劑有限公司生產);
微晶纖維素(安徽山河藥用輔料股份有限公司生產);
淀粉(安徽山河藥用輔料股份有限公司生產);
糊精(安徽山河藥用輔料股份有限公司生產);
滑石粉(廣西龍勝華美滑石開發有限公司生產);
包衣液(上海卡樂康包衣技術有限公司生產)。
實施例1
取黃芪2.5kg、葛根5.0kg、桑白皮2.5kg,加8倍量70%乙醇回流提取兩次,每次3小時,濾過,合并濾液,50nm陶瓷膜過濾,收集濾液,回收乙醇并濃縮(溫度:70℃;氣壓:-0.8~-0.6mpa)至相對密度1.32~1.35(70℃),收膏備用。同法制得三份:浸膏1、浸膏2和浸膏3。
取上述三批浸膏,分別加入占總量40~60%的微晶纖維素、淀粉和糊精,各加入5%的滑石粉作為抗黏劑,混勻,加適量水制軟材,擠出滾圓成微丸,此步驟的工藝參數為:擠出速度35rpm、滾圓時間4min、滾圓速度1000rpm。60±10℃干燥3小時,過18和24目篩,取能通過18目篩而不能通過24目篩的微丸,進行包薄膜衣。薄膜包衣的工藝參數為:進風頻率1500rpm、出風頻率1500rpm、霧化壓力0.3mpa、包衣液流速4rpm和物料溫度45℃。干燥,過16和24目篩,收集通過16目篩而不能通過24目篩的微丸,質檢,包裝,即得成品。
結果:分別單獨選用上述三種稀釋劑制備微丸時,微晶纖維素的最高載藥量為60%;淀粉最高載藥量為40%;糊精最高載藥量為38%。,其中,最高載藥量指的是在保證可以制成丸劑的基礎上,選用輔料可允許加入中藥提取物的量。
實施例2
取黃芪2.5kg、葛根5.0kg、桑白皮2.5kg,加8倍量70%乙醇回流提取兩次,每次3小時,濾過,合并濾液,50nm陶瓷膜過濾,收集濾液,回收乙醇并濃縮(溫度:70℃;氣壓:-0.8~-0.6mpa)至相對密度1.32~1.35(70℃),收膏備用。同法制得三份:浸膏1、浸膏2和浸膏3。
取以上三批浸膏,分別考察微晶纖維素、淀粉和糊精對微丸收率的影響,各加入5%的滑石粉作為抗黏劑,使載藥量為50%,混勻,加適量水制軟材,擠出滾圓成微丸,此步驟的工藝參數為:擠出速度35rpm、滾圓時間4min、滾圓速度1000rpm。60±10℃干燥3小時,過18和24目篩,取能通過18目篩而不能通過24目篩的微丸,進行包薄膜衣。薄膜包衣的工藝參數為:進風頻率1500rpm、出風頻率1500rpm、霧化壓力0.3mpa、包衣液流速4rpm和物料溫度45℃。干燥,過16和24目篩,收集通過16目篩而不能通過24目篩的微丸,質檢,包裝,即得成品。
結果:微晶纖維素的微丸收率為94±5%;淀粉和糊精均無法成型。
實施例3
取黃芪2.5kg、葛根5.0kg、桑白皮2.5kg,加8倍量70%乙醇回流提取兩次,每次3小時,濾過,合并濾液,50nm陶瓷膜過濾,收集濾液,回收乙醇并濃縮(溫度:70℃;氣壓:-0.8~-0.6mpa)至相對密度1.32~1.35(70℃),收膏備用。
取以上浸膏,加入占總量40%的微晶纖維素和5%的滑石粉,混勻,加適量水制軟材,擠出滾圓成微丸,此步驟的工藝參數為:擠出速度35rpm、滾圓時間4min、滾圓速度1000rpm。60±10℃干燥3小時,過18和24目篩,取能通過18目篩而不能通過24目篩的微丸,進行包薄膜衣。薄膜包衣的工藝參數為:進風頻率1500rpm、出風頻率1500rpm、霧化壓力0.3mpa、包衣液流速4rpm和物料溫度45℃。干燥,過16和24目篩,收集通過16目篩而不能通過24目篩的微丸,質檢,包裝,即得成品。
結果:滾圓后微丸的粒徑1mm,微丸收率為97.5%,包衣增重3%,包衣效率為97.6%,成品檢驗合格。
實施例4
取黃芪2.5kg、葛根5.0kg、桑白皮2.5kg,加1倍量5%乙醇回流提取5小時,濾過,合并濾液,300nm陶瓷膜過濾,收集濾液,回收乙醇并濃縮(溫度:70℃;氣壓:-0.8~-0.6mpa)至相對密度1.35~1.40(70℃),收膏備用。
取以上浸膏,加65%微晶纖維素,混勻,加適量水制軟材,擠出滾圓成微丸,該步驟工藝參數為:擠出速度10rpm、滾圓時間10min、滾圓速度600rpm。60±10℃干燥3小時,過18和24目篩,取能通過18目篩而不能通過24目篩的微丸進行包薄膜衣。薄膜包衣的工藝參數為:進風頻率800rpm、出風頻率800rpm、霧化壓力0.2mpa、包衣液流速2rpm和物料溫度45℃。干燥,過16和24目篩,收集通過16目篩而不能通過24目篩的微丸,質檢,包裝,即得成品。
結果:滾圓后微丸的粒徑0.5mm,微丸收率為77.0%,包衣增重3%,包衣效率為95.4%,成品檢驗合格。
實施例5
取黃芪2.5kg、葛根5.0kg、桑白皮2.5kg,加15倍量95%乙醇回流提取5次,每次1小時,濾過,合并濾液,20nm陶瓷膜過濾,收集濾液,回收乙醇并濃縮(溫度:70℃;氣壓:-0.8~-0.6mpa)至相對密度1.25~1.30(70℃),收膏備用。
取以上浸膏,加總重量的25%微晶纖維素和5%滑石粉,混勻,加適量水制軟材,擠出滾圓成微丸。該步驟的工藝參數為:擠出速度50rpm、滾圓時間10min和滾圓速度1500rpm。60±10℃干燥3小時,過18和24目篩,取能通過18目篩而不能通過24目篩的微丸進行包薄膜衣。薄膜包衣的工藝參數:進風頻率2000rpm、出風頻率2000rpm、霧化壓力0.5mpa、包衣液流速8rpm和物料溫度65℃。干燥,過16和24目篩,收集通過16目篩而不能通過24目篩的微丸,質檢,包裝,即得成品。
結果:滾圓后微丸的粒徑5mm,微丸收率為90.3%,包衣增重5%,包衣效率為96.1%,成品檢驗合格。
實施例6
取黃芪2.5kg、葛根5.0kg、桑白皮2.5kg,加5倍量60%乙醇回流提取3次,每次2小時,濾過,合并濾液,20nm陶瓷膜過濾,收集濾液,回收乙醇并濃縮(溫度:70℃;氣壓:-0.8~-0.6mpa)至相對密度1.30~1.35(70℃),收膏備用。
取以上浸膏,加60%微晶纖維素和5%滑石粉,混勻,加適量水制軟材,擠出滾圓成微丸,該步驟的工藝參數:擠出速度20rpm、滾圓時間5min和滾圓速度1200rpm。60±10℃干燥2小時,過18和24目篩,取能通過18目篩而不能通過24目篩的微丸,包薄膜衣。薄膜包衣的工藝參數:進風頻率1000rpm、出風頻率1000rpm、霧化壓力0.2mpa、包衣液流速3rpm和物料溫度40℃。干燥,過16和24目篩,收集通過16目篩而不能通過24目篩的微丸,質檢,包裝,即得成品。
結果:滾圓后微丸的粒徑0.5mm,微丸收率為92.1%,包衣增重2%,包衣效率為95.7%,成品檢驗合格。
實施例7
取取黃芪2.5kg、葛根5.0kg、桑白皮2.5kg,加10倍量80%乙醇提取2次,每次3小時,濾過,合并濾液,100nm陶瓷膜過濾,收集濾液,回收乙醇并濃縮(溫度:70℃;氣壓:-0.8~-0.6mpa)至相對密度1.35~1.40(70℃),收膏備用。
取以上浸膏,加總重量的40%微晶纖維素和2%滑石粉,混勻,加適量水制軟材,擠出滾圓成微丸,該步驟工藝參數為:擠出速度40rpm、滾圓時間8min和滾圓速度800rpm。60±10℃干燥4小時,過篩,取合格微丸,包薄膜衣。薄膜包衣的工藝參數:進風頻率2000rpm、出風頻率2000rpm、霧化壓力0.4mpa、包衣液流速6rpm和物料溫度50℃。干燥,過篩,收集合格微丸,質檢,包裝,即得。
結果:滾圓后微丸的粒徑2mm,微丸收率為93.5%,包衣增重5%,包衣效率為96.3%,成品檢驗合格。
上述實施例采用微晶纖維素、滑石粉與中藥組合物的浸膏配合制備治療糖尿病腎病的中藥丸劑。該制備方法采用陶瓷膜超濾技術能夠富集有效成分,所得中藥組合物的浸膏直接與微晶纖維素和滑石粉配合進行擠出滾圓制粒和薄膜包衣,載藥量高,產品收率高且包衣效率高。同時,采用該制備方法制備的中藥丸劑,便于服用,依從性好,生物利用度高,對微丸進行薄膜包衣能夠避光、防潮和抗氧化,提高藥物的穩定性。
優選地,當采用當微晶纖維素的用量為40-60%且滑石粉的用量在2-5%時,微丸的收率在92.1-97.5%,粒徑在0.5-2mm之間,質量均一、穩定且可控。尤其,當采用加8倍量70%乙醇回流提取兩次,每次3小時,濾過,合并濾液,50nm陶瓷膜過濾,收集濾液,回收乙醇并濃縮(溫度:70℃;氣壓:-0.8~-0.6mpa)至相對密度1.32~1.35(70℃),得浸膏。再向所得浸膏中加入占總量40%的微晶纖維素和5%的滑石粉,滾圓制得后微丸的粒徑1mm,微丸的收率最高為97.5%,包衣效率為97.6%。
(二)效應實驗
實施例8
氧化應激、細胞凋亡和細胞膜電荷屏障破壞是糖尿病腎病的重要表現。細胞膜電荷屏障破壞在糖尿病腎病中主要體現在負電荷減少。本實施例通過晚期糖基化終末產物(ages)對氧化應激、細胞凋亡、細胞膜電荷屏障的影響。
1實驗材料
1.1儀器
ix71、ix81顯微鏡,日本奧林巴斯公司;
ldz4-1.2低速離心機,北京京立離心機有限公司;
sartoriusbs224s/cb-25a電子分析天平,北京賽多利斯儀器系統有限公司;
cp-st100aco2培養箱,長沙長錦科技有限公司;
24孔細胞培養板,美國corning公司。
1.2試劑及藥品
低糖dmem培養基,gibco公司;
胎牛血清,浙江天杭生物科技有限公司;
吖啶橙(ao),廣州杰特偉生物科技有限公司;
溴化乙錠(eb)、二甲基亞砜(dmso)、蘇木素、牛血清白蛋白(bsa)、d-葡萄糖,sigma公司;
阿爾新藍(alcainblue,ab),biosharp公司;
超氧化物陰離子熒光探針(dihydroethidium),碧云天生物技術研究所;
維生素e(vite),alfaaesar公司;
青霉素鈉,華北制藥公司;
硫酸鏈霉素,大連美羅大藥廠。
其余試劑均為市售國產分析純。
組合物浸膏,由實施例1制備獲得。
1.3細胞株
人臍靜脈內皮細胞株huvec,來源于美國模式培養物集存庫(atcc)。
2實驗方法
2.1試劑配制
晚期糖基化終末產物(ages)制備:5gbsa、9gd-葡萄糖溶于100mlpbs中,過濾除菌后分裝,置37℃co2培養箱中培養90d,經廣泛透析除去未反應的蛋白和葡萄糖,即得。
dihydroethidium配制:取dihydroethidium適量,dmso溶解成10mm的母液,分裝,-20℃避光冷藏備用。使用前,以pbs稀釋成5μm的工作液后使用。
ao-eb染液配制:取ao、eb各1mg,分別溶于5mlpbs中,得200μg/ml的儲備液,4℃冷藏備用。使用前等體積混合即可。
ab染液配制:取阿爾新藍0.05g,溶于100ml3%醋酸中,即得0.5g/l的ab染液。
harris蘇木素染液配制:取5.0g蘇木素放入50ml無水乙醇中,攪拌至完全溶解。將44g硫酸鋁鉀加入1000ml蒸餾水內,加熱溶解,然后加入蘇木素無水乙醇液,使溶液盡快沸騰后,離開火焰。攪拌溶液,待溫度下降至91℃時,將5g氧化汞緩緩加入。繼續攪拌至看不到氧化汞的黃色為止,迅速置于冷水中,用紗布置于瓶口處蓋之。次日,過濾,加入4g檸檬酸攪勻,即得。
vite配制:取vite91.0μl,加入無水乙醇410μl,配成400mm的母液,4℃冷藏備用,使用時以pbs稀釋成所需濃度。
受試藥配制:取組合物浸膏,以水稀釋至濃度100g/l,再以水10倍稀釋為10g/l至10-2g/l,4℃冷藏備用。
2.2分組
實驗分為空白對照組、模型組(ages,終濃度為100μg/l)、陽性藥組(vite,終濃度為200μmol/l)、組合物各濃度組(終濃度分別為10、1、0.1、0.01、1x10-3g/l)。
2.3細胞培養及給藥
huvec細胞,以含5%fbs的低糖dmem常規培養。取對數生長期細胞制成單細胞懸液,以1ml/孔接種于放有用多聚賴氨酸預處理過的蓋玻片的24孔板中,細胞數1×105/孔,37℃5%co2培養24h后,同步化細胞。
棄去細胞上清液,分別加入含5%fbs的低糖dmem和各藥物(或pbs),使總體積為1.5ml。正常對照組加入pbs,模型組加入pbs和ages,陽性組加入vite和ages,各供試藥組分別加入所配各濃度藥物和ages。
2.4細胞氧化應激檢測
細胞培養48h后,棄去培養基,pbs清洗2次,每孔加入dihydroethidium工作液50μl,37℃避光反應30min。取出細胞爬片,pbs洗凈,濾紙吸干,細胞面朝下置于載玻片上,以顯微鏡wib熒光通道觀察,并攝片。所得圖片采用ipp圖像分析軟件,統計其陽性染色積分光密度(即積分光密度5000以上部分)、細胞著色總面積(即積分光密度100以上部分總面積),按公式陽性染色百分率=陽性染色積分光密度/細胞著色總面積x100%計算其陽性染色百分率。以上實驗均重復3次。
2.5細胞凋亡檢測
細胞培養48h后,取出細胞爬片,pbs洗凈,濾紙吸干備用。取ao-eb染液5μl滴加于載玻片,將細胞爬片細胞面朝下覆于ao-eb染液上,30秒后以顯微鏡wib熒光通道觀察,并攝片。所得圖片采用ipp圖像分析軟件,統計其紅色和橙色部分積分光密度、細胞著色總面積(即紅色+橙色+綠色部分總面積),按公式凋亡百分率=紅色和橙色部分積分光密度/細胞著色總面積x100%計算其凋亡百分率。以上實驗均重復3次。
2.6細胞膜負電荷檢測
細胞培養48h后,取出細胞爬片,pbs洗凈,濾紙吸干,10%甲醛固定20min;ab染液染色5min,自來水沖洗5min;蘇木素復染10s,自來水沖洗5min;濃度依次為76%、90%、96%、100%乙醇分別脫水二次,每次10min;二甲苯透明,中性樹膠封片,鏡檢并攝片。所得圖片采用ipp圖像分析軟件,統計其陽性染色面積(即細胞膜淡藍色部分著色面積)、細胞總面積,按公式陽性染色百分率=陽性染色面積/細胞總面積×100%計算其陽性染色百分率。以上實驗均重復3次。
3數據處理
采用excel進行數據匯總,以均值±方差表示。數據采用學生t檢驗,p<0.05表示有統計學意義。
4實驗結果
4.1對細胞氧化應激的影響
由表1和圖1可知,與正常組相比,模型組細胞的陽性染色百分率明顯增加(p<0.01)。與模型組相比,陽性藥組和質量濃度為1至1x10-3g/l之間的組合物能明顯降低ages所致細胞的陽性染色百分率增加(p<0.05,0.01),表明該組合物在該濃度范圍內能夠防止細胞氧化應激反應的過度發生,具有明顯的抗氧化作用。當組合物的質量濃度為10g/l時,則不能降低ages所致細胞的陽性染色百分率增加的情況。
表1組合物對ages誘導huvec細胞的抗氧化作用
vscontrol,##p<0.01;vsmodel,*p<0.05,**p<0.01
4.2對細胞凋亡的影響
由表2和圖2可知,與正常組相比,模型組的細胞凋亡百分率明顯升高,且與正常組的細胞凋亡百分率具有顯著性差異(p<0.05)。與模型組相比,陽性藥組和質量濃度為0.1g/l的組合物所在組的細胞凋亡率明顯降低,具有顯著性差異(p<0.05),屬于最優劑量。當組化物的質量濃度在10至0.01g/l之間,同樣能夠明顯降低細胞凋亡的百分率。但是當組合物的質量濃度很低時,如1×10-3g/l時,則不能有效抑制模型組細胞的凋亡。
表2組合物對ages誘導huvec細胞凋亡的影響
vscontrol,#p<0.05;vsmodel,*p<0.05
4.3對細胞膜負電荷的影響
由表3和圖3可知,與正常組相比,模型組細胞的huvec細胞膜與阿爾新藍結合量顯著減少(p<0.01)。與模型組相比,陽性藥組與阿爾新藍結合量明顯增加,具有統計學意義(p<0.05);質量濃度為0.1g/l的組合物能夠有效抵抗細胞膜負電荷的減少(p<0.01),大于或小于該質量濃度的組合物能夠在一定程度上抗細胞膜負電荷減少,表明該組化物具有保護腎臟的電荷屏障的作用。
表3組合物對ages誘導huvec細胞膜負電荷減少的影響
vscontrol,##p<0.01;vsmodel,*p<0.05,**p<0.01
5實驗結論
由表1至表3及圖1至圖3可知,在由ages誘導的糖尿病腎病的細胞模型試驗中,該組合物浸膏在一定的質量濃度范圍內具有顯著的抗細胞氧化、抗細胞凋亡和抗細胞膜負電荷減少作用,且量效關系明顯,表明該組合物浸膏具有保護腎臟細胞的結構屏障和電荷屏障,起到保護腎臟的作用。
實施例9
本實施例探索了中藥丸劑在治療stz-cfa聯合誘導的糖尿病腎病模型大鼠的效果。
1實驗材料
1.1動物
spf級雄性wistar大鼠140只,體重180-220g,南方醫科大學實驗動物中心,合格證號:scxk(粵)2011-0015。
1.2藥品
受試藥:組合物微丸,由廣州康臣藥物研究有限公司制劑室提供,批號:20131012;
陽性藥:厄倍沙坦膠囊,由浙江弘盛藥業有限公司提供,批號:671321;
streptozotocin,sigma公司,批號slbb7526v;
completefreund'sadjuvant,chondrex公司,批號120383;
葡萄糖檢測試劑盒,德國羅氏診斷公司產品,批號:673318;
尿液總蛋白檢測試劑盒,德國羅氏診斷公司產品,批號:675595;
肌酐檢測試劑盒,德國羅氏診斷公司產品,批號:673318,688815;
尿素/尿素氮檢測試劑盒,德國羅氏診斷公司產品,批號:686545;
膽固醇檢測試劑盒,德國羅氏診斷公司產品,批號:682310;
低密度脂蛋白膽固醇檢測試劑盒,德國羅氏診斷公司產品,批號:674550;
大鼠微白蛋白elisa檢測試劑盒,武漢華美生物工程有限公司產品,批號:u05018355;
大鼠sodelisa檢測試劑盒,武漢華美生物工程有限公司產品,批號:v25017660;
大鼠mdaelisa檢測試劑盒,武漢華美生物工程有限公司產品,批號:w09017654;
大鼠ageselisa檢測試劑盒,武漢華美生物工程有限公司產品,批號:v25017656;
大鼠il-6elisa檢測試劑盒,武漢華美生物工程有限公司產品,批號:v18017652;
大鼠tnf-αelisa檢測試劑盒,武漢華美生物工程有限公司產品,批號:t30017658;
微白蛋白測定試劑盒,浙江寧波賽克生物技術有限公司,批號20130508,20140314;
肌酐測定試劑盒,南京建成科技有限公司,批號20131101;
尿素氮測定試劑盒,南京建成科技有限公司,批號20131025;
總蛋白測定試劑盒,上海碧云天生物技術有限公司,批號20130521;
sod試劑盒,南京建成生物工程研究所產品,批號:20140107;
mda測定試劑盒,南京建成生物工程研究所產品,批號:20140106;
枸櫞酸,枸櫞酸鈉等常用試劑均為國產分析純。
1.3主要儀器
羅氏血糖儀及試紙,羅氏診斷中國公司;
spectramax190,美國moleculardevices公司;
coda無創血壓儀,美國kent公司;
bs224s型電子天平,德國sartorius公司;
羅氏p800生化儀,德國羅氏診斷公司產品;
sunrise全自動酶標儀,瑞士tecan公司產品。
2實驗方法
2.1試劑及藥物配制
0.1mol/l枸櫞酸-枸櫞酸鈉緩沖液:精密稱取1.1976g枸櫞酸,1.2646g枸櫞酸鈉,以滅菌注射用水配成100ml溶液,備用。
stz配制:取1gstreptozotocin,以0.1mol/l枸櫞酸-枸櫞酸鈉緩沖液配制成44mg/ml溶液,0.22μm濾膜過濾除菌,現配現用。
丸劑配制:取中藥丸劑適量,以超純水配至濃度為2.4、1.2g/ml,分別為高、低劑量,4℃冷藏備用。
厄貝沙坦配制:取浙江弘盛藥業有限公司所產膠囊劑,取出內容物,以超純水配至濃度為6mg/ml,常溫儲存,每2天配制一次。
2.2造模方法
動物自由飲水、進食。大鼠90只,隨機分為兩組,正常對照組10只,造模組80只。造模組按30mg/kg腹腔注射stz,第二天腹腔注射cfa,0.1ml/只,每周一次;對照組注射相應體積的檸檬酸緩沖液。連續3周重復上述步驟,注射部位用酒精棉球消毒。造模組飼以高脂飼料,正常組常規飼養。動物飼養環境保持明:暗時間為12:12小時。
2.3血糖測定
大鼠尾尖用羅氏血糖儀配套采血針取血,直接測定血糖值,采血部位用酒精棉球消毒。動物給予造模藥物前,自由飲水進食條件下,測定正常血糖一次,給予造模藥物三周內,每周測定血糖一次。
2.4動物分組與給藥
造模動物第3周結束后測定血糖,以血糖值在16~30mmol/l者為合格動物,合格動物按照血糖分組,每組15只,每組動物的血糖值在組間無顯著差異。分組情況為:模型組,丸劑高(劑量為5.4g/kg)、低劑量組(劑量為2.7g/kg),厄倍沙坦組(劑量為13.5mg/kg)。正常對照組大鼠10只,保持不變。
給藥組分別給予相應藥物,體積為0.5ml/220g,均采用灌胃給藥的方法;正常對照組、模型組給予同體積生理鹽水。每周給藥6天,連續11周。
2.5動物日常管理及觀察
造模及給藥期間,每日每只大鼠給食30g和新鮮涼開水,正常組給予普通飼料,其余各組給予高脂飼料;每日更換墊料。每日觀察動物狀態。
2.6指標檢測
給藥期間每周稱1次體重,每2周測1次尿量。給藥第5周,收集24小時尿液,檢測尿液中總蛋白、微白蛋白、肌酐含量。
給藥結束后,收集24小時尿液,測定尿液中總蛋白、微白蛋白、肌酐含量。采集動物血清,測定血糖、總膽固醇(chol)、丙二醛(mda)、血肌酐、血尿素氮、晚期糖基化終產物(ages)、低密度脂蛋白(ldl)、超氧化物歧化酶(sod)、腫瘤壞死因子(tnf-alpha)、白介素6(il-6)含量,并計算肌酐清除率。取一側腎臟福爾馬林保存備用,切片,he、pas染色觀察腎臟病理變化,并對he染色進行病理評分,對pas染色作圖像分析,計算陽性百分率。
he染色病理評分標準:
1)腎小球:①系膜細胞增殖:無,輕,中,重分別記0,1,2,3分;②基質增寬:正常0,輕度變化,毛細血管袢無明顯影響1,中度變化呈彌漫性增寬,50%以下毛細血管袢狹窄閉鎖2,重度變化呈彌漫性增寬,50%以上毛細血管袢狹窄閉鎖3;③硬化改變:正常0,局灶節段分布,硬化腎小球<30%1,30-60%2,>60%3;④腎小球囊。2)腎小管:①變性,壞死,萎縮,無0,小灶性1,片灶裝2,彌漫性3;②間質炎細胞浸潤,無0,小灶性1,片灶裝2,彌漫性3;③間質纖維化,無0,小灶性1,片灶裝2,彌漫性3。小球,小管分別按總體評分0級,0分;1級1-4分;2級5-8分;3級9-12分。
3數據處理
各組數據采用均數±標準差
4實驗結果
4.1對體重的影響
由表4可看出,與正常組相比,模型組中的大鼠體重明顯降低(p<0.01)。與模型組相比,陽性藥物組及中藥丸劑高、低量組中的大鼠的體重緩慢上升,但仍然低于正常組大鼠的平均體重,減輕,表明該中藥丸劑的活性成分能夠緩解模型動物的體重減輕的癥狀。
表4對stz-cfa聯合誘導的糖尿病腎病模型大鼠體重的影響
vs正常:##p<0.01
4.2對24小時尿量、尿微白蛋白等尿生化指標、血肌酐等血清生化指標及肌酐清除率的影響
由表5可看出,與正常組相比,模型組24h尿量明顯升高(p<0.01)。與模型組相比,丸劑低劑量組在不同時期能夠改善尿量。
表5對stz-cfa聯合誘導的糖尿病腎病模型大鼠24h尿量的影響
vs正常:#p<0.05,##p<0.01;vs模型:*p<0.05,**p<0.01
由表6可知,與正常組相比,模型組大鼠的24尿液中尿微白蛋白的量顯著升高。與模型組相比,丸劑的高低劑量組均可以減少尿液中尿微白蛋白的量。
表6對stz-cfa聯合誘導的糖尿病腎病模型大鼠24h尿微白蛋白的影響
vs正常:#p<0.05,##p<0.01;vs模型:*p<0.05,**p<0.01
由表7可看出,與正常組相比,模型組中的大鼠的尿液中的尿總蛋白、尿肌苷和尿尿素氮顯著增加,肌酐清除率明顯增大。與模型組相比,厄爾沙坦組和高低劑量丸劑組均能有效降低模型組中的大鼠的尿液中的尿總蛋白、尿肌苷和尿尿素氮的含量,降低肌酐清除率。
表7stz-cfa聯合誘導的糖尿病腎病模型大鼠尿總蛋白、尿素、尿肌酐及肌酐清除率的影響
vs正常:#p<0.05,##p<0.01;vs模型:*p<0.05,**p<0.01;
由表8可看出,與正常組相比,模型組中相關指標均有顯著性變化。與模型組相比,厄貝沙坦對mda、ldl、ages、il-6、tnf-α也具有明顯改善或抑制相關指標的變化的作用(p<0.05,p<0.01);丸劑高低劑量組可明顯改善或抑制相關指標的變化(p<0.05,p<0.01)。
表8stz-cfa聯合誘導的糖尿病腎病模型大鼠sod、mda、chol、ldl、ages、il-6和tnf-α的變化
vs正常:#p<0.05,##p<0.01;vs模型:*p<0.05,**p<0.01
4.3對腎臟病理學的影響
由表9可以看出,與正常對照組相比,模型組的he染色病理評分和pas染色陽性百分率均明顯升高(p<0.01)。與模型組相比,丸劑高低劑量組和厄爾沙坦組均可降低he染色病理評分數值和pas陽性百分率(p<0.01)。另外,由圖4可以看出,模型組的腎小球和腎小管多處病變,給予藥物后,病變程度有所減輕。由圖5可以看出,模型組陽性染色明顯增加,各給藥組與模型組是陽性染色百分率具有顯著差異。
表9對stz-cfa聯合誘導的糖尿病腎病模型大鼠腎臟病理學的影響
vs正常:##p<0.01;vs模型:**p<0.01
5、結論
該中藥丸劑對stz-cfa聯合誘導的糖尿病腎病模型動物的多個指標具有顯著療效或改善作用,這也符合治療糖尿病腎病中藥復方往往多途徑、多環節起效的作用。丸劑高低劑量組均可明顯降低模型動物的尿總蛋白、尿微白蛋白、尿肌苷、尿尿素氮水平和肌酐清除率;明顯降低模型動物血清中mda、chol、ldl、ages、il-6、tnf-α水平,升高血清中sod、血肌酐水平,降低腎臟he染色病理評分,明顯改善pas染色陽性百分率,具有保護腎臟的作用。
綜上所述,本發明提供了一種治療糖尿病腎病的中藥丸劑,其由活性成分、稀釋劑、抗黏劑以及潤濕劑制備而成,所述活性成分為黃芪、葛根和桑白皮制備的中藥組合物,選用微晶纖維素作為稀釋劑,選用滑石粉作為抗黏劑,載藥量高,產品收率高,包衣效率高。通過細胞試驗研究發現:在由ages即糖基化終產物制備的糖尿病腎病模型的細胞試驗中,該活性成分具有明顯的抗細胞氧化、抗細胞凋亡和抗細胞膜負電荷減少的作用,且量效關系顯著,能夠有效保護腎臟細胞的結構屏障和電荷屏障。在stz-cfa加高脂質聯合誘導的糖尿病腎病的動物模型試驗中,該中藥丸劑能夠明顯降低模型動物的尿總蛋白、尿微白蛋白、尿肌苷、尿素氮水平和肌酐清除率,能夠明顯降低模型動物血清中的mda、chol、ldl、ages、il-6、tnf-α水平,升高血清中sod、血肌酐水平,能夠降低糖尿病腎病的動物模型中腎臟he染色病理評分,明顯改善pas染色陽性百分率,具有明顯的保護腎臟的作用。
本發明提供的中藥丸劑的制備方法采用超濾技術能夠富集有效成分,所得中藥組合物的浸膏直接與微晶纖維素和滑石粉配合進行擠出滾圓制粒并包薄膜衣,載藥量高,產品收率高,包衣效率高。該制備方法具有操作簡單,工藝穩定和重現性好的優點。尤其當使用60-80%的乙醇提取2-3次,通過20-100nm陶瓷膜過濾獲得的活性成分,并配合用量為40-60%的微晶纖維素的和用量為2-5%的滑石粉制備的中藥微丸,微丸的收率在92.1-97.5%,粒徑在0.5-2mm之間,質量均一、穩定且可控。
以上所述實施例的各技術特征可以進行任意的組合,為使描述簡潔,未對上述實施例中的各個技術特征所有可能的組合都進行描述,然而,只要這些技術特征的組合不存在矛盾,都應當認為是本說明書記載的范圍。
以上所述實施例僅表達了本發明的幾種實施方式,其描述較為具體和詳細,但并不能因此而理解為對發明專利范圍的限制。應當指出的是,對于本領域的普通技術人員來說,在不脫離本發明構思的前提下,還可以做出若干變形和改進,這些都屬于本發明的保護范圍。因此,本發明專利的保護范圍應以所附權利要求為準。
- 還沒有人留言評論。精彩留言會獲得點贊!