Box?Behnken效應面法優化制備氯諾昔康柔性脂質體的制作方法
本發明屬于藥物領域,特別提供一種采用Box-Behnken效應面法優化制備氯諾昔康柔性脂質體的方法。
背景技術:
氯諾昔康(Lornoxicam),是一種具有抗炎、鎮痛和退熱作用的非甾體類抗炎藥,能高度選擇性抑制環加氧酶抑制劑(COX-II)。臨床上主要用于慢性關節炎癥、手術和急性創傷后的疼痛、上呼吸道感染引起的發熱等。目前,氯諾昔康在臨床上有片劑、顆粒劑及干混懸劑等劑型,但由于其溶解度很小,生物利用度低,且波動性較大,局部濃度低,需頻繁給藥,有一定的胃腸道不良反應,且肝臟毒性較大。
脂質體作為外用藥物載體具有靶向性、高效、長效、降低藥物不良反應等優勢。由于脂質體可以使藥物具有較大的角質層透過量,而進入血液循環的藥量較少,從而表現出相對的皮膚組織靶向性。柔性納米脂質體(ultra flexible nano-niosomes,UNN)是將膽酸鈉、吐溫、司盤等表面活性劑加入到制備脂質體的類脂材料中制成,可高效地穿過比其自身小數倍的脂質載體,柔性脂質體具有高效滲透性、親水性和高度柔韌性。氯諾昔康作為有效成分制備柔性納米脂質囊泡,不僅能減少氯諾昔康對胃腸道及肝臟的不良反應,也避免了藥物的首過效應,延長了鎮痛時間。
Box-Behnken效應面法設計實驗是適用于多因素考察的新型科學設計方法。其優勢在于運用非線性擬合模型從而提高準確度,近年來多被研究者用來進行處方及工藝優化。
技術實現要素:
本發明的目的在于提供一種采用Box-Behnken效應面法篩選制備氯諾昔康柔性脂質體最佳處方的方法,效應面法具有試驗設計全面、科學準確、可以研究多個因素交互作用等優點,針對制備柔性脂質體過程中影響較大的磷脂濃度,磷脂與膽固醇質量比,總脂質與吐溫80質量比,總脂質與藥物質量比四個因素分別進行考察,以包封率和粒徑作為優化指標進行Box-Behnken效應面實驗設計,優化氯諾昔康柔性脂質體的最佳處方。
本發明具體方案如下:
一種采用Box-Behnken效應面法優化制備氯諾昔康柔性脂質體的方法,其特征在于:采用薄膜分散水化法制備脂質體,分別以磷脂濃度、磷脂與膽固醇質量比、總脂質與吐溫80質量比、總脂質與藥物質量比為考察對象,以包封率、粒徑為評價指標,采用4因素3水平Box-Behnken效應面設計法篩選氯諾昔康柔性脂質體的最佳處方。
本發明所述采用Box-Behnken效應面法優化制備氯諾昔康柔性脂質體的方法,其特征在于:采用葡聚糖G50微柱離心法測定包封率,動態激光散射法測定脂質體的粒徑和ζ-電位。
采用本發明所述方法優化而成的制備氯諾昔康柔性脂質體的方法,其特征在于:將氯諾昔康與大豆卵磷脂、膽固醇、吐溫80混合,加入溶劑溶解,然后減壓除去溶劑,得到淡黃色透明均勻薄膜;加入重蒸水水化,50-60℃條件下水化15-25min后,探頭超聲3-5min,然后過0.22μm濾膜,得淡黃色氯諾昔康柔性脂質體混懸液。由體外釋放考察中可知,相比于原料藥溶液組,優化后制得的氯諾昔康柔性脂質體包封率較高,大小分布均勻,具有緩釋特點。
其中,最優處方工藝條件為:大豆卵磷脂濃度為16.94mg/mL,大豆卵磷脂與膽固醇質量比為4.46:1,總脂質與吐溫80質量比為8.12:1,總脂質與藥物質量比為18.65:1。以最優處方制備的氯諾昔康柔性脂質體平均粒徑較小(93.86±7.58)nm、ζ-電位較好(-20.21±2.31mV)、包封率較高(90.23±1.46)%,實際值與預測值偏差較小。82.06%的藥物在24h內從脂質體中釋放出來,具備明顯的緩釋特性。
本發明所述制備氯諾昔康柔性脂質體的方法,其特征在于:所述溶劑為無水氯仿;水化條件優選為:55℃條件下水化20min。
本發明通過Box-Behnken效應面法得到優化的氯諾昔康柔性脂質體制備工藝,按該處方制備3批脂質體,同時對其包封率和粒徑進行測定。從測定結果看,實際值與預測值相差較小,證明該方法預測性能良好,是脂質體處方工藝優化的有效方法。優化后制得的氯諾昔康柔性脂質體包封率較高,大小分布均勻,具有緩釋特點,這為后期將其制成親水凝膠提供了較好的實驗基礎。
附圖說明
圖1氯諾昔康柔性脂質體洗脫曲線。
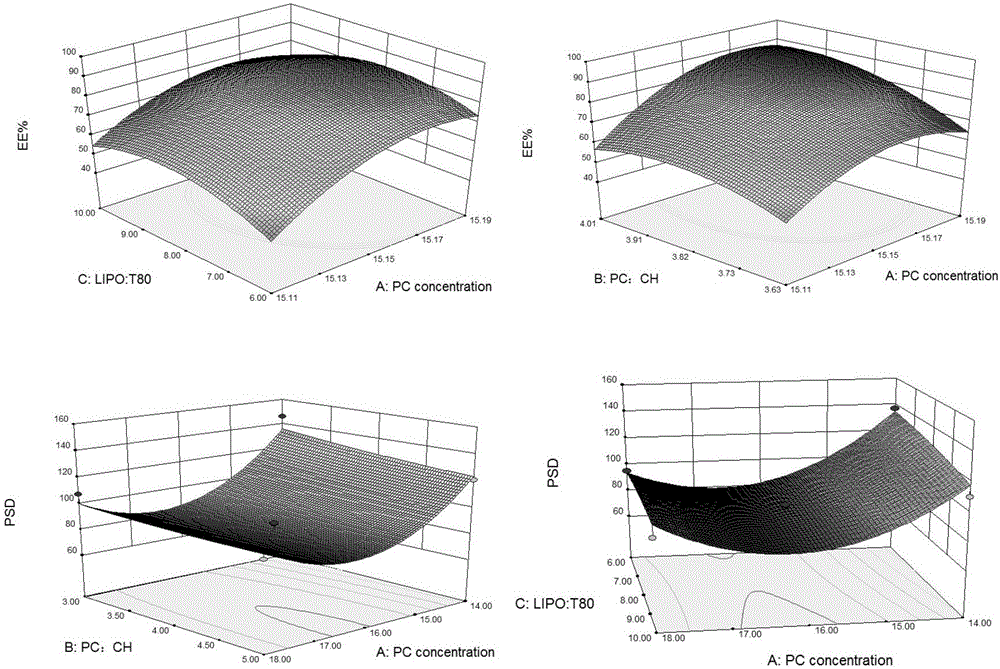
圖2因素交互作用對包封率和粒徑的曲面效應圖。
圖3氯諾昔康柔性脂質體的粒徑分布(a)。
圖4氯諾昔康柔性脂質體的ζ-電位(b)。
圖5氯諾昔康柔性脂質體的透射電鏡照片。
圖6氯諾昔康溶液和氯諾昔康柔性脂質體體外釋放。
具體實施方式
1儀器與材料
JY9222D超聲波細胞粉碎機(寧波新芝科器研究所),SHZ-D(Ⅲ)循環水式真空泵(鞏義市英峪華儀器廠),旋轉蒸發儀(上海亞榮生化儀器廠),DL-180型超聲波清洗機(浙江省象山縣石浦海天電子儀器廠),TGL-16C臺式離心機(上海安亭科學儀器廠),UV-9100紫外可見分光光度計(北京瑞利分析儀器公司),JEM-1200EX透射電子顯微鏡(日本Electron株式會社),FA1104電子天平(上海民橋精密科學儀器有限公司),Spectrum-754PC型紫外掃描儀(上海光譜儀器有限公司),DF-101S集熱式恒溫加熱磁力攪拌器(鞏義市英峪華儀器廠),ZetasizerNano ZS-90激光粒徑測定儀(英國Malvern Instru-ments公司)。
氯諾昔康(東京化成工業株式會社),大豆卵磷脂(PC>96%,上海艾偉特醫藥科技有限公司),膽固醇(生化純,天津市博迪化工股份有限公司),葡聚糖G50(如吉生物科技有限公司),其他試劑均為分析純。
2方法與結果
2.1氯諾昔康柔性脂質體的制備
稱取大豆卵磷脂64mg、膽固醇16mg、吐溫80 10mg、氯諾昔康4mg于250mL茄型瓶中,加入10mL無水氯仿溶解后在50℃減壓除去無水氯仿,得到淡黃色透明均勻薄膜,加入重蒸水4mL水化,55℃條件下水化20min后,探頭超聲(200W)3min后,過0.22μm濾膜2次,得淡黃色氯諾昔康柔性脂質體混懸液,同法制備空白脂質體。
2.2含量測定方法學的建立
2.2.1檢測波長的選擇
取制備的空白脂質體適量,分別對氯諾昔康和空白脂質體進行紫外全波長掃描。氯諾昔康在378nm處有最大吸收,且空白脂質體不干擾測定,因此選擇氯諾昔康檢測波長為378nm。
2.2.2標準曲線的制備
精密稱取氯諾昔康對照品5mg于50mL棕色容量瓶中,以甲醇配成質量濃度為100μg·mL-1的儲備液,分別精密量取0.1、0.2、0.5、1.0、1.5、2.0mL儲備液于10mL棕色量瓶中,用甲醇定容后得到濃度分別為1、2、5、10、15、20μg·mL-1的氯諾昔康溶液并于378nm測定其吸光度(A)。以吸光度(A)對藥物質量濃度(C)進行線性回歸,得標準曲線方程為:C=44.455A-3.2031(R2=0.9999)。結果表明,氯諾昔康質量濃度在1~20μg·mL-1內與吸光度呈良好線性關系。
2.3氯諾昔康柔性脂質體包封率的測定
2.3.1柱分離度的考察
a微型柱的制備
取四只2.5mL注射針筒,底部放一層脫脂棉,加入3.0g經PBS溶液浸泡飽和過,并用蒸餾水洗至中性的葡聚糖凝膠(Sephadex G50),將裝好的微柱放入套管中4000r·min-1離心5min,除去微柱中殘留的水,備用。
b洗脫曲線的考察
精密吸取氯諾昔康柔性脂質體0.2mL,緩緩加入柱頂中心處,4000r·min-1離心5min后在柱頂部加入0.2mL蒸餾水,4000r·min-1離心5min,收集濾過液,再于柱頂部加入同體積的蒸餾水,重復以上操作。收集1~8管濾液分別置于5mL容量瓶中,甲醇定容,采用紫外-可見分光光度計,以甲醇為對照,于378nm處測定吸光度值,制備洗脫曲線(圖1)。
由圖1可知,洗脫曲線呈單峰。用雙蒸水洗脫一次后即可把脂質體全部洗脫下來。最終確定洗脫條件為脂質體混懸液上樣離心后再用同體積雙蒸水洗脫一次。
2.3.2空白脂質體回收實驗
精密量取0.2mL空白脂質體上樣,收集濾過液,用同體積雙蒸水洗脫一次,合并濾過液并置于5mL容量瓶中,雙蒸水定容至刻度,搖勻,于500nm處測定吸光度值定為Aa;精密量取空白脂質體0.2mL于5mL容量瓶中,雙蒸水定容至刻度,搖勻,于500nm處測定吸光度值定為Ab,計算回收率(R),R(%)=(Aa/Ab)×100%,結果見表1。
表1脂質體回收率實驗(n=3)
2.3.3脂質體包封率的測定
分別精密量取氯諾昔康柔性脂質體0.2mL 2份。1份加于G50柱頂,離心后以重蒸水進行洗脫,合并洗脫液并置于10mL容量瓶中,用甲醇定容并超聲破乳后在378nm處測定吸光度為A1;另1份直接加入10mL的容量瓶中,加甲醇定容并超聲破乳于378nm處測定吸光度為A2。包封率(EE/%)計算方法如下:
EE/%=(A1/A2)×100%
2.4Box-Behnken效應面法試驗設計
在預試驗基礎上,根據單因素實驗考察結果,選擇對氯諾昔康柔性脂質體制劑學性質影響較為明顯的4個因素:磷脂濃度(X1)、磷脂與膽固醇質量比(X2)、總脂質與吐溫80質量比(X3)、總脂質與藥物質量比(X4),在低中高3個水平上進行優化,同時以包封率(Y1,EE/%)及粒徑(Y2,d/nm)為評價指標進行實驗考察,影響因素及水平見表2,實驗設計和評價指標結果見表3。
表2 Box-Behnken效應面法中的變量
2.4.1二次回歸模型的建立
利用Box-Behnken實驗軟件對表2實驗數據進行回歸分析,得擬合方程為:
EE/%=-1051.67+104.44X1+2.27X2+43.37X3+7.71X4+2.00X1X2-0.56X1X3-0.26X1X4+2.89X2X3+0.48X2X4-0.25X3X4-3.04X12-7.48X22-2.52X32-0.13X42(R2=0.8604,P<0.0001) (1)
dPD=2004.03-264.79X1-35.54X2-15.20X3+41.55X4+1.40X1X2+1.40X1X3-0.54X1X4+1.48X2X3-0.66X2X4-0.39X3X4+7.86X12+1.41X22-0.42X32-0.72X42(R2=0.8085,P=0.0001) (2)
2.4.2方差顯著性檢驗
兩個擬合方程R2值說明該模型擬合程度較好,可以用此模型對處方工藝進行預測分析。從表4回歸系數顯著性檢驗可知,模型1中,X1(P<0.0001)、X2(P=0.0005)、X12(P<0.0001)、X22(P=0.0038)、X32(P=0.0004)極顯著,X4(P=0.0683)、X2X3(P=0.0540)顯著,其他項不顯著。模型2中,X1(P<0.0001)、X12(P<0.0001)極顯著,其他項不顯著。
表3 Box-Bchnken效應面法優化Lor-FLS處方的組合和相應值
表4回歸方程中系數的顯著性檢驗
2.4.3效應面優化與預測
根據回歸方程,應用Design Expert 8.0.6試驗設計軟件,繪制影響較大的2個因素對于各指標三維曲面圖(圖2)。根據Box-Behnken效應面實驗結果最優處方為X1=16.94,X2=4.46,X3=8.12,X4=18.65。按此最優處方制備3批柔性脂質體,其包封率、粒徑見表5。從表5可知,實測值和模型預測值偏差都較小,說明該模型預測性良好。對于優化處方制備的制劑進行了ζ電位的測定,從圖4可看出,氯諾昔康柔性脂質體的ζ電位為-20.23mV。通常ζ電位在±20mV以上時,由于靜電排斥會阻止微粒間相互碰撞,使制劑不易沉降,從而有利于制劑的穩定。
表5 Lor-FLS的實際值和預測值
2.5氯諾昔康柔性質體的透射電鏡檢查
取適量氯諾昔康柔性脂質體混懸液滴在噴碳銅網上,以2.0%磷鎢酸染色,采用JEM-1200EX透射電子顯微鏡觀察載藥脂質體的形態。從圖5可知,氯諾昔康柔性脂質體大小較均一,表面光滑,近似成球形。
2.6體外釋放度實驗
采用透析法對氯諾昔康柔性脂質體進行體外釋放考察。根據最優處方制備適量脂質體于40C冰箱保存備用。由于氯諾昔康的溶解度在pH 8.0較大,能夠符合漏槽條件,因此選擇PBS(pH 8.0)緩沖液為溶出介質。具體方法如下:取氯諾昔康柔性脂質體混懸液5mL于截留分子量為2000的透析袋中,同時以等量的氯諾昔康PBS(pH 8.0)緩沖液溶液為對照,分別置于含有200mL的PBS(pH 8.0)緩沖液的錐形瓶中,于37℃水浴震蕩,分別于0.25、0.5、0.75、1、2、3、4、6、8、10、12、16、20、24h吸取1mL釋放介質,同時補加1mL PBS緩沖液并按照“2.2.2”方法測定釋放介質中藥物濃度,計算藥物累計釋放百分率。由圖6可知,溶液組在4h內就可完全釋放,而脂質體組在24h內有82.06%藥物從脂質體中釋放出來,存在明顯的緩釋作用。
上述實施例只為說明本發明的技術構思及特點,其目的在于讓熟悉此項技術的人士能夠了解本發明的內容并據以實施,并不能以此限制本發明的保護范圍。凡根據本發明精神實質所作的等效變化或修飾,都應涵蓋在本發明的保護范圍之內。
- 還沒有人留言評論。精彩留言會獲得點贊!