舌下右美托咪定組合物及其使用方法與流程
技術領域:
本申請描述了右美托咪定(右美托咪啶,dexmedetomidine)、其藥用鹽、及其衍生物的鎮痛舌下噴霧制劑(sublingual-sprayformulation),以及它們的使用方法。
背景技術:
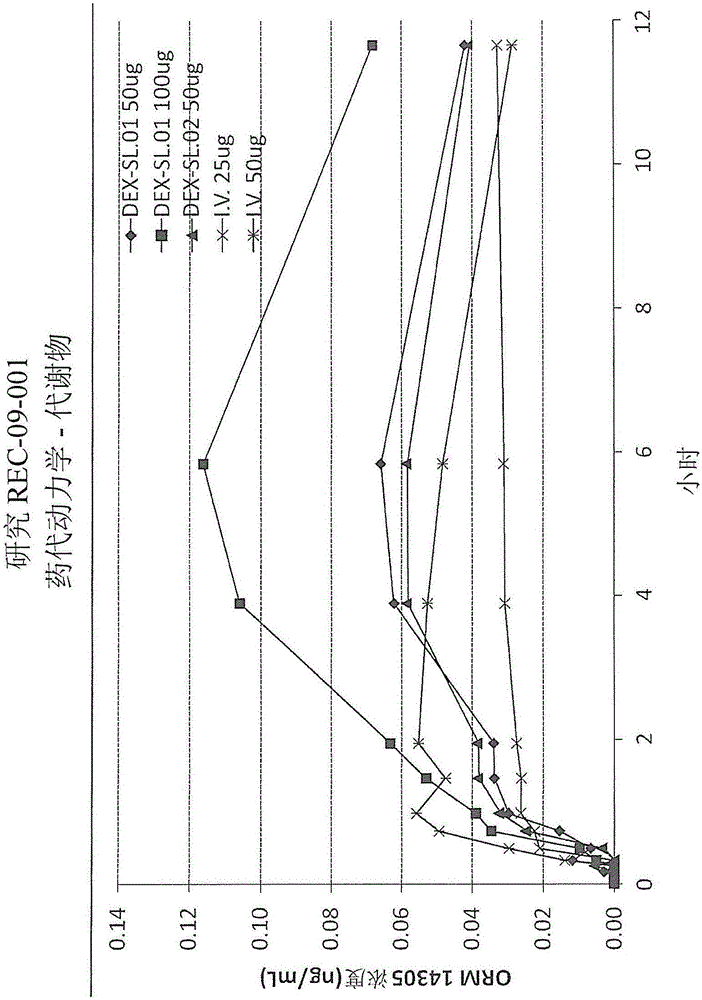
:右美托咪定,5-[(1S)-1-(2,3-二甲基苯基)乙基]-1H-咪唑,是具有鎮靜和鎮痛性質的非麻醉性α2-腎上腺素受體激動劑。目前,右美托咪定僅可作為用于鎮靜的注射制劑商購獲得,并且其必須通過健康護理專業人員經靜脈給藥使用。雖然右美托咪定具有鎮痛性能,但是不能商購獲得可用作鎮痛藥的制劑。此外,由于各種各樣的原因,可商購獲得的注射制劑不適于用作能夠自行給藥的鎮痛藥。對于例如可以自行給藥以產生鎮痛作用(或其他方式治療或預防疼痛)同時沒有顯著鎮靜作用的基于右美托咪定的鎮痛藥存在持續且未得到滿足的需求。技術實現要素:本文提供了右美托咪定和/或其藥用鹽、和/或其衍生物的新的鎮痛舌下噴霧制劑,以及它們在治療和預防疼痛中的使用方法。這樣的藥物組合物包括如足以產生鎮痛作用(例如治療或預防疼痛)的量的右美托咪定或其藥用鹽或衍生物(例如前藥),和藥用液體載體,以及可選的調味劑、增壓推進劑(pressurizedpropellant)、防腐劑、賦形劑、乳化劑、緩沖劑、著色劑等。在一個實例中,提供了一種用于治療或預防疼痛的方法,包括以下步驟:將一種藥物組合物施用于人的口腔粘膜,該藥物組合物包含一個劑量的在藥用液體載體中的右美托咪定或其藥用鹽,其中右美托咪定或其藥用鹽通過所述口腔粘膜吸收并產生鎮痛同時沒有鎮靜作用。在另一個實例中,右美托咪定或其藥用鹽的劑量在約0.05μg/kg和約1.50μg/kg之間。通過另外的實例,利用所述方法,其中的人是成人,且右美托咪定或其藥用鹽的劑量在約5μg和約50μg之間。進一步地,該方法可以提供在右美托咪定經跨粘膜吸收(transmucosalabsorption)到所述人的體循環系統中后的血藥Cmax(血漿Cmax)低于約0.30ng/mL。在另一個實例中,提供了一種用于治療或預防疼痛的方法。在該實例中,其步驟包括將全身性吸收的藥物組合物給藥至哺乳動物的口腔粘膜,該藥物組合物包含在給藥之后有效治療或預防所述哺乳動物的疼痛的量的右美托咪定、或其藥用鹽或前藥,其中該藥物組合物以在給藥1小時內產生鎮痛作用同時沒有鎮靜作用的速率將生理活性量的右美托咪定提供到所述哺乳動物的體循環系統中。在另一個實例中,提供了一種鎮痛藥物組合物,其包含在藥用液體載體中的右美托咪定、或其藥用鹽或前藥(或右美托咪定或其藥用鹽或前藥在該藥用液體載體中),所述藥物組合物配制并適用于通過將所述鎮痛藥物組合物施用于哺乳動物的粘膜而跨粘膜(透過粘膜)給藥至所述哺乳動物。進一步地,該鎮痛藥物組合物可以被配制并適用于通過將所述組合物施用于所述哺乳動物舌下的粘膜而進行舌下給藥。在另一個示例性實施方式中,一種用于將右美托咪定、或其藥用鹽或衍生物給予哺乳動物的方法,包括用經計量的劑量的噴霧組合物噴射哺乳動物的口腔粘膜,該噴霧(劑)組合物包含在藥用液體載體中的右美托咪定、或其藥用鹽或衍生物,其量為通過該哺乳動物的口腔粘膜將藥學有效量的右美托咪定的跨粘膜吸收提供到哺乳動物的體循環系統中。在跨粘膜吸收后,右美托咪定在哺乳動物中產生鎮痛作用。其他特征可以通過參考下面的詳細描述和實施例理解。附圖說明圖1示出了不同劑量的右美托咪定經舌下和靜脈內給藥的藥代動力學數據;圖2示出了不同劑量的右美托咪定代謝物經舌下和靜脈內給藥的藥代動力學數據;圖3示出了不同劑量的右美托咪定經舌下給藥的藥代動力學數據;圖4示出了不同劑量的右美托咪定經舌下和靜脈內給藥的靜息心率數據;圖5示出了不同劑量的右美托咪定經舌下和靜脈內給藥的靜息舒張血壓數據;圖6示出了不同劑量的右美托咪定經舌下和靜脈內給藥的靜息收縮血壓數據;圖7示出了單劑量的右美托咪定經舌下給藥的藥代動力學數據;圖8示出了單劑量的右美托咪定和安慰劑分別經舌下給藥的疼痛強度數據的對比;圖9示出了單劑量的右美托咪定和安慰劑分別經舌下給藥后,反應者的疼痛強度數據的對比;圖10示出了單劑量的右美托咪定和安慰劑分別經舌下給藥后,完全反應者的疼痛強度數據的對比;圖11示出了單劑量的右美托咪定和安慰劑分別經舌下給藥的疼痛緩解數據的對比;圖12示出了單劑量的右美托咪定和安慰劑分別經舌下給藥的靜息心率數據的對比;圖13示出了單劑量的右美托咪定和安慰劑分別經舌下給藥的靜息收縮血壓數據的對比;圖14示出了單劑量的右美托咪定和安慰劑分別經舌下給藥的靜息舒張血壓數據的對比;圖15示出了多劑量的右美托咪定經舌下給藥的藥代動力學數據;圖16示出了多劑量的右美托咪定經舌下給藥的疼痛強度數據;圖17示出了多劑量的右美托咪定經舌下給藥的靜息心率數據;圖18示出了多劑量的右美托咪定經舌下給藥的靜息收縮血壓數據;圖19示出了多劑量的右美托咪定經舌下給藥的靜息舒張血壓數據;圖20示出了右美托咪定經舌下給藥的不良反應數據。具體實施方式本文提供右美托咪定、或其藥用鹽或衍生物的新的鎮痛舌下噴霧制劑,以及它們在預防、治療和管理(調節,management)疼痛中的使用方法。右美托咪定是一種特定α2-腎上腺素受體激動劑,其在哺乳動物中引起鎮靜、麻醉和鎮痛。在人中,右美托咪定是商購獲得的用于在重癥監護情形的治療期間的起初插管和機械通氣患者的鎮靜,以及非插管患者在手術或其他過程之前或期間的鎮靜。參見例如美國專利No.6,716,867和6,313,311。已研究了靜脈內(i.v.)、肌內(i.m.)和經皮給藥后右美托咪定在人體中的藥代動力學。平均消除半衰期(meaneliminationhalf-life)在靜脈內和肌內給藥后分別為1.5h至3h,以及在經皮給藥后為5.6h。在肌內給藥和經皮給藥后,在血液中達到最大濃度的時間分別為1.6-1.7h和6h,并且估計絕對生物利用度分別為73%和88%。參見例如“Pharmacodynamicsandpharmacokineticsofintramusculardexmedetomidine,”Scheininetal.,Clin.Pharmacol.Ther.52,53-46(1992);“Thepharmacokineticsandhemodynamiceffectsofintravenousandintramusculardexmedetomidinehydrochlorideinadulthumanvolunteers,”Dycketal.,Anesthesiology78,813-20(1993);以及“Pharmacokineticsandpharmacodynamicsoftransdermaldexmedetomidine,”etal.,Eur.J.Clin.Pharmacol.46,345-49(1994)。右美托咪定也從口腔吸收。在頰部給藥(其中人受試者在口中保持右美托咪定的溶液而不吞咽)后,測得平均頰部生物利用度為81.8%,其中最大濃度在約1.5h以及明顯消除半衰期為1.9h。參見例如“Bioavailabilityofdexmedetomidineafterextravasculardosesinhealthysubjects,”Anttilaetal.,Br.J.Clin.Pharmacol.56,691-93(2003)。根據本發明,右美托咪定可以給藥至動物或人受試者,用于改善、管理、治愈、預防或其他方式治療疼痛的目的。在一個示例性實施方式中,一種用于將右美托咪定、或其藥用鹽或衍生物給予哺乳動物的方法,包括用經計量的一個劑量的噴霧組合物噴射哺乳動物的口腔,該噴霧組合物包含在藥用液體載體中的右美托咪定、或其藥用鹽或衍生物,其量為通過該哺乳動物的口腔粘膜將藥學有效量的右美托咪定的跨粘膜吸收提供到哺乳動物的體循環系統中。在跨粘膜吸收后,右美托咪定在哺乳動物中產生鎮痛作用。例如,不管是慢性鎮痛療法,患有癌癥和其他疾病的許多患者持續經歷中度到嚴重的疼痛,并且這經常由于患者活動程度增加而作為間歇性爆發性疼痛(breakthroughpain)出現。通過增加鎮痛藥長效制劑的劑量以抵抗這種類型的疼痛的嘗試,經常產生鎮痛起效慢以及不期望的鎮靜、便秘或惡心和嘔吐的副作用,尤其用阿片類鎮痛藥。然而,本文描述的右美托咪定的鎮痛舌下噴霧制劑選擇性地提供了改善、管理、治愈、預防、或其他方式治療這樣的疼痛的中度至快速起作用的、有效的非麻醉性鎮痛藥。本文描述的右美托咪定產品是用于治療疼痛的藥物制劑。如本文中使用的,術語“藥用(或藥學上可接受的)”包括這樣的化合物、材料、組合物、劑型、以及它們的使用方法,其在合理醫學判斷的范圍內,并且適用于與人類和哺乳動物的組織接觸,并且沒有過度的毒性、刺激、過敏反應、或其他問題或并發癥,同時相稱地具有合理的利益/風險比并引發期望的藥理學反應。右美托咪定含有能夠與藥用酸形成藥用鹽的堿性氮原子。在這個方面,術語“藥用鹽”指的是右美托咪定的相對非毒性的無機和有機酸加成鹽。這些鹽可以在右美托咪定的最后分離和純化過程中原位制備,或通過單獨地使游離堿形式的純化的右美托咪定與適當有機酸或無機酸反應,之后分離由此形成的鹽而制得。此外,該鹽可以在生產噴霧制劑的制造過程中形成。代表性的藥用鹽包括氫鹵化物(包括氫溴化物和氫氯化物)、硫酸鹽、硫酸氫鹽、磷酸鹽、硝酸鹽、乙酸鹽、戊酸鹽、油酸鹽、棕櫚酸鹽、硬脂酸鹽、月桂酸鹽、苯甲酸鹽、乳酸鹽、磷酸鹽、甲苯磺酸鹽、檸檬酸鹽、馬來酸鹽、延胡索酸鹽、琥珀酸鹽、酒石酸鹽、萘酸鹽(napthylate)、去鐵胺、葡庚糖酸鹽、乳糖酸鹽、2-羥基乙基磺酸鹽和月桂基磺酸鹽等。參見例如“PharmaceuticalSalts”,Bergeetal.,J.Pharm.Sci.66,1–19(1977)。右美托咪定鹽酸鹽是藥用鹽的一個實例。在本文描述的噴霧制劑中,相對于使用美托咪定本身,優選使用右美托咪定鹽酸鹽,因為在一些情況中,鹽酸鹽具有更高的水溶性和針對環境氧的氧化的穩定性。右美托咪定衍生物可以包括產生前藥的共價改性。在給藥后,前藥衍生物經歷通過哺乳動物產生右美托咪定的化學改性。前藥可用于有利地改變右美托咪定的生物分布(biodistribution)或藥代動力學,或用于產生其他期望的特性。例如,右美托咪定的反應性氮可以與酶促地或非酶促地、還原地、氧化地或水解地分開從而暴露活性藥物成分的官能團衍生化。某些類型的前藥的使用是已知的(參見例如R.B.Silverman,1992,“TheOrganicChemistryofDrugDesignandDrugAction,”AcademicPress,Chp.8)。例如,前藥可在這些化合物的最后分離和純化過程中原位制備,或通過單獨地使游離堿形式的純化的化合物與適當衍生試劑反應而制備。右美托咪定噴霧組合物包括一種或多種藥用液體(以重量計為約30%至約99.995%)。這些液體可以是用于右美托咪定、或其藥用鹽或衍生物的溶劑、共溶劑、或非溶劑。適合的材料是在室溫下為液體,并且在室溫下保持液體狀態,優選在環境壓力以及在提高的壓力下都如此。可用的液體沒有特殊的限制,只要它們不干擾該噴霧組合物的期望醫藥用途,并且它們載送治療有效量的右美托咪定、或其藥用鹽或衍生物(如右美托咪定鹽酸鹽)。藥用液體的實例包括水、乙醇、二甲基亞砜、丙二醇、聚乙二醇、碳酸丙二酯、藥用油類(如大豆油、向日葵油、花生油等)等。選擇藥用液體以溶解活性藥物成分,從而產生其穩定的均質懸液,或者形成懸液或溶液的任何組合。除了前述構成成分,右美托咪定的舌下噴霧制劑可以包括一種或多種不同于該藥學活性藥的賦形劑,其在制造過程中包括或包含在最終藥物產品劑型中。賦形劑的實例包括粘度調節物質(如聚合物類、糖類、糖醇類、樹膠類、粘土類、硅石類等(例如聚乙烯吡咯烷酮(PVP))(以重量計為約0.001%至約65%))。賦形劑的其他實例包括防腐劑(如乙醇、苯甲醇、尼泊金丙酯和尼泊金甲酯)(以重量計為約0.001%至約10%)。賦形劑還可以是調味劑、甜味劑(如糖類(蔗糖、葡萄糖、右旋葡萄糖、麥芽糖、果糖等)、人造甜味劑(糖精、阿斯巴甜糖(aspartame)、乙酰舒泛(acesulfame)、三氯蔗糖(sucralose))、或糖醇類(甘露醇、木糖醇、拉克替醇(lactitol)、麥芽糖醇糖漿))(以重量計為約0.001%至約65%)。賦形劑的其他實例包括緩沖劑和pH-調節劑(如氫氧化鈉、檸檬酸鹽和檸檬酸)(以重量計為約0.01%至約5%)。其他之中,著色劑(以重量計為約0.001%至約5%)、香味劑(以重量計為約0.001%至約1%)、螯合劑(如EDTA)(以重量計為約0.001%至約1%)、UV吸收劑(以重量計為約0.001%至約10%)、和消泡劑(如低分子量醇類、二甲硅油、西甲硅油(simethicone))(以重量計為約0.001%至約5%)也是合適賦形劑另外的實例。舌下右美托咪定制劑(如噴霧劑、滴劑等)可以根據標準的良好制造實踐方法,通過混合恰當量的前述成分而制備。這樣的賦形劑可包含于制劑中以改善患者或受試者接受以及味道、提高生物利用度、增長貨架期、降低制造和包裝成本、符合政府管理機構的要求,以及用于其他目的。每個成分的相對量應不干擾所得制劑的期望藥理學和藥代動力學性質。本文描述的右美托咪定的鎮痛舌下制劑用于直接給藥至粘膜(如哺乳動物的口腔粘膜)。藥物遞送基本經由口腔跨粘膜路徑發生,并且不經由吞咽之后的胃腸道吸收。術語“跨粘膜”指的是跨過或穿過粘膜遞送。尤其,藥物的“口腔跨粘膜”遞送包括跨過口腔、咽、喉、氣管、或上胃腸道的任何組織,尤其是舌下、頰部、齒齦和腭粘膜組織的遞送。術語“舌下”字面意思是“在舌下面”,并且指的是以使物質經由舌下面的血管而不是經由消化道快速吸收的方式經由嘴給予該物質的方法。舌下吸收通過高血管化的舌下粘膜發生,這允許物質直接進入血液循環,由此獨立于胃腸道影響而提供直接的全身給藥,并避免不期望的首先經過肝代謝。與其他的給藥路徑相比,本發明制劑中的右美托咪定的跨粘膜吸收可以具有顯著更快的起效且具有更大的生物利用度。因此,該制劑中的活性藥物成分的總量可以減少,由此降低有害的副作用的可能性,并向制造商提供成本效益。所述制劑可以給予需要其的哺乳動物,包括人、以及人類伙伴動物(如貓、狗)、農業家畜、和其他動物。應理解,將傳統劑型,如片劑、膠囊、糖漿劑等或注射鎮痛制劑給予非人動物經常是成問題的,而本文中描述的舌下噴霧制劑尤其可用于這樣的動物的治療。“鎮痛”是疼痛感覺的緩和或消除。如本文使用的,“疼痛”涵蓋寬范圍的臨床表現,并且具有廣泛的含義。疼痛感是高度主觀的,而且不同的人以不同方式和極大不同的強度經歷疼痛。國際疼痛研究協會(InternationalAssociationfortheStudyofPain)將疼痛定義為“一種與實際或潛在的組織損傷、或依據這樣的損傷描述的不愉快的感覺和情緒經歷”。更簡單地說,疼痛包括引起痛苦并且與自我身體的不愉快意識相關的任何感覺經歷。疼痛的非限制性類型和原因包括神經痛、肌痛、痛覺過敏、痛覺過度、神經炎和神經病。疼痛經常是一種潛在的生理異常的癥狀,如癌癥或關節炎。疼痛的一些類型沒有明確確定的原因,如偏頭痛。疼痛也可以由身體創傷引起,如燒傷或手術。病毒感染,如帶狀皰疹(Herpeszoster)(禽痘和帶狀皰疹),也可以引起疼痛。戒斷對酒精或濫用藥物的化學依賴也經常與疼痛癥狀相關。因此,“疼痛”在本文中應理解成具有非常寬的含義,并且其要求的使用應不被解釋為限于任何特定疾病或障礙。如本文使用的“鎮靜”意思是受壓抑的意識,其中患者或受試者保持獨立地和連續地維持開放的氣道和有規律的呼吸模式的能力,以及適當和理性地對物理刺激和口頭指令有反應的能力。如本文使用的“沒有顯著的鎮靜”意思是患者經歷在拉姆齊鎮靜量表(RamsaySedationScale)上不大于第3級的鎮靜水平,換言之,患者處于這樣的級別:第1級=焦慮、激動、或不安;第2級=合作的、有方向的(oriented)、和安靜的;或第3級=鎮靜但對指令有反應的水平。如本文使用的“顯著鎮靜”意思是患者或受試者在拉姆齊鎮靜量表上經歷第4級或更高的鎮靜,其中第4級=睡著;對輕敲眼瞼或大聲的耳朵刺激有敏捷反應;第5級=睡著;對輕敲眼瞼或大聲的耳朵刺激有遲緩反應;第6級=睡著;對疼痛刺激沒有反應。如本文使用的“顯著鎮靜”在斯坦福瞌睡量表(StanfordSleepinessScale)上也與患者的自我評價一致,其中受試患者將他們鎮靜的程度評定為高于或等于第3級,其中:第1級=感覺活躍、充滿活力的、警覺的、或完全清醒的;第2級=機能在高水平,但不在頂點,能夠集中;第3級=清醒,但放松;有反應但不完全警覺;第4級=有些迷糊,松勁;第5級=迷糊,對保持清醒失去興趣;慢;第6級=瞌睡、昏沉、掙扎睡眠;更喜歡躺下;或第7級=不再掙扎睡眠,馬上入睡;具有像做夢的思維。本文描述的右美托咪定舌下制劑可以與其他治療疼痛的藥物共同給藥,包括NSAIDS(非類固醇性抗炎藥)如阿司匹林、布洛芬(ibuprofen)、萘普生(naproxen)、塞來考布(celecoxib)、對乙酰氨基酚,以及其他環加氧酶抑制劑;阿片類如可待因、羥考酮、嗎啡、美沙酮(methadone)、和芬太尼;抗驚厥藥和抗心律不齊藥如苯妥英(phenytoin)和卡馬西平(carbamazepine);以及抗抑郁藥如阿米替林(amitriptyline)、丙咪嗪(imipramine)、文拉法辛(venlafaxine)、可樂定(clonidine)和其他活性α2受體激動劑化合物。這樣的共同給藥可以是同時的,其中右美托咪定和另一種疼痛治療藥物二者在相同時間給藥。可替換地,因為本文描述的舌下組合物的選擇性中度至快速起作用性質,所以患者可以按常規方案給予長時間作用于疼痛的藥物,其中按需要在全天或按要求間斷地給予舌下噴霧右美托咪定。在某些情況下,長時間起作用的疼痛治療藥物的劑量可以減少,因為由右美托咪定產生的有益協同效應,這補充了最初的藥理治療。尤其是,右美托咪定可以顯著地增強阿片類的效能,允許所需要的阿片劑量減少同時維持等同的治療效用。右美托咪定、或其藥用鹽或衍生物的鎮痛舌下噴霧制劑(或本文中的其他舌下和/或頰部制劑)優選以經計量的劑量提供,以使預定量的活性藥物成分正確地以藥物有效量給予受試者。例如,舌下噴霧制劑可以包裝為在泵噴霧系統中含有多個劑量的大量液體,該泵噴霧系統包括安裝有計量泵的密閉容器。典型地,人類患者通過舌下自行給藥進行治療,如通過從噴霧泵的一次或多次啟動。本文中的舌下噴霧遞送實例的優點是通過單次、離散的啟動根據需要通過單個劑量滴定患者的能力。這個優點通常不存在于其中在標準方案中給予全能劑量(one-size-fits-alldosage)的其他藥物遞送形式(如貼劑、錠劑、片劑和栓劑)中。舌下噴霧制劑的其他優點包括它們使用方便,尤其是當沒有健康護理專業人員在場下自行給藥時。泵啟動噴霧特征在于要求施加用于啟動的外部壓力,例如,外部的手動、機械、或電啟動的壓力。這與增壓系統相反,如推進劑驅動的氣溶膠或壓縮氣體噴霧,其中的啟動典型地通過壓力的受控釋放實現,例如通過閥門的受控打開。在某些實施方式中,優選泵噴霧,因為泵噴霧與本文中的制劑一起使用,允許給予具有小的平均直徑和可控尺寸分布的液滴(微滴,droplet)或液滴的顆粒。在其他實施方式中,包含加壓推進氣體(如二氧化碳、氮、氯氟碳、氫氟烷烴等)的儲罐的加壓系統可以產生適合的顆粒或液滴。具有太小直徑的液滴或顆粒具有在給藥后進入人的肺中的可能性。在某些優選的實施方式中,與用例如滴管置于舌下相反,被遞送制劑的液滴尺寸通過在舌下噴霧進一步提供了增大的表面積。噴霧顆粒的尺寸和噴射模式的形狀也可以有助于活性成分是否被吸收到不同于口腔粘膜的身體系統(如肺)中。噴霧泵裝置可以是預先計量或,可替換地,該裝置可以是裝置計量的。預先計量裝置優選包括可以在制造過程中或在使用前由患者包含在該裝置中的預先測量的劑量或在某些類型單元(如溶液的單個單位劑量、單個或多個泡或其他空腔)中的劑量部分。典型的裝置計量單元具有容納足夠用于多劑量的制劑的儲罐,這些劑量在患者啟動時通過裝置自身作為計量的噴霧劑遞送。裝置可以計量遞送的藥物量(即每次啟動的劑量),以及每個劑量之間的時間長度。通過限制劑量能夠被遞送至患者的頻率,能夠防止過度使用限制的每個劑量之間的時間。制造的考慮包括能夠影響右美托咪定、其藥用鹽、或其衍生物在舌下的遞送的劑量重現性、噴霧羽流(sprayplume)、和顆粒/液滴尺寸分布。通過滿期注明日期維持這些參數的重現性,以及通過其在患者使用條件下的壽命期確保裝置的功能性(例如噴霧機制、電子特性、傳感器等)是重要的,因為這些參數的任何改變能夠導致給藥劑量和吸收的變化,這能夠導致潛在的副作用和下降的治療效用。給予的噴霧制劑的劑量可以取決于容器密閉系統的設計、重現性和性能特性。提供期望的液滴/顆粒尺寸分布的適合裝置對于右美托咪定產品的正確性能是一個重要因素。啟動參數(如力量、速度、保持和返回時間)對于裝置也應該被考慮。此外,該裝置應與制劑組分相容。而且,該裝置應設計成,當根據患者使用說明進行使用時,預防包含右美托咪定、其藥用鹽、或其衍生物的右美托咪定制劑的部分計量以及過計量。一種典型的噴霧劑遞送裝置包括基本單元(baseunit)、釋放啟動器、用于將制劑從裝置釋放的噴嘴、以及儲罐。優選地,儲罐在分配給患者之前,如在制造點,用藥物和其他賦形劑(如液體載體、香料、甜味劑等,如在本文其他地方述及的)填充。優選地,該儲罐限定在啟動后釋放的測定量的右美托咪定、其藥用鹽、或其衍生物。儲罐體可以是任何可接受的材料,如不銹鋼、透明材料等,以使其生產非常簡單。用于激活釋放的相對于噴嘴可移動的啟動器,可以提供在裝置上或與裝置在設置一起。在啟動移動過程中,儲罐打開,例如通過刺穿,從而通過噴嘴給予單個劑量。在啟動位置后的啟動行程的一部分期間,形成高壓。在相同方向持續的啟動移動的隨后部分中,介質可在一側釋放壓力并流至噴嘴。以這樣的方式,通過壓力作用將介質從儲罐并通過噴嘴推出。典型地,當液體制劑離開噴嘴,液滴沿著受噴嘴形狀、以及施加的壓力影響的軌道運行。在一些實施方式中,液滴尺寸、噴霧幾何形狀、和噴射方式依賴于泵的設計和/或制劑的性質。在某些實施方式中,啟動器的定向、泵設計和制劑的性質將影響噴霧的對稱性和形狀。噴霧方式也可以優化以在更寬路徑范圍分散液滴,由此增加能夠吸收化合物的表面積并減少吞咽反射。噴霧裝置可進一步設計成有利于方便患者使用和將給予的噴霧劑置于口腔粘膜的特定區域。前面優先的噴霧劑實施方式不用于限制。在實現本發明中,包含右美托咪定的制劑可以可替換地或另外地作為其他舌下和/或頰部相容性劑型提供。例如,本發明的發明人考慮了通過滴管或類似裝置作為與給藥方式相容的液體提供舌下液體。在另一個實例中,舌下制劑可以包裝在帶有可折斷頂部的藥用單位劑量瓶中,以運行打開的藥瓶在患者舌下傾斜而分配單個劑量的制劑。實施例以下的右美托咪定的舌下制劑通過混合表1中列出的組分制備。每個組分的相對量以重量計列出。表1**期望pH為約6.5至7.0,其比質子化的右美托咪定的pKa(pKa=7.1)稍微偏酸性表1中描述的制劑在哺乳動物中進行測試,如本文下面描述的。表1中的三個制劑的物理性質也在下面的表2中描述。表2制劑試驗編號外觀pH比重(g/mL)粘度(cP)“27”澄清、輕微淺黃色液體6.61.0704.05“28”*清澈、無色液體6.61.0752.89“29”**清澈、無色液體6.21.0782.63研究的目的是評估表1和2中描述的不同制劑在舌下噴霧給藥后,五只小獵犬(雄性、每只年齡為5至8個月并且體重在7.5和9.2kg之間)的組中右美托咪定的藥代動力學和絕對生物利用度。動物的倫理處理按照美國農業部動物福祉法案(USDAAnimalWelfareAct)(9C.F.R.,第1、2和3部分)中概述的原則和在實驗室動物的管理和使用指南(GuidefortheCareandUseofLaboratoryAnimals)(ILAR出版,1996,NationalAcademyPress)中規定的條件,其中考慮到受試者的福利與推進動物和人類的健康護理的可能性平衡。對于舌下給藥,噴霧劑應用通過泵裝置的一次下沉而給予到舌下的口腔中。為了確保正確的灌泵(pumppriming),在給藥前進行兩次啟動。在給藥后,在舌下給藥后的0(給藥前)、0.083、0.167、0.25、0.33、0.5、1、2和6小時,通過頸靜脈的靜脈穿刺從每個受試動物收集系列血液樣品。所有的舌下給藥沒有顯示不良反應。舌下給藥后,動物在給藥后的全部時間看起來正常。血液樣品收集在含有K2EDTA作為抗凝劑的真空管(vacutainertube)中,并將得到的血漿樣品冷凍儲藏直至分析。基于受試者的體重、給藥量、臨床觀察、和血液取樣時間的數據分析,表明舌下給藥的右美托咪定具有的Cmax=0.914ng/mL和Tmax=20min。以下的右美托咪定的舌下噴霧制劑通過混合表3中列出的組分制備,以提供每100μL含有50μg的右美托咪定。每個組分的量以重量計(g)列出,并且所得的制劑為0.05%(w/w)的右美托咪定。表3表3中的兩種制劑的物理性質在下面的表4中描述。表4制劑試驗編號外觀pH粘度(cp)B33清澈、極淺黃色液體7.24.34A34清澈、無色液體6.03.81這些制劑均利用制藥領域中熟知的設備制造。通過實例的方式,使用下面的方法來進行制劑試驗第“33B”號。每個成分在環境條件(67°F至72°F,相對濕度41%至56%)下進行稱重。將尼泊金甲酯和尼泊金丙酯溶解在乙醇中,將所得溶液加入到第一部分水中。混合物與聚維酮一起攪拌,直至完全溶解。將右美托咪定鹽酸鹽(粉末)加入到該溶液中,攪拌直到所有粉末已溶解。接著,加入麥芽糖醇糖漿,然后攪拌該溶液直至看起來同質(均勻)。最初在3.53的pH通過逐滴加入氫氧化鈉調節直至pH為6.99。總共加入5.7g氫氧化鈉溶液。加入足量的水(38.8g)使總重量至1000g。進行人類臨床研究以評估本文中描述的方法和組合物。在一個本文中稱為REC-09-001的實例中,執行第I階段、單劑量、3-方交叉研究,涉及24名男性和女性受試者。受試者分為4個治療組,涉及下面的制劑和劑量:1)制劑DEX-SL.01=50μg(1次泵啟動);2)制劑DEX-SL.01=100μg(2次泵啟動);3)制劑DEX-SL.02=50μg*(1次泵啟動);和4)商購10分鐘內的靜脈內(I.V.)50μg。表5*根據A的液體介質和藥物C的相對密度調節的API以上的表5示出了用于DEX-SL.03/.04的制劑,其中DEX-SL.03是為該制劑提供有用于給藥的50μL噴霧泵的這種制劑,而DEX-SL.04是作為總計100μL(即50μg劑量)的滴劑給予的這種相同制劑。研究結果表明,在研究的第1階段(交叉前),大量受試者經歷給藥后的低血壓,如下:受試者R006(100μg)=暈厥/眩暈發作約2分鐘;受試者R008(50μgIV)=給藥后直立性低血壓約4h;受試者R018(50μgIV)-經歷需要IV鹽水治療的直立性低血壓,給藥5h后恢復;以及受試者R021(100μg)=給藥1.25h后低血壓,并在給藥后4.5h時需要IV鹽水治療。在所有治療組中均觀察到鎮靜作用,其中在100μg舌下給藥組中觀察到的鎮靜處于明顯高于50μg舌下給藥組的水平。鑒于這些觀察結果,包括副作用以及不期望的高水平鎮靜作用,本發明的發明人在第2期和后續研究期中取消了100μg劑量。而且,將50μg的靜脈內劑量減少到25μg。本發明的發明人還將標準生命體征測量移到最先的4小時,并對每位受試者增加給藥前葡萄糖評估。在第2期前有三位受試者退出,如下:受試者R002,由于個人原因;受試者R003,由于在第1期中經歷的AE;和受試者R024,由于在第2期中給藥前的心動過緩。然后,余下的受試者重新隨機化,以確保所有受試者接受50μg的制劑(舌下噴霧劑)。在第2期中,又觀察到了低血壓,但是比第1期中的程度輕。在所有的治療組中也觀察到鎮靜作用。來自研究REC-09-001的其他觀察結果在本文的表中以及圖1-6中舉例說明。明顯地,如圖1-6中顯示的,在研究REC-09-001中,50μg的舌下制劑達到在約0.130至約0.245ng/mL之間的Cmax,并顯示出比100μg的舌下給藥(在約0.299至約0.574ng/mL之間的Cmax)更少的鎮靜作用以及比50μg和25μg的靜脈內(I.V)制劑(分別在約1.14至約1.72ng/mL之間和約0.496至約0.844ng/mL之間的Cmax)更少的鎮靜作用。此外,所有舌下制劑的Tmax平均為約60分鐘,而靜脈內(I.V)制劑平均為約10分鐘。在另一個實例中,進行了人第I階段臨床研究,本文中稱為REC-09-004。該研究為單劑量、3-因素完全交叉,涉及12名正常健康受試者。包括包含右美托咪定的三種制劑,如下:1)老制劑:DEX-SL.01=50μg(噴霧劑-用50μL的泵給予,以便2次啟動遞送50μg劑量);2)新制劑:DEX-SL.03—50μg(噴霧劑-用50μL的泵給予,以便2次啟動遞送50μg劑量);和3)新制劑:DEX-SL.04—50μg(滴劑-舌下給予)。然而,相比于研究REC-09-001的結果,發現來自這個患者群的藥代動力學(“PK”)結果不一致。因此,增加了另外的兩個治療,以提供另外的數據以及評價兩個可疑變量因素,即100μL與50μL的泵的使用以及口腔pH的影響的可能影響。因此,8名受試者用于兩個額外研究期的,其接受:4)DEX-SL.01—50μg(用100μL的泵給藥以一次啟動提供50μg的劑量);和5)DEX-SL.01—50μg(在口腔pH緩沖至~8.0后)。研究的結果在圖7-14中舉例說明。如所示的,對于每個制劑,右美托咪定的濃度在2小時內達到頂峰,達到低于0.15ng/ml的峰值Cmax,然后緩慢下降但在至少5小時內維持大于0.05的Cmax。在另一個實例中,執行另一個人第I階段臨床研究,本文中稱為REC-09-003。該研究涉及24名慢性下腰痛(CLBP)患者;12名為非阿片使用者,而另外9名為阿片使用者。研究分為兩部分。第1部分設計成評估在疼痛狀態下的血壓、心率、和鎮靜作用,并且也評估鎮痛。在第1部分中,給予的制劑為DEX-SL.0150μg(用50μL的泵給藥(2次啟動=50μg的劑量);與安慰劑相比)。第2部分設計成評估多劑量的安全性(q.6小時),以及右美托咪定聯用阿片的作用。同樣,給予的制劑為50μg的DEX-SL.01(用50μL的泵給藥(2次啟動=50μg的劑量))。鎮痛效果利用以下測量:1)涉及直觀類比標度的疼痛強度分數(范圍為0至100),其中表示沒有疼痛,而100表示可想到的最壞的疼痛;和2)疼痛緩解分數,其中0表示沒有疼痛,1表示輕微緩解,2表示中度緩解,3表示大多數緩解,而4表示完全緩解。研究REC-09-003的結果在圖7-20圖解示出。這些圖集中地說明了單劑量和多劑量的藥代動力學。圖7舉例說明了在第1部分中單劑量的藥代動力學,其中在阿片和非阿片患者組之間的反應方面沒有觀察到差別。如圖8-10所示,在藥物制劑和安慰劑之間在疼痛強度方面觀察到顯著的差異。對于第1部分,圖7舉例說明了在疼痛強度、鎮痛、和疼痛緩解方面觀察到的結果。圖11舉例說明了關于鎮痛觀察到的結果,而圖12-14分別舉例說明了第1部分對于靜息心率、靜息收縮壓和靜息舒張壓的觀察結果。關于在研究REC-09-003中的鎮靜作用,通過觀察者和患者進行測量。在觀察者情況下,應用拉姆齊鎮靜量表,如下:第1級=焦慮、激動、或不安;第2級=合作的、有方向的、和安靜的;或第3級=鎮靜但對指令有反應的水平;第4級=睡著;對輕敲眼瞼或大聲的耳朵刺激有敏捷反應;第5級=睡著;對輕敲眼瞼或大聲的耳朵刺激有遲緩反應;第6級=睡著;對疼痛刺激沒有反應。關于在研究REC-09-003中的患者受試者,應用斯坦福瞌睡量表,其中受試患者將他們鎮靜的程度評定為:第1級=感覺活躍、充滿活力的、警覺的、或完全清醒的;第2級=機能在高水平,但不在頂點,能夠集中;第3級=清醒,但放松;有反應但不完全警覺;第4級=有些迷糊,松勁;第5級=迷糊,對保持清醒失去興趣;緩慢;第6級=瞌睡、昏沉、掙扎睡眠;更喜歡躺下;或第7級=不再掙扎睡眠,馬上入睡;具有像做夢的思維。明顯地,在拉姆齊鎮靜量表上,所有受試者在基線處標定為“2”和12小時,實現峰值鎮靜作用,其中43%的DEX-SL.01受試者在2小時標定為第3級。明顯地,只有1名DEX-SL.01受試者在任何時間的定級高于第3級。至于患者在斯坦福瞌睡量表上的自我評價,所有受試者在基線處定級低于或等于第3級。69%的DEX-SL.01受試者經歷了峰值睡意,如由在2小時高于3的自我評級表明的。在研究REC-09-003的第2部分中,評估了多劑量的制劑的作用。如圖15-19中舉例說明的,制劑DEX-SL.01的多個劑量在q.6小時(給藥6小時)處的藥代動力學和作用在阿片和非阿片患者受試者之間是相似的,其中峰值血液濃度出現在約1小時至約2小時之間,以及再次在約7小時至7.5小時之間。明顯地,每次給藥后,血藥濃度維持在0.05ng/mL以上達約5小時-其中分布曲線顯示出與單劑量藥代動力學的高相似性。如圖16所示,還評估了q.6小時的多劑量方案的疼痛強度。在每次給藥后約2小時出現疼痛強度的峰值下降,與圖15中的藥代動力學中顯示的Cmax峰值基本一致。相似地,如圖17-19所示,評估了多劑量對靜息心率、靜息收縮血壓和靜息舒張血壓的影響,其中出現的峰值變化與每次劑量的峰值Cmax一致。反彈血壓圖形/波峰有時與第二個劑量相關(在q.6小時后不久),如圖17所示。雖然參考示例性實施方式進行了這種描述,但是本領域技術人員應理解,在不背離本發明范圍的情況下,本發明可以進行各種變化,并且對于其中的要素(特征)可被等同替換替代。另外,在不背離本發明實質性范圍的情況下,可以進行多種變形以使特定的情形或材料適合于本發明的教導。而且,在本發明的描述中,已公開了示例性實施方式,雖然可能已使用了特定的術語,但是除非另外說明,這些術語僅以一般的和描述性的意思使用,并不用于限制的目的,因此權利要求的范圍不會由此被限制。此外,本領域技術人員應理解,本文述及的方法的某些步驟可以以變換的順序排列,或步驟可以組合。因此,本發明所附權利要求不局限于本文中公開的具體實施方式。當前第1頁1 2 3
相關技術
網友詢問留言
已有0條留言
- 還沒有人留言評論。精彩留言會獲得點贊!
1