一種新型的含銅生物玻璃納米涂層涂敷的雞蛋膜及其制備方法和應用與流程
本發明涉及一種新型的含銅生物玻璃納米涂層涂敷的雞蛋膜及其制備方法和應用,屬生物材料領域。
背景技術:
皮膚作為人體最大的器官,承擔保護身體內部器官和組織免受病原微生物和物理化學性、機械性侵襲的重要功能。在外界致傷因子如外科手術、外力、火災以及機體內在因素如局部血液供應障礙等作用下會形成創面。創面一旦形成,皮膚的完整性破壞,造成組織丟失,其正常功能受損甚至將會威脅生命。傳統的皮膚修復通常采用自體組織移植和異體組織移植的方法。自體組織和器官移植雖然具有良好的修復效果,但面臨供體來源缺乏、第二次手術等條件的制約;異體、異種移植不僅面臨供體來源少的限制,而且存在引起免疫排斥反應、傳播病原等風險[1]。近些年興起的皮膚組織工程為解決這些問題提供了一種優越的方法,這種方法的核心是利用人工合成的皮膚敷料,結合皮膚組織細胞及生長因子來構建工程化皮膚,有效治療和修復大面積皮膚缺損。因此,設計新型創面敷料,提高創面修復質量成為研究者們的關注熱點。
設計創面敷料的基本原則包括預防和控制傷口感染,具有適當的通透性以便氣體流通和滲出液的排出,同時具有促進傷口處成血管的能力以提高創面修復的質量[2]。傷口組織處的新生血管有利于氧氣等營養物質和廢物代謝物的運輸和傳遞,有利于肉芽組織的形成和保持[3]。防止細菌等微生物的入侵,保持傷口處的清潔和濕潤的微環境是創面治療與修復過程中的必要條件[4]。因此,設計同時具備成血管能力和抗菌能力的創面敷料成為一大挑戰。
無機材料銅離子cu2+可以通過穩定低氧誘導因子(hypoxia-induciblefactor,hif-1α)的表達,模擬體內低氧環境,提高內皮細胞生長因子(vascularendothelialgrowthfactor,vegf)的表達,進而調控內皮細胞與成血管因子之間的相互作用,促進成血管化[5]。同時,cu2+具有明顯的抗菌效果,易在菌膜表面沉積并改變菌膜的通透性,使細菌內部的膜蛋白質、脂多糖等生物分子外流,從而造成細菌損傷[6]。研究人員已經發現cu2+對大腸桿菌、耐甲基西林金黃色葡萄球菌、艱難梭狀芽孢桿菌等細菌的活性有明顯抑制作用[7]。生物活性玻璃(bioactiveglass,bg)具有優良的生物活性、生物相容性和化學穩定性,在硬組織修復中應用廣泛。同時,生物玻璃能夠與皮膚等軟組織形成良好的結合,促進內皮細胞、成纖維細胞增 殖的增殖與粘附,以及刺激血管內皮生長因子的表達和蛋白分泌,因此,越來越多的研究人員將生物活性玻璃用于皮膚、心臟、血管等軟組織修復中[8]。
天然生物材料雞蛋膜(eggshellmembrane,esm)是介于雞蛋殼與蛋清之間的一層膜,厚度約為60-70μm,其主要成分為蛋白質,富含膠原蛋白(i,v和x型)。雞蛋膜具有纖維多孔結構,比表面積大,氣體通透性高,具有良好的抗菌性,材料便宜等優勢[9],有望用于創面敷料的基體材料。脈沖激光沉積(pulsedlaserdeposition,pld)技術利用高功率的脈沖激光聚焦于靶材表面,產生燒蝕等離子體,等離子體定向局域膨脹在襯底上沉積形成薄膜[10]。因其可在室溫下,原位制備均勻穩定的納米涂層得到廣泛應用。
參考文獻
[1]metcalfead,fergusonmwj.bioengineeringskinusingmechanismsofregenerationandrepair.biomaterials,2007,28(34):5100–5113.
[2]yildirimerl,thanhntk,seifalianam.skinregenerationscaffolds:amultimodalbottom-upapproach.trendsbiotechnol,2012,30(12):638–648.
[3]aguirrea,gonzáleza,navarrom,etal.controlofmicroenvironmentalcueswithasmartbiomaterialcompositepromotesendothelialprogenitorcellangiogenesis.eurcellsmater,2012,24(7):90-106.
[4]grzybowskij,janiakmk,oidake,etal.newcytokinedressings.ii.stimulationofoxidativeburstinleucocytesinvitroandreductionofviablebacteriawithinaninfectedwound.intjpharmaceut,1999,184(2):179–187.
[5]wuc,zhouy,xum,etal.copper-containingmesoporousbioactiveglassscaffoldswithmultifunctionalpropertiesofangiogenesiscapacity,osteostimulationandantibacterialactivity.biomaterials,2013,34(2):422-433.
[6]artunduagabonillajj,paredesguerrerodj,sánchezsuárezci,etal.invitroantifungalactivityofsilvernanoparticlesagainstfluconazole-resistantcandidaspecies.worldj.microb.biot.2015;31:1801-9.
[7]chatterjeeak,chakrabortyr,basut.mechanismofantibacterialactivityofcoppernanoparticles.nanotechnology,2014,25(13):135101.
[8]miguez-pachecov,henchll,boccacciniar.bioactiveglassesbeyondboneandteeth:emergingapplicationsincontactwithsofttissues.actabiomater,2015,13:1-15.
[9]
[10]wuc,zhaid,mah,etal.stimulationofosteogenicandangiogenicabilityofcellsonpolymersbypulsedlaserdepositionofuniformakermanite-glassnanolayer.actabiomater,2014, 10(7):3295-3306.。
技術實現要素:
本發明的目的為提供一種新型的含銅生物玻璃納米涂層涂覆的雞蛋膜及其制備方法。本發明的另一目的在于提供一種新型的含銅生物玻璃納米涂層涂覆的雞蛋膜在創面修復方面的應用。
為了達到這個目的,本發明提供了一種含銅生物玻璃納米涂層涂覆的雞蛋膜,所述含銅生物玻璃納米涂層涂覆的雞蛋膜包括具有纖維多孔結構的天然雞蛋膜以及沉積于具有纖維多孔結構的天然雞蛋膜表面的含銅生物玻璃納米涂層,所述含銅生物玻璃納米涂層中銅是以cu2+的形式均勻分布在si-ca-p生物玻璃中,所述cu2+的摩爾百分含量為0-5mol%,優選為大于0且為5mol%以下。
本發明采用脈沖激光沉積技術在雞蛋膜表面制備具有結構穩定的含銅生物玻璃納米涂層,提高了雞蛋膜表面的生物活性及抗菌性能。含銅生物玻璃納米涂層涂敷的雞蛋膜能夠利用該納米涂層中所含cu2+的成血管化作用及抗菌性能與雞蛋膜的纖維多孔結構,刺激并促進皮膚組織細胞的生長以及成血管相關基因與蛋白質的表達,有效預防傷口處的細菌感染,提高創面修復材料的生物活性和創面愈合質量。這將對于促進大面積創面愈合具有很高的研究價值。
較佳地,所述si-ca-p生物玻璃的主相為sio2和casio3。
較佳地,所述si-ca-p生物玻璃中sio2的相體積分數為50-80%,所述casio3的相體積分數與sio2的相體積分數的比為(0.1-0.25):1。
較佳地,所述含銅生物玻璃納米涂層的厚度為30-50nm,優選為40-50nm。
本發明還提供了一種含銅生物玻璃納米涂層涂敷的雞蛋膜的制備方法,包括:
采用正硅酸乙酯、磷酸三乙酯和四水合硝酸鈣為原料,以三水合硝酸銅為銅源,經溶膠、凝膠、陳化、干燥后在800-1000℃下煅燒2-5小時得到含cu的si-ca-p生物玻璃陶瓷粉體;
將所得含cu的si-ca-p生物玻璃陶瓷粉體經壓片后,并在1000-1400℃下煅燒2-5小時得到含cu的si-ca-p生物玻璃陶瓷;
以所得的含cu的si-ca-p生物玻璃陶瓷為靶材,以洗凈并風干后的雞蛋膜為襯底,采用脈沖激光沉淀法在襯底表面沉積含銅生物玻璃納米涂層。
較佳地,所述脈沖激光沉淀法中使用krf激光器,激光器頻率1-5hz;襯底與靶材之間的距離為5-10cm,激光束與靶材表面成30-60°角;脈沖激光沉積控制在室溫下,氧氣壓強為20-40pa,激光能量為120-180mj,沉積時間5-40分鐘。
除此之外,本發明還提供了一種含銅生物玻璃納米涂層涂敷的雞蛋膜在創面修復中的應用。
本發明通過脈沖激光沉積方法制備了含銅生物玻璃納米涂層涂覆的雞蛋膜,提高了雞蛋膜表面的生物活性及抗菌性能。通過脈沖激光沉積方法制備了含cu生物玻璃涂敷的雞蛋膜,具有工藝簡單,操作條件易于控制等優點。含cu生物玻璃納米涂層涂敷的雞蛋膜能夠有效釋放cu2+,促進創面區域的血管新生,用于創面修復材料具有良好的生物活性和抗菌性能,可顯著促進創面修復質量。因此,本發明制備的新型的含銅生物玻璃納米涂層涂覆的雞蛋膜在皮膚組織工程敷料材料的應用上具有很強的實用意義。
附圖說明
圖1為不同cu含量的si-ca-p生物玻璃陶瓷及不含cu的生物玻璃噴涂的雞蛋膜(0cu-bg/esm),含2mol%cu的生物玻璃噴涂的雞蛋膜(2cu-bg/esm),含5mol%cu的生物玻璃噴涂的雞蛋膜(5cu-bg/esm)外表面(貼近蛋殼)的xrd圖;
圖2為純雞蛋膜(esm),0cu-bg/esm,2cu-bg/esm,5cu-bg/esm薄膜的掃描電鏡照片;
圖3為5cu-bg/esm薄膜表面的元素mapping圖;
圖4為0cu-bg/esm與5cu-bg/esm薄膜的透射電鏡照片;
圖5為esm,xcu-bg/esm薄膜的表面硬度和接觸角圖片;
圖6為esm,xcu-bg/esm薄膜材料對大腸桿菌存活率的影響情況;
圖7為人臍靜脈內皮細胞(huvecs)在esm,xcu-bg/esm薄膜表面的粘附情況;
圖8為esm,xcu-bg/esm薄膜對huvecs的細胞增殖情況;
圖9為7天后,esm,xcu-bg/esm薄膜對huvecs成血管基因(vegf,hif-1α,kdr,enos)表達的情況;
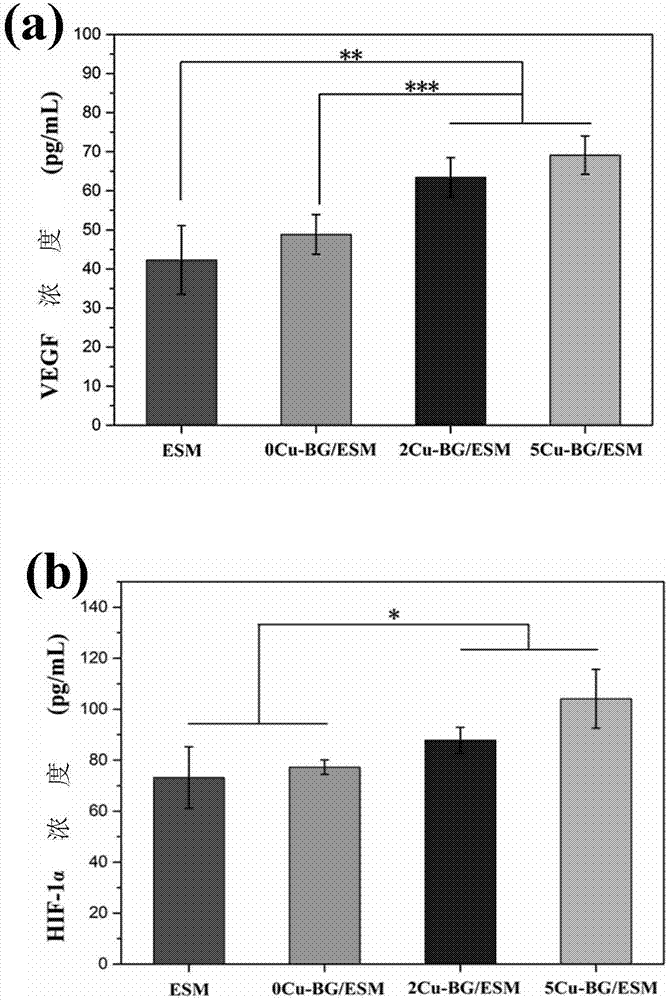
圖10為7天后,esm,xcu-bg/esm薄膜對huvecs成血管蛋白質(vegf,hif-1α)表達的情況;
圖11為將esm,xcu-bg/esm修復材料分別植入實驗鼠背部創傷區域,創傷面積隨時間的變化情況;
圖12為7天后,分別經過esm,xcu-bg/esm修復材料處理后的創傷區域組織的組織熒光染色(cd31)觀察情況;
圖13為7天后,分別經過esm,xcu-bg/esm修復材料處理后的masson’s三色染色情況,反應傷口處上皮組織的形成情況。
具體實施方式
以下結合實施方式進一步說明本發明,應理解,下述實施方式僅用于說明本發明,而非限制本發明。
本發明通過脈沖激光沉積技術制備了新型的含銅生物玻璃納米涂層涂敷的雞蛋膜,所述新型的含銅生物玻璃納米涂層涂覆的雞蛋膜包括具有纖維多孔結構的天然雞蛋膜以及沉積于具有纖維多孔結構的天然雞蛋膜表面的含銅生物玻璃納米涂層。
上述含銅生物玻璃納米涂層中銅是以cu2+的形式均勻分布在si-ca-p生物玻璃中。具體來說,本發明中銅是以cu3(po4)2的形式存在含cu的si-ca-p生物玻璃陶瓷中。其中,所述cu2+的摩爾百分含量為的0-5mol%。合適的含銅量可以通過穩定低氧誘導因子的表達,模擬體內低氧環境,提高內皮細胞生長因子的表達,進而調控內皮細胞與成血管因子之間的相互作用,促進成血管化。同時,cu2+具有明顯的抗菌效果,易在菌膜表面沉積并改變菌膜的通透性,使細菌內部的膜蛋白質、脂多糖等生物分子外流,從而造成細菌損傷。
上述si-ca-p生物玻璃的主相為sio2和casio3。si-ca-p生物玻璃具有優良的生物活性、生物相容性和化學穩定性,在硬組織修復中應用廣泛。同時,生物玻璃能夠與皮膚等軟組織形成良好的結合,促進內皮細胞、成纖維細胞增殖的增殖與粘附,以及刺激血管內皮生長因子的表達和蛋白分泌。其中,所述si-ca-p生物玻璃中sio2的相體積分數為50-80%,所述casio3的相體積分數與sio2的相體積分數的比為(0.1-0.25):1。此外除了主相外,所述si-ca-p生物玻璃中還有ca3(po4)2。
上述新型的含銅生物玻璃納米涂層的厚度為30-50nm,優選為40-50nm。
上述所述新型的含銅生物玻璃納米涂層涂敷的雞蛋膜中所述雞蛋膜介于雞蛋殼與蛋清之間的一層膜,厚度約為60-70μm,其主要成分為蛋白質,富含膠原蛋白(i、v和x型)。雞蛋膜具有纖維多孔結構,比表面積大,氣體通透性高,具有良好的抗菌性,材料便宜等優勢。
以下示例性的說明本發明提供的新型的含銅生物玻璃納米涂層涂敷的雞蛋膜的制備方法。
靶材的制備。本發明中用于脈沖激光沉積薄膜的靶材可為含cu的si-ca-p生物玻璃陶瓷。本發明采用正硅酸乙酯、磷酸三乙酯和四水合硝酸鈣為原料,以三水合硝酸銅為銅源,經溶膠、凝膠、陳化、干燥后在800-1000℃下煅燒2-5小時得到含cu的si-ca-p生物玻璃陶瓷粉體。再將所得含cu的si-ca-p生物玻璃陶瓷粉體經壓片后,并在1000-1400℃下煅燒2-5小時得到含cu的si-ca-p生物玻璃陶瓷。作為一個更詳細示例,實驗采用正硅酸乙酯(teos)、四水合硝酸鈣(ca(no3)2·4h2o)和磷酸三乙酯(tep)為原料,以三水合硝酸銅 (cu(no3)2·3h2o)為銅源,經溶膠、凝膠、陳化、干燥等過程,在800℃下煅燒得到含cu的si-ca-p生物玻璃陶瓷粉體;后經壓片(φ=25mm),并在1250℃下燒結得到含cu的si-ca-p生物玻璃陶瓷。
襯底的制備。本發明中實驗用脈沖激光沉積薄膜的襯底材料可為雞蛋膜。作為一個示例,取新鮮雞蛋,洗凈,小心揭下雞蛋膜,剪裁成大小為15×15mm的正方形,完全去除殘余蛋殼與蛋清,室溫下風干。
本發明以含cu的si-ca-p生物玻璃陶瓷為靶材,以洗凈并風干后的雞蛋膜為襯底,采用脈沖激光沉淀法襯底表面沉積含cu的si-ca-p生物玻璃納米涂層。本發明中實驗可采用krf激光器(波長248nm,脈沖寬度20ns),激光器頻率1-5hz,雞蛋膜與含cu的si-ca-p生物玻璃陶瓷靶材之間的距離可為5-10cm,激光束與靶材表面可成30-60°角。為提高沉積生物玻璃薄膜的均勻性以及防止靶材被擊穿,沉積過程中含cu的si-ca-p生物玻璃陶瓷以2400r/hr的速度旋轉。采用分子泵對沉積室抽真空至20-40pa,并使用機械泵控制其壓強。本實驗主要通過調節沉積溫度(室溫10-30℃),氧氣壓強(20-40pa)、靶基距(5-10cm)、激光能量(120-180mj)以及沉積時間(5-40min)來控制涂層的厚度、結晶度及晶粒大小。
本發明制備的新型的含銅生物玻璃納米涂層涂敷的雞蛋膜可應用于創面的修復。本發明系統的研究新型的含銅生物玻璃納米涂層涂敷的雞蛋膜的表面理化性質、抗菌性能,成血管化能力及促創面愈合質量,確定其能夠用作新型的創面修復敷料。
本發明制備的含銅生物玻璃納米涂層可通過廣角x射線衍射(xrd)、掃描電鏡(sem)、元素mapping及透射電鏡(tem)等手段對該納米涂層材料的物相組成、表面微觀機構與元素組成、涂層厚度進行分析與表征。通過對該納米涂層進行納米壓痕分析與接觸角測試,進一步分析涂層的表面硬度和親疏水性能。
下面進一步例舉實施例以詳細說明本發明。同樣應理解,以下實施例只用于對本發明進行進一步說明,不能理解為對本發明保護范圍的限制,本領域的技術人員根據本發明的上述內容作出的一些非本質的改進和調整均屬于本發明的保護范圍。下述示例具體的工藝參數等也僅是合適范圍中的一個示例,即本領域技術人員可以通過本文的說明做合適的范圍內選擇,而并非要限定于下文示例的具體數值。
實施例1:含cu生物玻璃納米涂層涂敷的雞蛋膜的制備
實驗采用正硅酸乙酯(teos)、ca(no3)2·4h2o和磷酸三乙酯(tep)為原料,cu(no3)2·3h2o為銅源,經溶膠、凝膠、陳化、干燥等過程,在800℃下煅燒得到含cu的si-ca-p生物玻 璃陶瓷粉體;后經壓片(φ=25mm),并在1250℃下燒結得到含cu的si-ca-p生物玻璃陶瓷塊體。取新鮮雞蛋,洗凈,小心揭下雞蛋膜,剪裁成大小為15×15mm的正方形,完全去除殘余蛋殼與蛋清,室溫下風干。實驗采用krf激光器(波長248nm,脈沖寬度20ns)。激光器頻率5hz,雞蛋膜襯底與生物玻璃靶材之間的距離設為5.5cm,激光束與靶材表面成45°角。為提高沉積薄膜的均勻性以及防止靶材被擊穿,沉積過程中含xcu-bg以2400r/hr的速度旋轉。采用分子泵對沉積室抽真空到20pa,并使用機械泵控制其壓強。本實驗主要通過調控沉積溫度(室溫)、氧氣壓強(20pa)、靶基距(5.5cm)、激光能量(160mj)以及沉積時間(40min)來控制涂層的厚度、結晶度及晶粒大小。
檢測所得生物玻璃納米涂層的效果。
所獲得的生物玻璃納米涂層通過廣角x射線衍射(xrd)、掃描電鏡(sem)、元素mapping及透射電鏡(tem)等手段對該納米涂層材料的物相組成、表面微觀機構與元素組成、涂層厚度進行分析與表征。通過對該納米涂層進行納米壓痕分析與接觸角測試,進一步分析涂層的表面硬度和親疏水性能。圖1為不同cu含量的si-ca-p生物玻璃陶瓷及不含cu的生物玻璃噴涂的雞蛋膜(0cu-bg/esm),含2mol%cu的生物玻璃噴涂的雞蛋膜(2cu-bg/esm),含5mol%cu的生物玻璃噴涂的雞蛋膜(5cu-bg/esm)外表面(貼近蛋殼)的xrd圖。附圖1中(a)為不同cu含量的si-ca-p生物玻璃陶瓷及(b)為雞蛋膜和xcu-bg/esm薄膜的xrd圖,其中,該si-ca-p生物玻璃陶瓷的主相是sio2和casio3,經脈沖激光沉積(pld)技術在雞蛋膜表面噴涂的生物玻璃納米涂層為無定型。圖2、圖3和圖4分別為esm、xcu-bg/esm薄膜的掃描電鏡、元素分析和透射電鏡照片。圖2為(a)(b)純雞蛋膜外表面(貼近蛋殼),(c)(d)0cu-bg/esm,(e)(f)0cu-bg/esm,(g)(h)5cu-bg/esm的掃描電鏡照片。圖3為(a)si元素,(b)ca元素,(c)p元素,(d)cu元素的元素分布照片。圖4為(a)(b)0cu-bg/esm,(c)(d)5cu-bg/esm的透射電鏡照片。從圖2、圖3和圖4中可知純雞蛋膜表面十分光滑,具有纖維多孔結構。經pld處理后,纖維表面形成了顆粒十分均勻的生物玻璃納米涂層。納米涂層中si、ca、p、cu各元素分布均勻。納米涂層的厚度約為40nm。圖5為esm、xcu-bg/esm薄膜的納米壓痕與接觸角測試結果,其中(a-d)分別為純雞蛋膜、0cu-bg/esm、2cu-bg/esm和5cu-bg/esm薄膜的接觸角照片,(e)為純雞蛋膜和xcu-bg/esm薄膜的納米壓痕硬度數據。從圖5中可知,生物玻璃納米涂層顯著提高了雞蛋膜的表面硬度與親水性。
實施例2:研究生物玻璃納米涂層中所含cu2+及雞蛋膜對大腸桿菌活性的影響情況
實驗通過檢測不同類型的材料對大腸桿菌活性的抑制情況,研究生物玻璃納米涂層中cu含 量對材料抗菌性能的影響。將esm,xcu-bg/esm四組材料剪裁成φ=10mm的圓形片狀,于75%的酒精中浸泡30min,徹底滅菌后,用磷酸鹽緩沖鹽水(pbs)清洗2次。無菌環境下,將新鮮大腸桿菌菌株稀釋至濃度約為2×108cfu/ml。將每組6片材料于4℃溫度下,在大腸桿菌懸浮液中浸泡4天。隨后,將細菌懸浮液稀釋6×104倍,取15μl涂平板,并在37℃下培養12h。最后,對各組大腸桿菌菌落數量進行計數,并計算細菌存活率;
圖6為各組材料對大腸桿菌存活率的影響情況,(a)為空白組、純esm組和5cu-bg/esm組大腸桿菌存活率的數據統計。(b)為0cu-bg/esm組、2cu-bg/esm和5cu-bg/esm組大腸桿菌存活率的數據統計。結果顯示,5cu-bg/esm薄膜的抗菌效果顯著,同時,隨cu含量在生物玻璃納米涂層中的增加,抗菌效果明顯增加。
實施例3:研究創面修復材料中含cu生物玻璃納米涂層對體外人臍靜脈內皮細胞(huvecs)粘附、增殖和成血管基因與蛋白質的影響。
3.1細胞粘附與增殖
將esm,xcu-bg/esm四組材料剪裁成φ=10mm的圓形片狀,于75%的酒精中浸泡30min,pbs清洗2次。將滅菌后的樣品在加有10%胎牛血清(fcs)的dmem培養基中浸泡,為種植細胞做準備。每個樣品表面種植6×103個細胞,使用的培養基為加有10%fcs的dmem,培養溫度為37℃,濕度95%,培養氣氛為含5%co2的空氣,培養基每兩天更換一次。培養1天后,樣品從培養基中取出,用濃度為4%的多聚甲醛溶液固定,pbs清洗后,用鬼筆環肽和dapi染料分別對細胞骨架和細胞核染色。材料表面的細胞形貌通過共聚焦顯微鏡觀察。
用mtt法來測試huvecs在材料表面的增殖。細胞培養1,3,7天后,從48孔板中完全移除培養基,每孔加入300μlmtt溶液(5mg/ml),在37℃下再培養4h。移除上清液同時加入二甲亞砜(dmso)溶解紫甲臜。用分光光度計在波長為590nm處測試溶液的吸光值。mtt值用吸光度表示,吸光度與材料表面活細胞的數量成正比。
圖7為huvecs細胞在不同類型材料表面的粘附情況,分別為(a-c)為純雞蛋膜,(d-f)0cu-bg/esm,(g-i)2cu-bg/esm,(j-l)5cu-bg/esm的細胞粘附照片。結果顯示,細胞在雞蛋膜表面數量少,且鋪展形態不理想。在xcu-bg/esm各組材料表面,細胞數量多,鋪展形態較好。圖8為培養1,3,7天后,huvecs細胞在各組材料表面的增殖情況。結果顯示,在3天和7天時,xcu-bg/esm各組的細胞增殖水平明顯高于esm組。7天時,2cu-bg/esm和5cu-bg/esm組增殖水平高于0cu-bg/esm組。
3.2成血管基因與蛋白質的表達
實驗各組中,成血管相關基因(vegf,hif-1α,kdr,enos)的表達采用實時-定量聚合酶鏈反應(rt-qpcr)檢測。成血管相關蛋白質(vegf,hif-1α)的表達采用酶聯免疫吸附實驗(elisa)檢測。
圖9為7天后,esm,xcu-bg/esm材料對huvecs成血管基因(vegf,hif-1α,kdr,enos)表達的情況,其中(a)為基因vegf,(b)為基因hif-1α,(c)為基因kdr,(d)為基因enos的表達情況。結果顯示,2cu-bg/esm與5cu-bg/esm材料顯著提高了成血管基因(vegf,hif-1α,kdr,enos)的表達。圖10為7天后,esm,xcu-bg/esm材料對huvecs成血管蛋白質(vegf,hif-1α)表達的情況,其中(a)為蛋白質vegf,(b)為蛋白質hif-1α的表達情況。結果顯示,隨生物玻璃納米圖層中cu含量的增加,vegf,hif-1α蛋白質表達越顯著。
實施例4:研究創面修復材料中含cu生物玻璃納米涂層對小鼠體內的創面修復質量的影響及其相關機理。
4.1體內全層創傷修復實驗
32只18g的雄性balb/c實驗鼠(國家嚙齒類實驗動物資源中心,中國上海分公司),將老鼠背部區域的毛發去除后,建立一個完整的厚度傷口(直徑為8mm)。將創面修復材料分別植入小鼠創傷區域,它們分別是:(1)空白對照組(control);(2)0cu-bg/esm;(3)2cu-bg/esm;(4)5cu-bg/esm,每組8只老鼠。實驗前,各組材料用75%的酒精浸泡滅菌30min,后用pbs清洗2次。植入后老鼠背部創傷區域用醫用膠帶固定。手術后,老鼠被分別關在無菌環境下的裝有充足水以及食物的籠子中。利用數碼相機在固定的時間點(1,3,5,7,9,11天)、固定的距離以及角度記錄創傷區域的變化情況;
另外,每組其中4只老鼠在7天時處死,取出創傷區域周圍的組織標本(2mm左右)進行組織分析。
圖11為將esm,xcu-bg/esm修復材料分別植入實驗鼠背部創傷區域,創傷面積隨時間的變化情況,其中(a)為植入不同材料后,實驗鼠背部創傷區域隨時間變化的數碼照片,(b)為植入不同材料后,實驗鼠創傷區域面積隨時間變化的數據統計。與空白對照組(control)和esm組相比,5cu-bg/esm組的傷口愈合較快。
4.2免疫組織熒光染色分析
將切片后的組織標本(5μm)在檸檬酸鈉緩沖溶液中浸泡20min,冷卻至室溫1h,后在4℃下進行一抗(rabbitpolyclonaltocd31antibody(abcam))孵化過夜。隨后,將其浸泡在pbs中清洗,室溫下進行2h小時的二抗孵化過程。最后,將dapi添加到樣品中(避光)。利用 熒光顯微鏡(leicaconfocalmicroscope)進行觀察分析。
圖12為7天后,分別經過esm,xcu-bg/esm修復材料處理后的創傷區域組織的組織熒光染色(cd31)觀察情況,其中(a)為cd31的染色圖片,(b)為cd31的定量數據統計。結果顯示,5cu-bg/esm組能夠顯著促進cd31的表達,即創傷區域血管的新生。
4.3創傷區域組織形態分析
將取得的組織標本用4%的多聚甲醛固定12h后,利用分級醇以及二甲苯脫水,并進行石蠟包埋,利用rm2155切片機切取5μm厚切片,采用蘇木精和曙紅對組織樣本進行常規組織染色固定。masson三色染色用作觀察創傷組織處膠原網絡的形成情況。采用奧林巴斯倒置顯微鏡觀察創傷區域情況,imageproplusversion6.0(mediacybernetics,rockville,md,usa)進行拍照,其中藍綠色表示膠原纖維。
圖13為7天后,分別經過esm,xcu-bg/esm修復材料處理后的masson’s三色染色情況,反應傷口處上皮組織的形成情況,其中(a)為空白組(control),(b)為0cu-bg/esm組,(c)為2cu-bg/esm組,(d)為5cu-bg/esm組的新上皮形成圖片。結果顯示,5cu-bg/esm組材料有利于促進傷口區域生成厚度均一且連續的上皮組織。
- 還沒有人留言評論。精彩留言會獲得點贊!