用于治療耵聹分泌過多的耳用制劑的制作方法
背景技術:
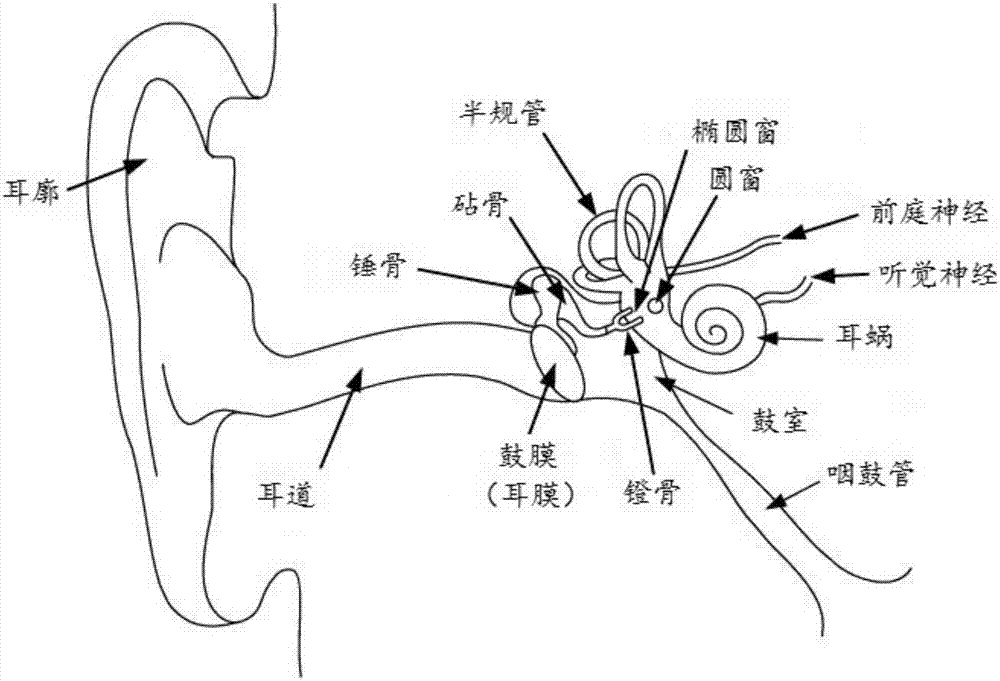
:耵聹,又稱外聽道(“eac”)垢或耳垢,是耳道中分泌的淡黃色蠟狀物質。耵聹有助于清潔和潤滑皮膚,并保護脆弱的皮膚區域免受潛在有害的生物體的侵害。技術實現要素:本文公開了適合向eac局部施用的、用于調節耵聹產生的藥物組合物。在一些實施方案中,所述組合物包含用于調節耵聹產生的耳用藥劑;以及耳可接受的凝膠。在一些實施方案中,所述耳可接受的凝膠為水性耳可接受的凝膠。在一些實施方案中,所述耳可接受的凝膠為耳外部可接受的凝膠。在一些實施方案中,所述耳外部可接受的凝膠為耳可接受的熱可逆性凝膠。在一些實施方案中,所述組合物具有約19℃至約42℃的膠凝溫度。在一些實施方案中,所述組合物具有約15,000cp至約1,000,000cp的表觀粘度。在一些實施方案中,所述組合物具有約100,000cp至約500,000cp的表觀粘度。在一些實施方案中,所述組合物具有約250,000cp至約500,000cp的表觀粘度。在一些實施方案中,所述組合物具有約150至約500mosm/l的實際容量摩爾滲透壓濃度。在一些實施方案中,所述組合物具有約200至約400mosm/l的實際容量摩爾滲透壓濃度。在一些實施方案中,所述組合物具有約250至約320mosm/l的實際容量摩爾滲透壓濃度。在一些實施方案中,所述耳用藥劑具有約30小時的平均溶出時間。在一些實施方案中,所述耳用藥劑經至少3天的時段從所述組合物中釋放。在一些實施方案中,所述耳用藥劑經至少4天的時段從所述組合物中釋放。在一些實施方案中,所述耳用藥劑經至少5天的時段從所述組合物中釋放。在一些實施方案中,所述耳用藥劑經至少7天的時段從所述組合物中釋放。在一些實施方案中,所述耳用藥劑經至少14天的時段從所述組合物中釋放。在一些實施方案中,所述耳用藥劑為中性分子、游離酸、游離堿、鹽、前藥或其組合的形式。在一些實施方案中,所述耳用藥劑包括多顆粒。在一些實施方案中,所述耳用藥劑基本為微粒化顆粒的形式。在一些實施方案中,所述耳用藥劑為微粒化顆粒的形式。在一些實施方案中,所述組合物的ph為約5.5至約9.0。在一些實施方案中,所述組合物的ph為約6.0至約8.5。在一些實施方案中,所述組合物的ph為約7.0至約8.0。在一些實施方案中,所述組合物基本不含醇溶劑。在一些實施方案中,所述組合物基本不含二元醇溶劑。在一些實施方案中,所述耳可接受的凝膠為生物可蝕解的。在一些實施方案中,所述耳用藥劑為膽堿酯或氨基甲酸酯、植物生物堿、可逆性膽堿酯酶抑制劑、乙酰膽堿釋放促進劑、抗腎上腺素能藥、擬交感神經藥或其組合。在一些實施方案中,所述耳用藥劑為膽堿酯或氨基甲酸酯,優選乙酰膽堿或卡巴膽堿。在一些實施方案中,所述耳用藥劑為植物生物堿,優選毛果蕓香堿。在一些實施方案中,所述耳用藥劑為可逆性膽堿酯酶抑制劑,優選新斯的明或毒扁豆堿。在一些實施方案中,所述耳用藥劑為乙酰膽堿釋放促進劑,優選氟哌利多、利培酮或曲唑酮。在一些實施方案中,所述耳用藥劑為抗腎上腺素能藥,優選可樂定、普萘洛爾、阿替洛爾或哌唑嗪。在一些實施方案中,所述耳用藥劑為擬交感神經藥,優選去甲腎上腺素或多巴胺。在一些實施方案中,所述組合物包含約0.1重量%至約20重量%的耳用藥劑。在一些實施方案中,所述組合物包含約1重量%至約10重量%的耳用藥劑。在一些實施方案中,所述組合物包含約5重量%至約8重量%的耳用藥劑。在一些實施方案中,所述組合物進一步包含一種或多種eac保護劑。在一些實施方案中,該eac保護劑選自角鯊烯、羊毛甾醇和膽固醇。在一些實施方案中,該eac保護劑為一種或多種抗微生物劑。在一些實施方案中,該抗微生物劑為抗微生物肽。在一些實施方案中,所述組合物用于治療耵聹分泌過多。在一些實施方案中,耵聹分泌過多與疾病或病況相關。在一些實施方案中,該疾病或病況為耳瘙癢、外耳炎、耳痛、耳鳴、眩暈、耳脹(earfullness)、聽力損失或其組合。本文還公開了調節耵聹產生的方法或治療耵聹分泌過多的方法。在一些實施方案中,該方法包括向有需要的個體施用藥物組合物,該藥物組合物包含一定量的調節耵聹產生的耳用藥劑;以及耳可接受的凝膠。在一些實施方案中,耵聹分泌過多與疾病或病況相關。在一些實施方案中,該疾病或病況為耳瘙癢、外耳炎、耳痛、耳鳴、眩暈、耳脹、聽力損失或其組合。在一些實施方案中,所述組合物局部施用于外聽道、鼓膜的外表面或其組合。在一些實施方案中,所述組合物不通過鼓膜施用。在一些實施方案中,所述方法進一步包括向有需要的個體施用eac保護劑。在一些實施方案中,該eac保護劑選自角鯊烷、羊毛甾醇和膽固醇。在一些實施方案中,該eac保護劑為一種或多種抗微生物劑。在一些實施方案中,該抗微生物劑為抗微生物肽。在一些實施方案中,所述eac保護劑并入包含所述耳用藥劑的藥物組合物中。在一些實施方案中,所述eac保護劑被配制成與包含所述耳用藥劑的藥物組合物分開施用的補充組合物。在一些實施方案中,該補充組合物進一步包含耳可接受的凝膠。在一些實施方案中,該補充組合物局部施用于外聽道、鼓膜的外表面或其組合。在一些實施方案中,該補充組合物不通過鼓膜施用。在一些實施方案中,在公開的方法中使用的藥物組合物如上所總結。在本文公開的藥物組合物或方法的一些實施方案中,所述藥物組合物不提供調節耵聹產生的耳用藥劑向中耳和/或內耳中的持續釋放。在本文公開的藥物組合物或方法的一些實施方案中,所述藥物組合物不提供調節耵聹產生的耳用藥劑向中耳和/或內耳中的任何釋放。通過以下詳細描述,本文所述的方法和組合物的其他特征和技術效果將變得顯而易見。然而應當理解,詳細描述和具體實例雖然指示具體實施方案,但僅以說明方式給出。附圖說明圖1示出了非持續釋放制劑與持續釋放制劑的比較。圖2示出了耳的解剖學。圖3顯示了活性劑從四種組合物中的預測的可調釋放。具體實施方式耵聹是正常和患病耳道均有的滲出物,其一旦積聚就可破壞或干擾正常的耳功能,并且甚至可引起患者的不適和疼痛。耵聹分泌過多或耵聹嵌塞可導致瘙癢、疼痛、漲感、噪聲以及甚至聽力損失。耳鼓堵塞可由于水進入耳道引起耳垢膨脹而非常突然地發生。這在游泳時將頭浸入水中的個體中是常見的情況,并且已知耳鳴以及甚至眩暈都由于耳壓增加而引起。去除耵聹的方法包括灌洗、灌洗之外的手動去除、用于軟化耵聹的耵聹溶解劑或其組合。這些方法有時會導致并發癥,諸如鼓膜穿孔、耳道撕裂、耳感染或聽力損失。本發明認識到向eac遞送藥物中的挑戰。在某些實施方案中,本文公開了用于調節耵聹產生的組合物、制劑、方法、用途、藥劑盒和遞送裝置。在某些實施方案中,本文公開了用于增加耵聹產生的組合物、制劑、方法、用途、藥劑盒和遞送裝置。在某些實施方案中,本文公開了用于防止或減少耵聹的積累或形成的組合物、制劑、方法、用途、藥劑盒和遞送裝置。在某些實施方案中,本文公開了用于去除耵聹的積累或形成的組合物、制劑、方法、用途、藥劑盒和遞送裝置。在某些實施方案中,本文公開了用于治療耵聹相關的疾病或病況如耵聹分泌過多的組合物、制劑、方法、用途、藥劑盒和遞送裝置。在某些實施方案中,本文公開了用于治療耵聹分泌過多相關的疾病或病況的組合物、制劑、方法、用途、藥劑盒和遞送裝置。本文還公開了用于調節耵聹的產生以及治療耵聹分泌過多和耵聹分泌過多相關疾病的控制釋放耳用組合物和制劑。本文所述的制劑提供了活性劑向外耳道環境中的恒定、持續、延長或延遲釋放速率,從而避免在耵聹產生、耵聹分泌過多和耵聹分泌過多相關疾病的治療中藥物暴露的任何可變性。本文進一步提供了以嚴格無菌性要求滅菌的且適合施用于外耳道的耳用制劑。在一些實施方案中,本文所述的耳相容性組合物基本不含致熱原和/或微生物。本文提供了滿足ph、容量摩爾滲透壓濃度、離子平衡、無菌性、內毒素和/或致熱原水平的特定標準的耳用制劑。本文所述耳用組合物與eac的微環境相容并適合施用于人。舉非限制性的實例而言,當配制用于施用至耳的藥劑時,應當限制、減少或排除下列常用溶劑的使用:醇類、丙二醇和環己烷。因此,在一些實施方案中,本文公開的耳用組合物或制劑不含或基本不含醇類、丙二醇和環己烷。在一些實施方案中,本文公開的耳用組合物或制劑包含少于約50ppm的醇類、丙二醇和環己烷中的每一種。在一些實施方案中,本文公開的耳用組合物或制劑包含少于約25ppm的醇類、丙二醇和環己烷中的每一種。在一些實施方案中,本文公開的耳用組合物或制劑包含少于約20ppm的醇類、丙二醇和環己烷中的每一種。在一些實施方案中,本文公開的耳用組合物或制劑包含少于約10ppm的醇類、丙二醇和環己烷中的每一種。在一些實施方案中,本文公開的耳用組合物或制劑包含少于約5ppm的醇類、丙二醇和環己烷中的每一種。在一些實施方案中,本文公開的耳用組合物或制劑包含少于約1ppm的醇類、丙二醇和環己烷中的每一種。此外,耳用制劑要求特別低濃度的已知具有耳毒性的若干種可能常見的污染物。其他劑型,盡管設法限制由這些化合物引起的污染,但并不要求耳用制劑所要求的嚴格預防措施。例如,耳用制劑中應當不存在或幾乎不存在下列污染物:砷、鉛、汞和錫。因此,在一些實施方案中,本文公開的耳用組合物或制劑不含或基本不含砷、鉛、汞和錫。在一些實施方案中,本文公開的耳用組合物或制劑包含少于約50ppm的砷、鉛、汞和錫中的每一種。在一些實施方案中,本文公開的耳用組合物或制劑包含少于約25ppm的砷、鉛、汞和錫中的每一種。在一些實施方案中,本文公開的耳用組合物或制劑包含少于約20ppm的砷、鉛、汞和錫中的每一種。在一些實施方案中,本文公開的耳用組合物或制劑包含少于約10ppm的砷、鉛、汞和錫中的每一種。在一些實施方案中,本文公開的耳用組合物或制劑包含少于約5ppm的砷、鉛、汞和錫中的每一種。在一些實施方案中,本文公開的耳用組合物或制劑包含少于約1ppm的砷、鉛、汞和錫中的每一種。某些定義除非上下文另有明確規定,否則如本文所用的單數形式“一個”、“一種”和“該”包括復數指代物。在本申請中,除非另有特別說明,否則單數的使用包括復數。除非另有說明,否則如本文所用的“或”的使用意指“和/或”。此外,術語“包括(including)”及其他形式(例如,“包括(include)”、“包括(includes)”和“包括(included)”)的使用是非限制性的。如本文所用的范圍和量可表示為“約”特定的值或范圍。約還包括確切的量。因此,“約40mg”意指“約40mg”,并且還指“40mg”。通常,術語“約”包括預期在實驗誤差內的量。如本文所用的,關于制劑、組合物或成分的術語“耳可接受的”包括對正在治療的受試者的eac沒有持久的有害作用。如本文所用的“耳藥學上可接受的”是指諸如載體或稀釋劑的物質,其不會消除化合物針對eac的生物活性或性質,并且對eac的毒性降低或相對地降低,即,該物質在施用至個體時不會引起不希望的生物效應或不會以有害方式與包含它的組合物中的任何組分相互作用。如本文所用的,通過施用特定的化合物或藥物組合物而改善或減輕特定的耳部疾病、病癥或病況的癥狀是指歸因于施用該化合物或組合物或與施用該化合物或組合物相關的任何嚴重程度的降低、發作的延遲、進展的減緩或持續時間的縮短,無論是永久性的還是暫時的,持久的還是短暫的。“血漿濃度”是指本文提供的化合物在受試者血液的血漿組分中的濃度。“載體材料”是與耳用藥劑以及耳可接受的藥物制劑的釋放曲線特性相容的賦形劑。這類載體材料包括例如粘合劑、懸浮劑、崩解劑、填充劑、表面活性劑、增溶劑、穩定劑、潤滑劑、潤濕劑、稀釋劑等。“耳藥學上相容的載體材料”包括但不限于阿拉伯膠、明膠、膠態二氧化硅、甘油磷酸鈣、乳酸鈣、麥芽糊精、甘油、硅酸鎂、聚乙烯吡咯烷酮(pvp)、膽固醇、膽固醇酯、酪蛋白酸鈉、大豆卵磷脂、牛磺膽酸、磷脂酰膽堿、氯化鈉、磷酸三鈣、磷酸氫二鉀、纖維素和纖維素綴合物、糖、硬脂酰乳酸鈉、角叉菜膠、甘油單酯、甘油二酯、預膠化淀粉等。術語“稀釋劑”是指用來在遞送前稀釋耳用藥劑且與eac相容的化學化合物“分散劑”和/或“粘度調節劑”是控制耳用藥劑通過液體介質擴散和均質化的材料。擴散促進劑/分散劑的實例包括但不限于親水聚合物、電解質、60或80、peg、聚乙烯吡咯烷酮(pvp;商業上稱為)和基于碳水化合物的分散劑,例如羥丙基纖維素(例如,hpc、hpc-sl和hpc-l)、羥丙基甲基纖維素(例如,hpmck100、hpmck4m、hpmck15m和hpmck100m)、羧甲基纖維素鈉、甲基纖維素、羥乙基纖維素、羥丙基纖維素、羥丙基甲基纖維素鄰苯二甲酸酯、醋酸硬脂酸羥丙基甲基纖維素(hpmcas)、非結晶纖維素、硅酸鎂鋁、三乙醇胺、聚乙烯醇(pva)、乙烯基吡咯烷酮/乙酸乙烯酯共聚物(s630)、4-(1,1,3,3-四甲基丁基)-苯酚與環氧乙烷和甲醛的聚合物(也稱為泰洛沙泊)、泊洛沙姆(例如,聚氧乙烯-聚氧丙烯三嵌段共聚物);以及泊洛沙胺(poloxamine)(例如,tetronic也稱為poloxamine其為通過將環氧丙烷和環氧乙烷相繼添加至乙二胺而獲得的四官能嵌段共聚物(basfcorporation,parsippany,n.j.))、聚乙烯吡咯烷酮k12、聚乙烯吡咯烷酮k17、聚乙烯吡咯烷酮k25或聚乙烯吡咯烷酮k30、聚乙烯吡咯烷酮/乙酸乙烯酯共聚物(s630)、聚乙二醇(例如,該聚乙二醇具有約300到約6000,或約3350到約4000,或約7000到約5400的分子量)、羧甲基纖維素鈉、甲基纖維素、聚山梨酯-80、藻酸鈉、樹膠(例如,黃蓍膠和阿拉伯樹膠、瓜爾膠、黃原膠(包括黃原膠樹膠))、糖、纖維素材料(例如,羧甲基纖維素鈉、甲基纖維素、羧甲基纖維素鈉)、聚山梨酯-80、藻酸鈉、聚氧乙烯失水山梨醇單月桂酸酯、聚氧乙烯失水山梨醇單月桂酸酯、聚維酮、卡波姆、聚乙烯醇(pva)、藻酸鹽、殼聚糖及其組合。增塑劑如纖維素或三乙基纖維素也被用作分散劑。在本文公開的耳用藥劑的脂質體分散和自乳化分散中有用的分散劑為二肉豆蔻酰磷脂酰膽堿、源自蛋中的天然磷脂酰膽堿、源自蛋中的天然磷脂酰甘油、膽固醇和肉豆蔻酸異丙酯。“藥物吸收”或“吸收”是指耳用藥劑從局部給藥部位(僅舉例而言,eac)的移動過程。如本文所用的,術語“共同施用”等意在包括向單個患者施用耳用藥劑,并且意在包括通過相同或不同的給藥途徑或在相同或不同的時間施用耳用藥劑的治療方案。如本文所用的術語“有效量”或“治療有效量”是指正在施用的耳用藥劑的足量,預期該量會在某種程度上減輕正在治療的疾病或病況的一種或多種癥狀。例如,施用本文公開的耳用藥劑的結果是降低和/或緩和耵聹分泌過多的體征、癥狀或病因。例如,對于治療性應用來說,“有效量”是在沒有過度的不良副作用的情況下提供疾病癥狀的減少或改善所需要的耳用藥劑(包括本文公開的制劑)的量。術語“治療有效量”包括,例如,預防有效量。本文公開的至少一種耳用藥劑組合物的調節劑的“有效量”是有效實現期望的藥理作用或治療改善而沒有過度的不良副作用的量。應當理解,在一些實施方案中,由于所施用的化合物的代謝,受試者的年齡、體重、總體狀況,正在治療的病況,正在治療的病況的嚴重程度,和處方醫師的判斷的差異,使得“有效量”或“治療有效量”根據受試者的不同而不同。還應當理解,基于藥代動力學和藥效學考慮,在延長釋放給藥形式中的“有效量”可能不同于在立即釋放給藥形式中的“有效量”。術語“增強”是指提高耳用藥劑的所需作用的效能或延長其持續時間,或減輕由施用治療劑引起的任何不良癥狀。因此,關于增強本文公開的耳用藥劑(例如,去乙酰化酶(sirtuin)調節劑)的作用,術語“增強”是指在效能上提高或在持續時間上延長與本文公開的耳用藥劑聯合使用的其他治療劑的作用的能力。如本文所用的“增強有效量”是指耳用藥劑或其他治療劑的量,該量足以增強在所需系統中另一治療劑或耳用藥劑對目標耳結構的作用。當在患者中使用時,對于該應用有效的量將依賴于疾病、病癥或病況的嚴重程度和病程,既往治療,患者的健康狀況和對藥物的反應,以及治療醫師的判斷。術語“抑制”包括在需要治療的患者中預防、減緩或逆轉病況的發展,或者例如病況的進展。“平衡障礙”是指導致受試者感覺不穩或有運動感的病癥、疾病或病況。此定義中包括頭暈、眩暈、不平衡和暈厥前期。被歸類為平衡障礙的疾病包括但不限于聽力損失、頭暈、眩暈、耳鳴和類似病況。術語“藥劑盒”和“制品”作為同義詞使用。“藥效學”是指決定在eac的所需部位相對于藥物濃度所觀察到的生物反應的因素。“藥代動力學”是指決定在eac的所需部位達到和維持適當的藥物濃度的因素。在預防性應用中,向易患特定疾病、病癥或病況例如耵聹分泌過多或處于該特定疾病、病癥或病況的風險下的患者或患有已知具有耵聹分泌過多特征的疾病或癥狀(僅舉例而言,其包括聽力損失、頭暈、眩暈和耳鳴)的患者施用包含本文所述的耳用藥劑的組合物。這樣的量被定義為“預防有效量或劑量”。在該應用中,精確的量還取決于患者的健康狀況、體重等。術語“基本上低的降解產物”意指不到5重量%的活性劑是該活性劑的降解產物。在進一步的實施方案中,該術語意指不到3重量%的活性劑是該活性劑的降解產物。在更進一步的實施方案中,該術語意指不到2重量%的活性劑是該活性劑的降解產物。在進一步的實施方案中,該術語意指不到1重量%的活性劑是該活性劑的降解產物。在一些實施方案中,本文所述制劑中存在的任何單獨的雜質(例如,金屬雜質、活性劑的降解產物和/或賦形劑等)少于活性劑的5重量%、少于2重量%或少于1重量%。在一些實施方案中,該制劑在儲存期間不含沉淀物或在制備和儲存后不改變顏色。僅舉例而言,如本文所用的“基本上是微粒化粉末的形式”包括,超過70重量%的活性劑是該活性劑的微粒化顆粒的形式。在進一步的實施方案中,該術語意指超過80重量%的活性劑是該活性劑的微粒化顆粒的形式。在進一步的實施方案中,該術語意指超過90重量%的活性劑是該活性劑的微粒化顆粒的形式。術語“微粒化的”是指如本文所述的顆粒的大小,并且不通過其制備過程限制顆粒。換言之,“微粒化”顆粒應包括通過尺寸縮減獲得的顆粒和在不進行尺寸縮減的情況下獲得的顆粒。平均停留時間(mrt)是給藥后活性劑的分子在耳結構中停留的平均時間。“前藥”是指在體內轉化為母體藥物的耳用藥劑。在某些實施方案中,前藥通過一個或多個步驟或過程酶促代謝為生物學、藥學或治療活性形式的化合物。為了產生前藥,對藥學活性化合物進行修飾,使得該活性化合物將在體內給藥后再生。在一個實施方案中,該前藥被設計為改變藥物的代謝穩定性或轉運特性以遮蔽副作用或毒性,或改變藥物的其他特性或性質。在一些實施方案中,本文提供的化合物被衍生為合適的前藥。“增溶劑”是指有助于或增加本文公開的耳用藥劑的溶解度的耳可接受的化合物,如三醋精、檸檬酸三乙酯、油酸乙酯、辛酸乙酯、十二烷基硫酸鈉、多庫酯鈉、維生素etpgs、二甲基乙酰胺、n-甲基吡咯烷酮、n-羥乙基吡咯烷酮、聚乙烯吡咯烷酮、羥丙基甲基纖維素、羥丙基環糊精、乙醇、正丁醇、異丙醇、膽固醇、膽汁鹽、聚乙二醇200-600、四氫呋喃聚乙二醇醚(glycofurol)、卡必醇(transcutol)、丙二醇和二甲基異山梨醇等。“穩定劑”是指與eac的環境相容的化合物如任何抗氧化劑、緩沖液、酸、防腐劑等。穩定劑包括但不限于將達到以下任一項的試劑:(1)提高賦形劑與包括注射器或玻璃瓶在內的容器或遞送系統的相容性,(2)提高組合物的組分的穩定性,或(3)提高制劑的穩定性。如本文所用的“穩態”是,在施用于eac的藥物的量等于在一個給藥間隔內消除的藥物的量時,導致目標結構中藥物暴露的穩定或恒定水平。如本文所用的,術語“受試者”用于指動物,優選哺乳動物,包括人類或非人類。術語患者和受試者可互換使用。“表面活性劑”是指耳可接受的化合物,如十二烷基硫酸鈉、多庫酯鈉、吐溫60或80、三醋精、維生素etpgs、失水山梨醇單油酸酯、聚氧乙烯失水山梨醇單油酸酯、聚山梨酯、polaxomer、膽汁鹽、單硬脂酸甘油酯等。一些其他表面活性劑包括聚氧乙烯脂肪酸甘油酯和植物油,例如聚氧乙烯(60)氫化蓖麻油;以及聚氧乙烯烷基醚和烷基苯基醚,例如辛苯聚醇10、辛苯聚醇40。在一些實施方案中,包括表面活性劑以增強物理穩定性或用于其他目的。如本文所用的術語“治療”或“處理”包括緩解、減輕或改善疾病或病況例如耵聹分泌過多、癥狀,預防另外的癥狀,改善或預防癥狀的潛在代謝起因,抑制疾病或病況,例如,阻止疾病或病況的發展,減輕疾病或病況,引起疾病或病況的消退,減輕由疾病或病況引起的狀況,或預防性地和/或治療性地阻止疾病或病況的癥狀。耵聹耵聹或耳垢是在外耳道(eac)各處發現的蠟質分泌物。通常,耵聹分為兩種表型,即濕表型和干表型。濕表型具有蜜棕色至深棕色外觀并以高濃度的脂質和色素顆粒為特征。在一些實施方案中,濕耵聹含有約50%的脂質。它主要發現于非洲人群和歐洲人群中。干表型具有灰色至白色片狀外觀并以低濃度的脂質和色素顆粒為特征。在一些實施方案中,干耵聹含有約20%的脂質。它主要發現于亞洲人群和美洲原住民人群中。此外,這兩種類型的耵聹在遺傳學上是不同的,其中染色體16上atp結合盒c11(abcc11)基因中的單個遺傳變化決定所述類型。具體地,濕表型的等位基因在abcc11的編碼區的538處含有g,而對于干表型,則在538處存在a。耵聹潤滑敏感的耳道內層使其免于干燥并保護耳朵免受細菌、真菌、昆蟲和外來顆粒的影響。實際上,在若干項研究中,當耳感染的發生始終與耵聹的缺失相關時,證明了耵聹的抗微生物性能。在一些實施方案中,耵聹對細菌和真菌發揮了抗微生物性能。示例性細菌包括但不限于流感嗜血菌(haemophilusinfluenza)、金黃色葡萄球菌(staphylococcusaureus)、銅綠假單胞菌(pseudomonasaeruginosa)和大腸桿菌(escherichiacoli)。示例性真菌包括但不限于黑曲霉(aspergillusniger)和白假絲酵母(candidaalbicans)。耵聹是由超過40種不同物質組成的混合物。耵聹的主要組分為角蛋白,其占約60重量%。其他組分包括來自皮脂腺和耵聹腺的分泌物、來自外耳道(eac)內的毛發的顆粒狀(gradular)分泌物、脫落的上皮細胞、飽和及不飽和長鏈脂肪酸、醇、角鯊烯、羊毛甾醇和膽固醇。eac包括耳廓(頭側面可見的外耳廓或外耳的肉質部分),聽道(外聽道)和鼓膜的朝向外的部分(也稱為耳鼓膜)(圖2)。耵聹發現于eac的各處。皮脂腺和耵聹腺(或改變的頂泌腺)是位于eac中的兩種外分泌腺。皮脂腺是位于皮膚中的外分泌腺。它們分泌皮脂——一種粘性的油質或蠟質分泌物,其用于使皮膚和毛發潤滑和防水。存在兩種類型的皮脂腺,即與毛囊連接的皮脂腺和獨立存在的皮脂腺。當皮脂腺與毛囊連接時,沉積的皮脂被分泌到毛發的基部上,隨后經由毛干運送到皮膚的表面上。已知皮脂腺參與先天免疫并參與促炎和抗炎功能。已顯示皮脂腺的產物皮脂也發揮抗微生物性能。皮脂包含甘油三酯、蠟酯、角鯊烯、膽固醇酯、膽固醇和脂肪酸例如皮脂酸(sapienicacid)。皮脂還含有游離脂肪酸(ffa),其已顯示對廣泛范圍的革蘭氏陽性菌表現出體外抗細菌活性。另外的脂肪酸如單烯脂肪酸(例如油酸和棕櫚油酸)也顯示出發揮抗細菌活性。實際上,已表明棕櫚油酸的施用減小了野生型c57bl/6和突變flake小鼠的細菌性病變的大小。在單獨的研究中,油酸和棕櫚油酸顯示對金黃色葡萄球菌(s.aureus)和化膿性鏈球菌(s.pyogenes)為抑制性的。除脂肪酸外,皮脂腺還釋放抗微生物肽(amp)如人β-防御素(hbd),包括hbd-1、hbd-2和hbd-3以及ll-37——抗菌肽抗微生物肽18(hcap-18)的37個氨基酸長的c-末端部分,該抗微生物肽進一步促進了耵聹的抗微生物特性。耵聹腺或改變的頂泌汗腺是位于外聽道皮下的特化的汗腺。耵聹腺包括形成盤繞的管狀腺的內部分泌細胞層和外部肌上皮細胞層。該腺體排入更大的導管,其隨后排入位于外聽道中的護毛(guardhairs)內。耵聹腺分泌與皮脂相比粘性較低的分泌物。當產生機制與消除機制不平衡時,出現異常耵聹。耵聹的積累可導致不適到嚴重的健康并發癥。在某些實施方案中,本文公開了用于調節耵聹的產生的組合物、制劑、方法、用途、藥劑盒和遞送裝置。在一些實施方案中,本文公開了用于增加耵聹的產生的組合物、制劑、方法、用途、藥劑盒和遞送裝置。在一些實施方案中,本文公開了用于防止耵聹的積累或形成的組合物、制劑、方法、用途、藥劑盒和遞送裝置。在一些實施方案中,本文公開了用于去除耵聹的積累或形成的組合物、制劑、方法、用途、藥劑盒和遞送裝置。在一些實施方案中,本文公開了用于治療耵聹相關疾病或病況如耵聹分泌過多的組合物、制劑、方法、用途、藥劑盒和遞送裝置。耵聹分泌過多當耳垢楔入并阻塞eac和/或嵌塞在耳膜上時,發生耵聹分泌過多或耵聹嵌塞。耵聹分泌過多發生在約十分之一的兒童中,二十分之一的成年人中,以及超過三分之一的老年人和發育遲緩的人群中。在美國每年約有1200萬人尋求醫療護理。在一些實施方案中,耵聹的嵌塞是eac的完全阻塞。在一些實施方案中,耵聹的嵌塞是eac的部分阻塞。耵聹分泌過多的發生可歸因于eac中耵聹的積累,正常的擠壓如導致復合耵聹的助聽器,或通過使用棉簽或復合出耵聹的其他耳清潔裝置。與耵聹分泌過多相關的疾病或病況包括耳瘙癢、耳痛、耳鳴、眩暈、耳脹和聽力損失。耵聹分泌過多的治療包括灌洗、灌洗之外的手動去除、用于軟化耵聹的耵聹溶解劑或其組合。灌洗包括通過耳注射使用水或鹽水溶液。灌洗之外的手動去除包括使用刮匙、探頭、鉤、鉗子或抽吸裝置。耵聹溶解劑包括水基、油基和非水基非油基試劑。例如,水基耵聹溶解劑包括乙酸、(三乙醇胺多肽油酸酯縮合物)、(多庫酯鈉)、(多庫酯鈉)、(2-苯氧乙醇中混合的對羥基苯甲酸酯、多庫酯鈉)、(三乙醇胺多肽油酸酯縮合物、丙二醇和氯丁醇)、過氧化氫、碳酸氫鈉和無菌鹽水溶液。油基耵聹溶解劑包括杏仁油、花生油、橄欖油、礦物油/液體凡士林組合、(礦物油、角鯊烯和薄荷(spiramint)油的組合物)、(花生油、松節油、氯丁醇和對二氯苯的組合物)、(二辛基磺基琥珀酸鈉、玉米油)和(花生油、杏仁油和精餾樟腦油)。非水基非油基耵聹溶解劑包括(水楊酸膽堿、甘油)、(過氧化脲)、(過氧化脲和無水甘油的組合物)和(過氧化脲和無水甘油)。有時,耵聹分泌過多的治療導致顯著的并發癥。例如,諸如鼓膜穿孔、耳道撕裂、耳感染或聽力損失等并發癥以1000次耳灌洗中約1例的比率發生。另外的并發癥包括外耳炎、疼痛、頭暈和暈厥或昏厥。本發明認識到對于減少或改善與耵聹去除相關的并發癥的耳用組合物和治療方法的需要。在某些實施方案中,本文公開了用于治療耵聹分泌過多的組合物、制劑、方法、用途、藥劑盒和遞送裝置,其包括向有需要的個體施用包含一定量的耳用藥劑和水性耳可接受的凝膠的組合物。在某些實施方案中,本文進一步公開了用于治療耵聹分泌過多相關疾病或病況的組合物、制劑、方法、用途、藥劑盒和遞送裝置,其包括向有需要的個體施用包含一定量的耳用藥劑和水性耳可接受的凝膠的組合物。耵聹分泌過多相關疾病或病況與耵聹分泌過多相關的疾病或病況包括耳瘙癢、外耳炎、耳痛、耳鳴、眩暈、耳脹和聽力損失。本文公開了調節耵聹的產生從而減輕本文所述疾病或病況的組合物和方法。耳瘙癢耳瘙癢或耳道發癢是一種瘙癢或刺激性的感覺,其引起抓撓受影響區域的欲望或反射。在一些情況下,在受影響區域可能發生發紅、腫脹、酸痛和剝落。耳瘙癢是由多種物質引起的。在一些實施方案中,耳瘙癢由于耳內的原發性微生物感染或由于來自身體、隨后擴散至耳道中的繼發性感染而發生。在一些實施方案中,皮膚病況如濕疹或銀屑病導致耳道內的皮膚刺激。另外,外部刺激物如發膠、洗發劑、沐浴露或變應原如灰塵、寵物和花粉可導致耳瘙癢。在一些實施方案中,耳瘙癢作為較嚴重的并發癥如外耳炎的早期體征。外耳炎外耳炎是外聽道的炎癥。它伴有耳痛(耳疼痛或不適)和耳漏(在外聽道中流出或來自外聽道)。另外,如果炎癥引起的腫脹足以使外聽道閉塞,則還可能發生耳脹和聽力損失。外耳炎被分為兩種類型:慢性外耳炎和急性外耳炎(aoe)。aoe主要由細菌或真菌感染引起。然而,它還可能與非感染性全身或局部皮膚病過程如特應性皮炎、銀屑病、脂溢性皮炎、痤瘡和紅斑狼瘡相關。在一些實施方案中,已知銅綠假單胞菌和金黃色葡萄球菌是感染的主要細菌來源,而白假絲酵母和曲霉種是真菌對應物。一般而言,為輕度病例開出含有干燥劑和/或抗生素的局部溶液。然而,在重度病例中,可能需要全身性鎮痛藥如可待因和非甾體抗炎藥(nsaid)。耳痛耳痛(otalgia)也稱為耳朵痛(earache)或耳朵疼痛,其分為兩種類型,即原發性耳痛和牽涉性耳痛(referredotalgia)。原發性耳痛是源于耳朵內部的耳疼痛。牽涉性耳痛是源于耳朵外部的耳疼痛。雖然牽涉性耳痛的病因可能是復雜的,但幾種公知的病因包括牙齒病癥、鼻竇炎、頸部問題、扁桃體炎、咽炎以及來自迷走神經和舌咽神經的感覺分支。在一些情況下,牽涉性耳痛與頭頸部惡性腫瘤相關。耳脹耳脹或耳朵脹滿被描述為耳朵堵塞、塞滿或充滿的感覺。類似于耳痛,耳脹的病因因許多潛在的原因而多種多樣。通常,耳脹還可能伴有耳鳴、耳痛和聽力損傷。聽力損失聽力損失是聽力的部分或完全損傷。聽力損失可分為三種類型,即傳導性聽力損失、感音神經性聽力損失和混合性聽力損失。當聲音不能通過外聽道有效傳導至鼓膜或耳膜時,發生傳導性聽力損失。在一些實施方案中,傳導性聽力損失包括聲級或聽見微弱聲音的能力的降低。治療包括矯正性醫藥或手術程序。當存在對耳蝸(內耳)或對耳蝸至腦的神經通路的損傷時,發生感音神經性聽力損失。這種類型的聽力損失通常導致永久性聽力損失。混合性聽力損失是傳導性聽力損失和感音神經性聽力損失的組合,其中損傷沿著外耳和內耳區域發生。聽力損失的程度或嚴重性分為正常、輕微、輕度、中度、中等重度、重度至深度(pround)七組。此外,聽力損失可以基于頻率進行分層。例如,僅影響高音的聽力損失被稱為高頻聽力損失,而影響低音的聽力損失被稱為低頻聽力損失。在一些情況下,聽力損失既影響高頻又影響低頻。聽力損失常常伴有另外的病因和癥狀,如耵聹分泌過多、外耳炎、耳痛、耳鳴和眩暈。在一些實施方案中,已表明耵聹分泌過多可使聽敏度降低40-45db。這樣的損傷,尤其是在老年人群體中,可導致交流困難以及甚至無法進行身體移動。耳鳴耳鳴被定義為在不存在任何外部刺激的情況下有聲音的感知。它可連續地或偶發地發生于一只或兩只耳朵,并且最常被描述為振鈴聲。它最常用作其他疾病的診斷癥狀。存在兩種類型的耳鳴:客觀的和主觀的。前者是在體內產生的任何人均可聽見的聲音。后者是僅受影響個體可聽見的。研究估計,超過5000萬美國人經歷某種形式的耳鳴。在這5000萬人中,約1200萬人經歷重度耳鳴。存在幾種耳鳴治療方法。靜脈內施用的利多卡因減少或消除了約60-80%的患者中與耳鳴相關的噪音。選擇性神經遞質再攝取抑制劑,如去甲替林、舍曲林和帕羅西汀,也已經證明有抗耳鳴的功效。也開出苯二氮雜類來治療耳鳴。眩暈眩暈被描述為在身體靜止時旋轉或搖擺的感覺。存在兩種類型的眩暈。主觀眩暈是身體移動的錯誤感覺。客觀眩暈是對人的周圍物體在移動的感知。它常常伴有惡心、嘔吐和難以保持平衡。在一些實施方案中,外耳炎可引起眩暈。藥劑本文提供了調節耵聹的產生的組合物或制劑。本文還提供了調節本文公開的外分泌腺的功能或活性的組合物或制劑。本文進一步提供了改善或減輕耵聹分泌過多的組合物或制劑。此外,本文提供了改善或減輕耵聹分泌過多相關病癥的組合物或制劑,該病癥包括耳瘙癢、外耳炎、耳痛、耳鳴、眩暈、耳脹和聽力損失。耵聹、耵聹分泌過多和耵聹分泌過多相關病癥顯示出對本文公開的藥劑有反應的病因和癥狀。明確地包括本文未公開但對于改善或根除耵聹和耵聹分泌過多相關病癥有用的耳用藥劑,并且預期它們在提出的實施方案的范圍內。在一些實施方案中,耳用藥劑包括膽堿酯或氨基甲酸酯、植物生物堿、可逆性膽堿酯酶抑制劑、乙酰膽堿釋放促進劑、抗腎上腺素能藥、擬交感神經藥或其組合。在一些實施方案中,耳用藥劑為膽堿酯或氨基甲酸酯、植物生物堿、可逆性膽堿酯酶抑制劑、乙酰膽堿釋放促進劑、抗腎上腺素能藥、擬交感神經藥或其組合。在一些實施方案中,耳用藥劑為膽堿酯或氨基甲酸酯,優選乙酰膽堿或卡巴膽堿。在一些實施方案中,耳用藥劑為植物生物堿,優選毛果蕓香堿。在一些實施方案中,耳用藥劑為可逆性膽堿酯酶抑制劑,優選新斯的明或毒扁豆堿。在一些實施方案中,耳用藥劑為乙酰膽堿釋放促進劑,優選氟哌利多、利培酮或曲唑酮。在一些實施方案中,耳用藥劑為抗腎上腺素能藥,優選可樂定、普萘洛爾、阿替洛爾或哌唑嗪。在一些實施方案中,耳用藥劑為擬交感神經藥,優選去甲腎上腺素或多巴胺。在一些實施方案中,這樣的藥劑在本文一些實施方案中是有用的:其先前已經顯示在其他器官系統中在全身或局部施加過程中為毒性、有害或無效的,例如通過肝處理后形成的毒性代謝物,藥物在特定器官、組織或系統中的毒性,通過實現功效所需的高水平,通過不能經系統途徑釋放,或通過不良pk特性。因此,在本文公開的實施方案的范圍內涉及沒有或具有有限的全身釋放、系統毒性、不良pk特性或其組合的藥劑。本文公開的包含耳用藥劑的制劑任選地直接靶向需要治療的耳結構。在一些實施方案中,將本文公開的包含耳用藥劑的制劑涂敷至外聽道、鼓膜的外表面或其組合。這樣的實施方案還任選地包括藥物遞送裝置,其中該藥物遞送裝置通過使用注射器和/或針頭、泵、滴管、原位成形水凝膠材料或其任意組合遞送所公開的制劑。任選地,控制釋放耳用制劑包含耳保護劑,如抗氧化劑、α硫辛酸、鈣、磷霉素或鐵螯合劑,以抵消可能由特定的治療劑或賦形劑、稀釋劑或載體的使用而引起的潛在耳毒性作用。eac保護劑外分泌腺分泌的物質考慮將外分泌腺分泌物和外分泌腺分泌的物質與本文公開的制劑一起使用。因此,一些實施方案并入模擬天然耵聹組合物和/或發揮抗微生物性能的分泌物質的使用。外分泌腺被分為三類,即全泌腺、局泌(或外分泌)腺和頂泌腺。全泌腺將其分泌物積累至每個細胞的細胞質中并將全細胞釋放至導管中。皮脂腺是全泌腺的一個實例。頂泌腺包括汗腺,其中耵聹腺為一個實例。皮脂是由皮脂腺分泌的產物。在一些實施方案中,皮脂包含甘油三酯、蠟酯、角鯊烯、膽固醇酯、膽固醇和脂肪酸。在一些實施方案中,皮脂包含角鯊烯、羊毛甾醇和膽固醇。作為皮脂的一部分而分泌的角鯊烯充當包括羊毛甾醇和膽固醇在內的所有動物類固醇的前體。角鯊烯通過負責產生膽固醇和其他類異戊二烯的甲羥戊酸途徑產生。hmg-coa(或3-羥基-3-甲基戊二酰-輔酶a)還原酶是甲羥戊酸途徑中的速率控制酶。在一些實施方案中,外分泌腺分泌的物質包含甘油三酯、蠟酯、角鯊烯、膽固醇酯、膽固醇和脂肪酸中的至少一種。在一些實施方案中,外分泌腺分泌的物質包含角鯊烯、羊毛甾醇和膽固醇中的至少一種。在一些實施方案中,耵聹的組分包括外分泌腺分泌的物質。在一些實施方案中,耵聹包含甘油三酯、蠟酯、角鯊烯、膽固醇酯、膽固醇和脂肪酸中的至少一種。在一些實施方案中,耵聹包含角鯊烯、羊毛甾醇和膽固醇中的至少一種。在一些實施方案中,本文公開的耳用組合物進一步包含另外的活性劑。在一些實施方案中,該另外的活性劑包含甘油三酯、蠟酯、角鯊烯、膽固醇酯、膽固醇和脂肪酸中的至少一種。在一些實施方案中,該另外的活性劑包含角鯊烯、羊毛甾醇和膽固醇中的至少一種。在一些實施方案中,所述耳用組合物進一步包含甘油三酯、蠟酯、角鯊烯、膽固醇酯、膽固醇和脂肪酸中的至少一種。在一些實施方案中,所述耳用組合物進一步包含角鯊烯、羊毛甾醇和膽固醇中的至少一種。在一些實施方案中,所述耳用組合物進一步包含角鯊烯、羊毛甾醇和膽固醇。在一些實施方案中,角鯊烯的重量百分比為約1%至約20%。在一些實施方案中,角鯊烯的重量百分比為約2%至約15%。在一些實施方案中,角鯊烯的重量百分比為約3%至約10%。在一些實施方案中,角鯊烯的重量百分比為約5%至約8%。在一些實施方案中,角鯊烯的重量百分比為約1%、約2%、約3%、約4%、約5%、約6%、約7%、約8%、約9%、約10%、約11%、約12%、約13%、約14%、約15%、約16%、約17%、約18%、約19%或約20%。在一些實施方案中,羊毛甾醇的重量百分比為約1%至約20%。在一些實施方案中,羊毛甾醇的重量百分比為約2%至約15%。在一些實施方案中,羊毛甾醇的重量百分比為約3%至約10%。在一些實施方案中,羊毛甾醇的重量百分比為約5%至約8%。在一些實施方案中,羊毛甾醇的重量百分比為約1%、約2%、約3%、約4%、約5%、約6%、約7%、約8%、約9%、約10%、約11%、約12%、約13%、約14%、約15%、約16%、約17%、約18%、約19%或約20%。在一些實施方案中,膽固醇的重量百分比為約1%至約20%。在一些實施方案中,膽固醇的重量百分比為約2%至約15%。在一些實施方案中,膽固醇的重量百分比為約3%至約10%。在一些實施方案中,膽固醇的重量百分比為約5%至約8%。在一些實施方案中,膽固醇的重量百分比為約1%、約2%、約3%、約4%、約5%、約6%、約7%、約8%、約9%、約10%、約11%、約12%、約13%、約14%、約15%、約16%、約17%、約18%、約19%或約20%。抗微生物劑在一些實施方案中,耵聹包含發揮抗微生物性能的物質。在一些實施方案中,這些物質包括脂質、蛋白質和抗微生物肽(amp)。在一些實施方案中,脂質包括脂肪酸、膽固醇、蠟、甾醇、甘油單酯、甘油二酯、甘油三酯和磷脂。在一些實施方案中,脂肪酸包括游離脂肪酸(ffa)和不飽和脂肪酸如油酸和棕櫚油酸。在一些實施方案中,amp包括hbd-1、hbd-2、hbd-3和ll-37。在一些實施方案中,本文公開的耳用組合物進一步包含抗微生物劑。在一些實施方案中,該抗微生物劑包含ffa、油酸、棕櫚油酸和amp中的至少一種。在一些實施方案中,該抗微生物劑包含ffa、油酸、棕櫚油酸、hbd-1、hbd-2、hbd-3和ll-37中的至少一種。在一些實施方案中,本文公開的耳用組合物進一步包含ffa、油酸、棕櫚油酸和amp中的至少一種。在一些實施方案中,本文公開的耳用組合物進一步包含ffa、油酸、棕櫚油酸、hbd-1、hbd-2、hbd-3和ll-37中的至少一種。在一些實施方案中,抗微生物劑的重量百分比為約1%至約20%。在一些實施方案中,抗微生物劑的重量百分比為約2%至約15%。在一些實施方案中,抗微生物劑的重量百分比為約3%至約10%。在一些實施方案中,抗微生物劑的重量百分比為約5%至約8%。在一些實施方案中,抗微生物劑的重量百分比為約1%、約2%、約3%、約4%、約5%、約6%、約7%、約8%、約9%、約10%、約11%、約12%、約13%、約14%、約15%、約16%、約17%、約18%、約19%或約20%。聯合治療皮質類固醇考慮與本文公開的耳用制劑聯合使用的是減少或改善由自身免疫病和/或炎癥病癥引起的癥狀或作用的皮質類固醇藥劑。這樣的類固醇包括潑尼松龍、地塞米松、倍氯米松、21-乙酰氧基孕烯醇酮、阿氯米松、阿爾孕酮、安西奈德、倍氯米松、倍他米松、布地奈德、氯潑尼松、氯倍他索、氯倍他松、氯可托龍、氯潑尼醇、皮質酮、可的松、可的伐唑、地夫可特、地奈德、去羥米松、地塞米松、磷酸地塞米松、二氟拉松、二氟可龍、二氟潑尼酯、甘草次酸、氟扎可特、氟氯奈德、氟米松、氟尼縮松、氟輕松(fluocinoloneacetonide)、醋酸氟輕松(fluocinonide)、氟可丁丁酯(luocortinbutyl)、氟可龍、氟米龍、醋酸甲氟龍、醋酸氟潑尼定、氟潑尼龍、氟氫縮松、丙酸氟替卡松、福莫可他、哈西奈德、丙酸鹵倍他索、鹵米松、醋酸鹵潑尼松、氫可他酯、氫化可的松、依碳酸氯替潑諾(loteprednoletabonate)、馬潑尼酮、甲羥松、甲潑尼松、甲潑尼龍、糠酸莫米松、帕拉米松、潑尼卡酯、潑尼松龍、25-二乙基氨基-乙酸潑尼松龍、潑尼松龍磷酸鈉、強的松、潑尼松龍戊酸酯(prednival)、潑尼立定、利美索龍、替可的松、曲安西龍、曲安奈德、苯曲安奈德、己曲安奈德及其組合。止吐劑/中樞神經系統藥劑止吐劑任選與本文公開的耳用藥劑制劑聯合使用。止吐劑包括抗組胺劑和中樞神經藥劑,其包括抗精神病劑、巴比妥類藥物、苯二氮雜類和吩噻嗪類。其他止吐劑包括5-羥色胺受體拮抗劑,其包括多拉司瓊、格拉司瓊、昂丹司瓊、托烷司瓊、帕洛諾司瓊及其組合;多巴胺拮抗劑,其包括多潘立酮、氟哌利多(properidol)、氟哌啶醇、氯丙嗪、異丙嗪、丙氯拉嗪及其組合;大麻酚類(cannabinoids),其包括屈大麻酚、大麻隆、大麻酚(sativex)及其組合;抗膽堿能類藥物,其包括東莨菪堿;以及類固醇類,其包括地塞米松;曲美芐胺(trimethobenzamine)、愈吐寧錠(emetrol)、異丙酚、蠅蕈醇及其組合。任選地,中樞神經系統藥劑和巴比妥類藥物用于治療伴隨耳部病癥的惡心和嘔吐癥狀。當使用時,選擇合適的巴比妥類藥物和/或中樞神經系統藥劑來減輕或改善特定的癥狀,而沒有包括耳毒性在內的可能的副作用。此外,如上所討論的,將藥物靶向eac減少了由全身性施用這些藥物導致的可能的副作用和毒性。用作中樞神經系統抑制劑的巴比妥類藥物包括了阿洛巴比妥、苯烯比妥(alphenal)、異戊巴比妥、阿普比妥、巴比沙隆(barnexaclone)、巴比妥、溴烯比妥、仲丁巴比妥、布他比妥、丁溴比妥、丁巴比妥、corvalol、巴豆基巴比妥(crotylbarbital)、環己巴比妥、烯丙環戊烯巴比妥(cyclopal)、依沙比妥、非巴氨酯、庚巴比妥、己巴比妥、海索比妥、美沙比妥、美索比妥、甲基苯巴比妥、那可比妥、尼阿比妥、戊巴比妥、苯巴比妥、普里米酮、普羅比妥、丙溴比妥、普昔巴比妥(proxibarbital)、雙環辛巴比妥(reposal)、司可巴比妥、溴烯丙另戊巴比妥、硫噴妥鈉、他布比妥、硫烯比妥、硫戊巴比妥、硫巴比妥、仲丁硫巴比妥鈉、圖伊諾爾(tuinal)、哇洛凡(valofane)、戊烯比妥、乙烯比妥及其組合。任選與本文公開的耳用藥劑制劑聯合使用的其他中樞神經系統藥劑包括苯二氮雜類或吩噻嗪類。有用的苯二氮雜類包括但不限于地西泮、勞拉西泮、奧沙西泮、普拉西泮、阿普唑侖、溴西泮、氯氮(chlordiazepoxide)、氯硝西泮、氯拉酸(clorazepate)、溴替唑侖、艾司唑侖、氟硝西泮、氟西泮、氯普唑侖、氯甲西泮、咪達唑侖、硝甲西泮、硝西泮、四氫西泮(ternazepam)、三唑侖及其組合。吩噻嗪的實例包括丙氯拉嗪、氯丙嗪、丙嗪、三氟丙嗪、左美丙嗪(levopromazine)、甲氧異丙嗪(methotrimepramazine)、美索達嗪、硫利達嗪(thiroridazine)、氟奮乃靜、奮乃靜、氟哌噻噸、三氟拉嗪及其組合。抗組胺劑或組胺拮抗劑用于抑制組胺的釋放或作用。靶向h1受體的抗組胺劑可用于減輕或減少與耳部病癥相關的惡心和嘔吐癥狀。這樣的抗組胺劑包括但不限于美克洛嗪、苯海拉明、氯雷他定和喹硫平。其他的抗組胺劑包括美吡拉敏、哌羅克生、安他唑啉、卡比沙明、多西拉敏、氯馬斯汀、茶苯海明、非尼拉敏、撲爾敏、氯苯那敏(chlorpheniramine)、右氯苯那敏、溴苯那敏、曲普利啶、賽克利嗪、氯環嗪、羥嗪、異丙嗪、阿利馬嗪、異丁嗪、賽庚啶、阿扎他啶、酮替芬、奧沙米特及其組合。活性劑的濃度在一些實施方案中,按組合物的重量計,本文所述的組合物具有活性藥物成分濃度為約0.01%至約90%、約0.01%至約80%、約0.1%至約70%、約0.1%至約30%、約0.1%至約50%、約0.1%至約40%、約0.1%至約30%、約0.1%至約20%、約0.1%至約10%或約0.1%至約5%的活性成分或其藥學上可接受的前藥或鹽。在一些實施方案中,按組合物的重量計,本文所述的組合物具有活性藥劑的濃度為約1%至約50%、約5%至約50%、約10%至約40%或約10%至約30%的活性成分或其藥學上可接受的前藥或鹽。在一些實施方案中,按制劑的重量計,本文所述的制劑包含約70重量%的耳用藥劑或其藥學上可接受的前藥或鹽。在一些實施方案中,按制劑的重量計,本文所述的制劑包含約60重量%的耳用藥劑或其藥學上可接受的前藥或鹽。在一些實施方案中,按制劑的重量計,本文所述的制劑包含約50重量%的耳用藥劑或其藥學上可接受的前藥或鹽。在一些實施方案中,按制劑的重量計,本文所述的制劑包含約40重量%的耳用藥劑或其藥學上可接受的前藥或鹽。在一些實施方案中,按制劑的重量計,本文所述的制劑包含約30重量%的耳用藥劑或其藥學上可接受的前藥或鹽。在一些實施方案中,按制劑的重量計,本文所述的制劑包含約25重量%的耳用藥劑或其藥學上可接受的前藥或鹽。在一些實施方案中,按制劑的重量計,本文所述的制劑包含約20重量%的耳用藥劑或其藥學上可接受的前藥或鹽。在一些實施方案中,按制劑的重量計,本文所述的制劑包含約19重量%的耳用藥劑或其藥學上可接受的前藥或鹽。在一些實施方案中,按制劑的重量計,本文所述的制劑包含約18重量%的耳用藥劑或其藥學上可接受的前藥或鹽。在一些實施方案中,按制劑的重量計,本文所述的制劑包含約17重量%的耳用藥劑或其藥學上可接受的前藥或鹽。在一些實施方案中,按制劑的重量計,本文所述的制劑包含約16重量%的耳用藥劑或其藥學上可接受的前藥或鹽。在一些實施方案中,按制劑的重量計,本文所述的制劑包含約15重量%的耳用藥劑或其藥學上可接受的前藥或鹽。在一些實施方案中,按制劑的重量計,本文所述的制劑包含約14重量%的耳用藥劑或其藥學上可接受的前藥或鹽。在一些實施方案中,按制劑的重量計,本文所述的制劑包含約13重量%的耳用藥劑或其藥學上可接受的前藥或鹽。在一些實施方案中,按制劑的重量計,本文所述的制劑包含約12重量%的耳用藥劑或其藥學上可接受的前藥或鹽。在一些實施方案中,按制劑的重量計,本文所述的制劑包含約11重量%的耳用藥劑或其藥學上可接受的前藥或鹽。在一些實施方案中,按制劑的重量計,本文所述的制劑包含約10重量%的耳用藥劑或其藥學上可接受的前藥或鹽。在一些實施方案中,按制劑的重量計,本文所述的制劑包含約9重量%的耳用藥劑或其藥學上可接受的前藥或鹽。在一些實施方案中,按制劑的重量計,本文所述的制劑包含約8重量%的耳用藥劑或其藥學上可接受的前藥或鹽。在一些實施方案中,按制劑的重量計,本文所述的制劑包含約7重量%的耳用藥劑或其藥學上可接受的前藥或鹽。在一些實施方案中,按制劑的重量計,本文所述的制劑包含約6重量%的耳用藥劑或其藥學上可接受的前藥或鹽。在一些實施方案中,按制劑的重量計,本文所述的制劑包含約5重量%的耳用藥劑或其藥學上可接受的前藥或鹽。在一些實施方案中,按制劑的重量計,本文所述的制劑包含約4重量%的耳用藥劑或其藥學上可接受的前藥或鹽。在一些實施方案中,按制劑的重量計,本文所述的制劑包含約3重量%的耳用藥劑或其藥學上可接受的前藥或鹽。在一些實施方案中,按制劑的重量計,本文所述的制劑包含約2.5重量%的耳用藥劑或其藥學上可接受的前藥或鹽。在一些實施方案中,按制劑的重量計,本文所述的制劑包含約2重量%的耳用藥劑或其藥學上可接受的前藥或鹽。在一些實施方案中,按制劑的重量計,本文所述的制劑包含約1.5重量%的耳用藥劑或其藥學上可接受的前藥或鹽。在一些實施方案中,按制劑的重量計,本文所述的制劑包含約1重量%的耳用藥劑或其藥學上可接受的前藥或鹽。在一些實施方案中,按制劑的重量計,本文所述的制劑包含約0.5重量%的耳用藥劑或其藥學上可接受的前藥或鹽。在一些實施方案中,按制劑的重量計,本文所述的制劑包含約0.1重量%的耳用藥劑或其藥學上可接受的前藥或鹽。在一些實施方案中,按制劑的重量計,本文所述的制劑包含約0.01重量%的耳用藥劑或其藥學上可接受的前藥或鹽。在一些實施方案中,按制劑的體積計,本文所述的制劑具有活性藥物成分或其藥學上可接受的前藥或鹽的濃度為約0.1至約70mg/ml、約0.5mg/ml至約70mg/ml、約0.5mg/ml至約50mg/ml、約0.5mg/ml至約20mg/ml、約1mg至約70mg/ml、約1mg至約50mg/ml、約1mg/ml至約20mg/ml、約1mg/ml至約10mg/ml或約1mg/ml至約5mg/ml的活性劑或其藥學上可接受的前藥或鹽。一般滅菌方法本文提供了調節耵聹的產生和/或調節本文公開的外分泌腺的功能或活性的耳用組合物。本文還提供了改善或減輕耵聹分泌過多和耵聹分泌過多相關病癥的耳用組合物。本文進一步提供了包括施用本文公開的耳用組合物的方法。在一些實施方案中,將組合物滅菌。在本文公開的實施方案內包括對本文公開的用于人類的藥物組合物進行滅菌的手段和過程。目的在于提供相對不含引起感染的微生物的安全的藥物產品。美國食品和藥品管理局已在可從http://www.fda.gov/cder/guidance/5882fnl.htm獲得的出版物“guidanceforindustry:steriledrugproductsproducedbyasepticprocessing”(通過引用全文并入本文)中提供了監管指導。如本文所用的,滅菌意指一種用于消滅或去除存在于產品或包裝中的微生物的過程。使用可用于對物體和組合物進行滅菌的任何合適的方法。用于使微生物失活的可用方法包括但不限于施加極熱、致死性化學品或γ輻射。在一些實施方案中是用于制備耳用治療制劑的過程,該過程包括使該制劑經歷選自熱滅菌、化學滅菌、輻射滅菌或過濾除菌的滅菌方法。所用的方法主要取決于待滅菌的裝置或組合物的性質。許多滅菌方法的詳細描述在由lippincott、williams和wilkins出版的remington:thescienceandpracticeofpharmacy的第40章中給出,并且該文獻通過引用與本發明主題相關的內容并入本文。熱滅菌許多方法可用于通過施加極熱進行滅菌。一種方法是通過使用飽和蒸汽高壓滅菌器。在該方法中,使溫度為至少121℃的飽和蒸汽與待滅菌的物體接觸。在待滅菌的物體的情況下,熱量直接轉移至微生物,或者通過加熱待滅菌的水溶液本體將熱量間接地轉移到微生物。這種方法被廣泛采用,因為它使得滅菌過程具有靈活性、安全性和經濟性。干熱滅菌是一種用于在升高的溫度下殺死微生物并進行去熱原的方法。該過程在適合于將hepa過濾的無微生物空氣加熱到至少130-180℃的溫度用于滅菌過程且加熱到至少230-250℃的溫度用于去熱原過程的設備中發生。用來重建濃縮制劑或粉末制劑的水也由高壓滅菌器滅菌。在一些實施方案中,本文所述的制劑包含微粒化的耳用藥劑(例如,微粒化的力諾吡啶粉末),該耳用藥劑經過干熱滅菌,例如,在130-140℃的內部粉末溫度下加熱約7-11小時,或在150-180℃的內部溫度下加熱1-2小時。化學滅菌化學滅菌方法是用于不能承受熱滅菌極端條件的產品的替代方法。在該方法中,多種具有殺菌性質的氣體和蒸汽,如環氧乙烷、二氧化氯、甲醛或臭氧,用作凋亡劑。例如,環氧乙烷的殺菌活性來源于其充當反應性烷化劑的能力。因此,該滅菌過程需要環氧乙烷蒸汽與待滅菌的產品直接接觸。輻射滅菌輻射滅菌的一個優點是能夠對許多種類型的產品進行滅菌而不會發生熱降解或其他損害。常用的輻射為β輻射,或者可替代地,為來自60co源的γ輻射。γ輻射的穿透能力允許其用于對許多產品類型進行滅菌,包括溶液、組合物和非均相混合物。輻射的殺菌作用由γ輻射與生物大分子的相互作用引起。該相互作用產生帶電荷的物質和自由基。隨后的化學反應,如重排和交聯過程,導致這些生物大分子的正常功能喪失。任選地,本文所述的制劑還采用β輻射進行滅菌。過濾過濾除菌是一種用于從溶液中去除微生物但不破壞微生物的方法。膜過濾器用于過濾熱敏性溶液。此類過濾器是混合纖維素酯(mce)、聚偏氟乙烯(pvf;也稱為pvdf)或聚四氟乙烯(ptfe)的堅韌、均質的薄聚合物,且具有0.1到0.22μm范圍的孔徑。任選地,采用不同的濾膜過濾不同特征的溶液。例如,pvf和ptfe膜非常適于過濾有機溶劑,而水溶液通過pvf或mce膜進行過濾。過濾器設備可用于在許多規模下使用,其范圍從附接至注射器的單使用點一次性過濾器直到在制造廠中使用的商業規模的過濾器。膜過濾器通過高壓滅菌器或化學滅菌進行滅菌。膜過濾系統的驗證依照標準化的方案(microbiologicalevaluationoffiltersforsterilizingliquids,vol4,no.3,washington,d.c:healthindustrymanufacturersassociation,1981)進行,并且包括用已知量(約107/cm2)的極小微生物(如缺陷短波單胞菌(brevundimonasdiminuta)(atcc19146))攻擊膜過濾器。藥物組合物任選地通過穿過膜過濾器進行滅菌。包含納米顆粒(美國專利號6,139,870)或多層囊泡(richard等人,internationaljournalofpharmaceutics(2006),312(1-2):144-50)的制劑適合通過經由0.22μm過濾器過濾來滅菌,而不破壞其組織化的結構。在一些實施方案中,本文公開的方法包括借助于過濾除菌對制劑(或其組分)進行滅菌。在另一個實施方案中,耳可接受的耳用制劑包含顆粒,其中該顆粒制劑適于過濾除菌。在進一步的實施方案中,所述顆粒制劑包含大小小于300nm、大小小于200nm、大小小于100nm的顆粒。在另一個實施方案中,耳可接受的制劑包括顆粒制劑,其中通過前體組分溶液的無菌過濾來確保該顆粒的無菌性。在另一個實施方案中,耳可接受的制劑包括顆粒制劑,其中通過低溫無菌過濾來確保該顆粒制劑的無菌性。在進一步的實施方案中,低溫無菌過濾在0到30℃、0到20℃、0到10℃、10到20℃或20到30℃的溫度下進行。在另一個實施方案中是一種用于制備耳可接受的顆粒制劑的過程,其包括:在低溫下通過除菌過濾器過濾含有顆粒制劑的水溶液;將無菌溶液凍干;以及在施用前用無菌水重建該顆粒制劑。在一些實施方案中,將本文所述的制劑制備為在含有微粒化的活性藥物成分的單個小瓶制劑中的懸浮液。通過將無菌的泊洛沙姆溶液與無菌的微粒化活性成分(例如,膽堿酯或氨基甲酸酯、植物生物堿、可逆性膽堿酯酶抑制劑、乙酰膽堿釋放促進劑、抗腎上腺素能藥、擬交感神經藥)無菌混合并將該制劑轉移至無菌的藥物容器中來制備單個小瓶制劑。在一些實施方案中,將含有作為懸浮液的本文所述制劑的單個小瓶在分配和/或施用之前重懸。在特定的實施方案中,過濾和/或填充程序在比本文所述的制劑的膠凝溫度(t膠凝)低約5℃的溫度下且在低于理論值100cp的粘度下進行,以允許采用蠕動泵在合適的時間內過濾。在另一個實施方案中,耳可接受的耳用制劑包括納米顆粒制劑,其中該納米顆粒制劑適于過濾除菌。在進一步的實施方案中,該納米顆粒制劑包含大小小于300nm、大小小于200nm或大小小于100nm的納米顆粒。在另一個實施方案中,耳可接受的制劑包括熱可逆性凝膠制劑,其中通過低溫無菌過濾來確保該凝膠制劑的無菌性。在進一步的實施方案中,該低溫無菌過濾在0到30℃、或0到20℃、或0到10℃、或10到20℃或20到30℃的溫度下進行。在另一個實施方案中是一種用于制備耳可接受的熱可逆性凝膠制劑的過程,其包括:在低溫下通過除菌過濾器過濾含有熱可逆性凝膠組分的水溶液;將無菌溶液凍干;以及在施用前用無菌水重建該熱可逆性凝膠制劑。在某些實施方案中,將活性成分溶解于合適的媒介物(例如緩沖液)中并單獨滅菌(例如通過熱處理、過濾、γ或電子束輻射)。在一些情況下,活性成分在干燥狀態下單獨滅菌。在一些情況下,活性成分作為懸浮液或作為膠態懸浮液滅菌。在單獨的步驟中,通過合適的方法(例如,對冷卻的賦形劑混合物的過濾和/或輻射)對剩余的賦形劑(例如,在耳用制劑中存在的流體凝膠組分)進行滅菌;然后將單獨滅菌的兩種溶液無菌混合以提供最終的耳用制劑。在一些情況下,最終的無菌混合在臨施用本文所述的制劑之前進行。在一些情況下,常規使用的滅菌方法(例如,熱處理(例如,在高壓滅菌器中)、γ輻射、過濾)導致制劑中的聚合物組分(例如,熱固性或膠凝性)和/或活性劑的不可逆降解。在一些情況下,如果制劑包含在過濾過程中膠凝的觸變性聚合物,則通過經由膜(例如,0.2μm膜)過濾對耳用制劑滅菌是不可能的。因此,本文提供了耳用制劑的滅菌方法,其防止聚合物組分(例如,熱固性和/或膠凝性組分)和/或活性劑在滅菌過程中的降解。在一些實施方案中,通過在制劑中使用緩沖組分的特定ph范圍和膠凝劑的特定比例來減少或消除活性劑(例如,本文所述的任何耳用治療劑)的降解。在一些實施方案中,選擇合適的膠凝劑和/或熱固性聚合物使得本文所述的制劑能夠通過過濾來滅菌。在一些實施方案中,對制劑使用合適的熱固性聚合物和合適的共聚物(例如,膠凝劑)與特定ph范圍的組合,使得能夠對所述制劑進行高溫滅菌,而治療劑或聚合物賦形劑基本不降解。本文提供的滅菌方法的一個優點是:在某些情況下,制劑經受通過高壓滅菌法的最終滅菌而活性劑和/或賦形劑和/或聚合物組分在滅菌步驟中沒有任何損失,且使得基本不含微生物和/或致熱原。微生物本文提供了調節耵聹的產生和/或調節本文公開的外分泌腺的功能或活性的耳可接受的組合物。本文還提供了改善或減輕耵聹分泌過多和耵聹分泌過多相關病癥的耳用組合物。本文進一步提供了包括施用本文公開的耳用組合物的方法。在一些實施方案中,該組合物基本不含微生物。可接受的生物負荷或無菌性水平基于限定治療上可接受的組合物的適用標準,包括但不限于美國藥典第<1111>章及以后章節。例如,可接受的無菌性(例如,生物負荷)水平包括約10個菌落形成單位(cfu)/克制劑、約50cfu/克制劑、約100cfu/克制劑、約500cfu/克制劑或約1000cfu/克制劑。在一些實施方案中,制劑的可接受的生物負荷水平或無菌性包括低于10cfu/ml、低于50cfu/ml、低于500cfu/ml或低于1000cfu/ml的微生物體。此外,可接受的生物負荷水平或無菌性包括指定的有害微生物體的排除。舉例而言,指定的有害微生物體包括但不限于大腸桿菌(e.coli)、沙門氏菌(salmonellasp.)、銅綠假單胞菌(p.aeruginosa)和/或其他特定的微生物體。耳可接受的耳用制劑的無菌性依照美國藥典第<61>、<62>和<71>章的無菌性保證程序來確認。無菌性保證質量控制、質量保證和驗證過程的關鍵部分是無菌性測試方法。僅舉例而言,無菌性測試通過兩種方法進行。第一種是直接接種,其中將待測組合物的樣品添加至生長培養基中并溫育最長21天的一段時間。生長培養基的濁度指示污染。該方法的缺點包括本體材料的取樣量小,從而降低了靈敏度,以及基于目視觀察來檢測微生物生長。一種替代方法是膜過濾無菌性測試。在該方法中,使一定體積的產品穿過較小的膜濾紙。然后將該濾紙置于培養基中以促進微生物的生長。由于對整個本體產品進行取樣,因此該方法具有靈敏度較高的優點。任選地使用可商購的milliporesteritest無菌性測試系統通過膜過濾無菌性測試進行測定。對于乳膏或軟膏的過濾測試,采用steritest過濾系統no.tlhvsl210。對于乳液或粘性產品的過濾測試,采用steritest過濾系統no.tlarem210或tdarem210。對于預填充注射器的過濾測試,采用steritest過濾系統no.tthasy210。對于分配為氣霧劑或泡沫的材料的過濾測試,采用steritest過濾系統no.tthva210。對于在安瓿或小瓶中的可溶性粉末的過濾測試,采用steritest過濾系統no.tthada210或tthadv210。對大腸桿菌和沙門氏菌的測試包括使用乳糖肉湯在30-35℃下溫育24-72小時,在macconkey和/或emb瓊脂中溫育18-24小時,和/或使用rappaport培養基。用于銅綠假單胞菌檢測的測試包括使用nac瓊脂。美國藥典第<62>章進一步列舉了針對指定的有害微生物的測試程序。在某些實施方案中,本文所述的任何控制釋放制劑具有每克制劑少于約60個菌落形成單位(cfu)、少于約50個菌落形成單位、少于約40個菌落形成單位或少于約30個菌落形成單位的微生物體。在某些實施方案中,將本文所述的耳用制劑配制為與eac等滲。內毒素本文提供了調節耵聹的產生和/或調節本文公開的外分泌腺的功能或活性的耳用組合物。本文還提供了改善或減輕耵聹分泌過多和耵聹分泌過多相關病癥的耳用組合物。本文進一步提供了包括施用本文公開的耳用組合物的方法。在一些實施方案中,該組合物基本不含內毒素。滅菌過程的另一方面是去除由微生物殺滅產生的副產物(下文中稱為“產物”)。去熱原過程將致熱原從樣品中去除。致熱原是誘導免疫應答的內毒素或外毒素。內毒素的一個實例是在革蘭氏陰性菌的細胞壁中發現的脂多糖(lps)分子。盡管滅菌程序(如高壓滅菌法或環氧乙烷處理)殺死細菌,但lps殘留物誘導促炎免疫應答,如膿毒性休克。由于內毒素的分子大小可能相差很大,因此內毒素的存在以“內毒素單位”(eu)表示。一個eu等同于100皮克的大腸桿菌lps。人可對低至5eu/kg體重產生應答。生物負荷(例如,微生物限度)和/或無菌性(例如,內毒素水平)以本領域公認的任意單位表示。在某些實施方案中,本文所述的耳用組合物含有與傳統可接受的內毒素水平(例如,5eu/kg受試者體重)相比更低的內毒素水平(例如,<4eu/kg受試者體重)。在一些實施方案中,耳可接受的耳用制劑具有低于約5eu/kg受試者體重。在其他實施方案中,耳可接受的耳用制劑具有低于約4eu/kg受試者體重。在另外的實施方案中,耳可接受的耳用制劑具有低于約3eu/kg受試者體重。在另外的實施方案中,耳可接受的耳用制劑具有低于約2eu/kg受試者體重。在一些實施方案中,耳可接受的耳用制劑具有低于約5eu/kg制劑。在其他實施方案中,耳可接受的耳用制劑具有低于約4eu/kg制劑。在另外的實施方案中,耳可接受的耳用制劑具有低于約3eu/kg制劑。在一些實施方案中,耳可接受的耳用制劑具有低于約5eu/kg產物。在其他實施方案中,耳可接受的耳用制劑具有低于約1eu/kg產物。在另外的實施方案中,耳可接受的耳用制劑具有低于約0.2eu/kg產物。在一些實施方案中,耳可接受的耳用制劑具有低于約5eu/g單位或產物。在其他實施方案中,耳可接受的耳用制劑具有低于約4eu/g單位或產物。在另外的實施方案中,耳可接受的耳用制劑具有低于約3eu/g單位或產物。在一些實施方案中,耳可接受的耳用制劑具有低于約5eu/mg單位或產物。在其他實施方案中,耳可接受的耳用制劑具有低于約4eu/mg單位或產物。在另外的實施方案中,耳可接受的耳用制劑具有低于約3eu/mg單位或產物。在某些實施方案中,本文所述的耳用組合物含有約1到約5eu/ml制劑。在某些實施方案中,本文所述的耳用組合物含有約2到約5eu/ml制劑、約3到約5eu/ml制劑或約4到約5eu/ml制劑。在某些實施方案中,本文所述的耳用組合物含有與傳統可接受的內毒素水平(例如,0.5eu/ml制劑)相比更低的內毒素水平(例如,<0.5eu/ml制劑)。在一些實施方案中,耳可接受的耳用制劑或裝置具有低于約0.5eu/ml制劑。在其他實施方案中,耳可接受的耳用制劑具有低于約0.4eu/ml制劑。在另外的實施方案中,耳可接受的耳用制劑具有低于約0.2eu/ml制劑。僅舉例而言,致熱原檢測通過若干種方法進行。針對無菌性的合適的測試包括在美國藥典(usp)<71>無菌性測試(第23版,1995)中描述的測試。兔致熱原測試和鱟變形細胞溶解物測試(limulusamebocytelysatetest)均在美國藥典第<85>和<151>章(usp23/nf18,biologicaltests,theunitedstatespharmacopeialconvention,rockville,md,1995)中說明。已基于單細胞活化-細胞因子試驗開發出替代的致熱原試驗。已開發出適用于質量控制應用的均一細胞系,并且這些細胞系已顯示出在已通過兔致熱原測試和鱟變形細胞溶解物測試的樣品中檢測致熱原性的能力(taktak等人,j.pharm.pharmacol.(1990),43:578-82)。在另外的實施方案中,對耳可接受的耳用治療劑制劑進行去熱原。在進一步的實施方案中,用于制備耳可接受的耳用治療劑制劑的過程包括測試制劑的致熱原性。在某些實施方案中,本文所述的制劑基本不含致熱原。ph和實際容量摩爾滲透壓濃度在一些實施方案中,本文公開的耳用組合物被配制為提供與外耳道(eac)相容的離子平衡。在一些實施方案中,制備本文公開的組合物,以便不擾亂外耳道(eac)的離子平衡。在一些實施方案中,本文公開的組合物具有與eac相同或基本相同的離子平衡。在一些實施方案中,本文公開的組合物不會擾亂eac的離子平衡以至于導致并發癥如耵聹分泌過多相關病況。如本文所用的,“實際容量摩爾滲透壓濃度(osmolarity)/重量摩爾滲透壓濃度(osmolality)”或“可遞送的容量摩爾滲透壓濃度/重量摩爾滲透壓濃度”意指通過測量活性劑和除了膠凝劑和/或增稠劑(例如,聚氧乙烯-聚氧丙烯共聚物、羧甲基纖維素等)之外的全部賦形劑的容量摩爾滲透壓濃度/重量摩爾滲透壓濃度而確定的組合物的容量摩爾滲透壓濃度/重量摩爾滲透壓濃度。本文公開的組合物的實際容量摩爾滲透壓濃度通過合適的方法來測量,例如,如在viegas等人,int.j.pharm.,1998,160,157-162中描述的冰點降低法。在一些情況下,本文公開的組合物的實際容量摩爾滲透壓濃度通過蒸汽壓滲透壓力測定法(例如,蒸汽壓降低法)來測量,該方法允許測定組合物在較高溫度下的容量摩爾滲透壓濃度。在一些情況下,蒸汽壓降低法允許測定包含膠凝劑(例如,熱可逆性聚合物)的組合物在較高溫度下的容量摩爾滲透壓濃度,其中該膠凝劑為凝膠形式。在一些實施方案中,本文所述的組合物在目標作用部位(例如,eac)處的容量摩爾滲透壓濃度與其遞送的容量摩爾滲透壓濃度大約相同。在一些實施方案中,本文所述的組合物具有約150mosm/l至約500mosm/l、約250mosm/l至約500mosm/l、約250mosm/l至約350mosm/l、約280mosm/l至約370mosm/l或約250mosm/l至約320mosm/l的可遞送容量摩爾滲透壓濃度。本文公開的耳用組合物的實際重量摩爾滲透壓濃度為約100mosm/kg至約1000mosm/kg、約200mosm/kg至約800mosm/kg、約250mosm/kg至約500mosm/kg,或約250mosm/kg至約320mosm/kg,或約250mosm/kg至約350mosm/kg,或約280mosm/kg至約320mosm/kg。在一些實施方案中,本文所述的組合物具有約100mosm/l至約1000mosm/l、約200mosm/l至約800mosm/l、約250mosm/l至約500mosm/l、約250mosm/l至約350mosm/l、約250mosm/l至約320mosm/l或約280mosm/l至約320mosm/l的實際容量摩爾滲透壓濃度。在一些實施方案中,將本文所述的組合物的ph調節(例如,通過使用緩沖液)至約5.5至9.0的eac相容ph范圍。在一些實施方案中,將本文所述的組合物的ph調節至約5.5至約8.5、約6至約8.5、約6.5至約8.0、約6.5至約8.0或約7.0至約8.0的eac相容的范圍。在一些實施方案中,將本文所述的組合物的ph調節至約7.0-7.6的適合eac的ph范圍。在一些實施方案中,有用的制劑還包含一種或多種ph調節劑或緩沖劑。合適的ph調節劑或緩沖液包括但不限于乙酸鹽、碳酸氫鹽、氯化銨、檸檬酸鹽、磷酸鹽、其藥學上可接受的鹽和組合或混合物。在一個實施方案中,當在本發明的制劑中使用一種或多種緩沖液時,它們與例如藥學上可接受的載體組合,并且以例如約0.1%至約20%、約0.5%至約10%范圍的量存在于最終的制劑中。在本發明的某些實施方案中,包含在凝膠制劑中的緩沖液的量為使得凝膠制劑的ph不干擾身體的自然緩沖系統的量。在一個實施方案中,還使用稀釋劑來穩定化合物,因為稀釋劑可提供更穩定的環境。溶解于緩沖溶液中的鹽(其還可提供ph控制或維持)在本領域中用作稀釋劑,包括但不限于磷酸鹽緩沖鹽水溶液。在一些實施方案中,本文所述的凝膠制劑具有這樣的ph,該ph允許在藥劑(例如,耳用藥劑)或包含凝膠的聚合物不降解的情況下將凝膠制劑滅菌(例如,通過過濾或無菌混合或熱處理和/或高壓滅菌(例如,最終滅菌))。為了降低滅菌過程中耳用藥劑和/或凝膠聚合物的水解和/或降解,緩沖液ph被設計為在滅菌(例如,高溫高壓滅菌)過程中維持制劑的ph在7-8范圍內。在特定的實施方案中,本文所述的凝膠制劑具有這樣的ph,該ph允許在藥劑(例如,耳用藥劑)或包含凝膠的聚合物不降解的情況下將凝膠制劑最終滅菌(例如,通過熱處理和/或高壓滅菌)。例如,為了降低高壓滅菌過程中耳用藥劑和/或凝膠聚合物的水解和/或降解,緩沖液ph被設計為在升高的溫度下維持制劑的ph在7-8范圍內。根據制劑中使用的耳用藥劑使用任何合適的緩沖液。在一些情況下,由于tris的pka隨溫度升高以約-0.03/℃降低,而pbs的pka隨溫度升高以約0.003/℃升高,因此在250°f(121℃)下高壓滅菌造成tris緩沖液明顯向下的ph變化(即酸性更強),而造成pbs緩沖液相對小得多的向上ph變化,并因此造成耳用藥劑在tris中比在pbs中大大增加的水解和/或降解。通過使用如本文所述的緩沖液和聚合添加劑(例如cmc)的適當組合來減少耳用藥劑的降解。在一些實施方案中,約5.0至約9.0、約5.5至約8.5、約6至約8.5、約6.5至約8.0、約6.5至約8.0、約7.0至約8.0、約7.0至約7.8、約7.0至約7.6、約7.2至7.6或約7.2至約7.4的制劑ph適合于本文所述的耳用制劑的滅菌(例如,通過過濾或無菌混合或熱處理和/或高壓滅菌(例如,最終滅菌))。在特定的實施方案中,約6.0、約6.5、約7.0、約7.1、約7.2、約7.3、約7.4、約7.5或約7.6的制劑ph適合于本文所述的任何組合物的滅菌(例如,通過過濾或無菌混合或熱處理和/或高壓滅菌(例如,最終滅菌))。在一些實施方案中,所述制劑具有如本文所述的ph,并且包含增稠劑(例如,粘度增強劑),舉非限制性實例而言,例如本文所述的纖維素基增稠劑。在一些情況下,二級聚合物(例如,增稠劑)的添加和如本文所述制劑的ph允許本文所述的制劑在耳用制劑中的耳用藥劑和/或聚合物組分沒有任何大量降解的情況下進行滅菌。在一些實施方案中,具有如本文所述的ph的制劑中熱可逆性泊洛沙姆與增稠劑的比例為約40:1、約35:1、約30:1、約25:1、約20:1、約15:1、約10:1或約5:1。例如,在某些實施方案中,本文所述的持續和/或延長釋放制劑包含比例為約40:1、約35:1、約30:1、約25:1、約20:1、約15:1、約10:1或約5:1的泊洛沙姆407(普朗尼克(pluronic)f127)與羧甲基纖維素(cmc)的組合。在一些實施方案中,本文所述的藥物制劑在至少約1天、至少約2天、至少約3天、至少約4天、至少約5天、至少約6天、至少約1周、至少約2周、至少約3周、至少約4周、至少約5周、至少約6周、至少約7周、至少約8周、至少約1個月、至少約2個月、至少約3個月、至少約4個月、至少約5個月或至少約6個月的任何時間段內在ph方面是穩定的。在其他實施方案中,本文所述的制劑在至少約1周的時間段內在ph方面是穩定的。本文還描述了在至少約1個月的時間段內在ph方面穩定的制劑。張度劑在一些實施方案中,張度劑以提供約100mosm/kg至約1000mosm/kg、約200mosm/kg至約800mosm/kg、約250mosm/kg至約500mosm/kg、或約250mosm/kg至約350mosm/kg、或約280mosm/kg至約320mosm/kg的耳用制劑實際重量摩爾滲透壓濃度的量添加至本文所述的制劑中。在一些實施方案中,本文所述的制劑具有約100mosm/l至約1000mosm/l、約200mosm/l至約800mosm/l、約250mosm/l至約500mosm/l、約250mosm/l至約350mosm/l、約280mosm/l至約320mosm/l或約250mosm/l至約320mosm/l的實際容量摩爾滲透壓濃度。在一些實施方案中,本文所述的任何制劑的可遞送容量摩爾滲透壓濃度被設計為與目標耳結構等滲。在一些實施方案中,本文所述的耳用組合物被配制為在目標作用部位處提供約250至約320mosm/l的遞送的容量摩爾滲透壓濃度;并且優選約270至約320mosm/l。在特定的實施方案中,本文所述的耳用組合物被配制為在目標作用部位處提供約250至約320mosm/kgh2o的遞送的重量摩爾滲透壓濃度;或約270至約320mosm/kgh2o的重量摩爾滲透壓濃度。在特定的實施方案中,調節制劑的可遞送容量摩爾滲透壓濃度/重量摩爾滲透壓濃度(即在不存在膠凝劑或增稠劑(例如,熱可逆性凝膠聚合物)的情況下制劑的容量摩爾滲透壓濃度/重量摩爾滲透壓濃度),例如,通過使用合適的鹽濃度(例如,鉀或鈉鹽的濃度)或使用張度劑,該張度劑使得在目標部位處遞送時制劑為相容的。由于變化量的水與聚合物的單體單元締合,因此包含熱可逆性凝膠聚合物的制劑的容量摩爾滲透壓濃度是不可靠的量度。制劑的實際容量摩爾滲透壓濃度(即,在不存在膠凝劑或增稠劑(例如熱可逆性凝膠聚合物)的情況下的容量摩爾滲透壓濃度))是可靠的量度,并通過任何合適的方法(例如,冰點降低法、蒸汽壓降低法)測量。在一些情況下,本文所述的制劑提供了可遞送容量摩爾滲透壓濃度(例如,在目標部位(例如,eac))處,其在施用時引起對環境的最小擾動并對哺乳動物引起最低程度的不適(例如,眩暈)。在一些實施方案中,合適的張度劑包括但不限于任何藥學上可接受的糖、鹽或其任意組合或混合物,諸如但不限于右旋糖、甘油、甘露醇、山梨醇、氯化鈉和其他電解質。有用的耳用組合物包含使組合物的重量摩爾滲透壓濃度處于可接受范圍內所需的量的一種或多種鹽。這樣的鹽包括具有鈉、鉀或銨陽離子,以及氯、檸檬酸根、抗壞血酸根、硼酸根、磷酸根、碳酸氫根、硫酸根、硫代硫酸根或亞硫酸氫根陰離子的那些鹽;合適的鹽包括氯化鈉、氯化鉀、硫代硫酸鈉、亞硫酸氫鈉和硫酸銨。顆粒大小使用縮減尺寸來增加表面積和/或調節制劑的溶出特性。縮減尺寸還用于維持本文所述的任何制劑的一致的平均粒度分布(psd)(例如,微米大小的顆粒、納米大小的顆粒等)。在一些實施方案中,本文所述的任何制劑包含多顆粒,即,多個顆粒大小(例如,微粒化的顆粒、納米大小的顆粒、非尺寸化的(non-sized)顆粒、膠體顆粒);即,該制劑是多顆粒制劑。在一些實施方案中,本文所述的任何制劑包含一種或多種多顆粒(例如,微粒化的)治療劑。微粒化是降低固體材料的顆粒的平均直徑的過程。微粒化的顆粒具有約微米大小的直徑至約納米大小的直徑。在一些實施方案中,微粒化固體的顆粒的平均直徑為約0.5μm至約500μm。在一些實施方案中,微粒化固體的顆粒的平均直徑為約1μm至約200μm。在一些實施方案中,微粒化固體的顆粒的平均直徑為約2μm至約100μm。在一些實施方案中,微粒化固體的顆粒的平均直徑為約3μm至約50μm。在一些實施方案中,顆粒狀微粒化固體包括小于約5微米、小于約20微米和/或小于約100微米的顆粒大小。在一些實施方案中,與包含非多顆粒的(例如,非微粒化的)耳用藥劑的制劑相比,耳用藥劑的顆粒(例如,微粒化的顆粒)的使用允許耳用藥劑從本文所述的任何制劑中延長和/或持續釋放。在一些情況下,含多顆粒的(例如微粒化的)耳用藥劑的制劑在沒有任何阻塞或堵塞的情況下從適配有27g針頭的1ml注射器中射出。舉例而言,顆粒大小縮減技術包括研磨、碾磨(例如,空氣-摩擦碾磨(噴射碾磨)、球磨)、凝聚、復凝聚、高壓勻漿、噴霧干燥和/或超臨界流體結晶。在一些情況下,顆粒通過機械撞擊(例如,通過錘式粉碎機、球磨機和/或針磨機)來尺寸化。在一些情況下,顆粒經由流體能(例如,通過螺旋噴射粉碎機(spiraljetmill)、循環噴射粉碎機(loopjetmill)和/或流化床噴射粉碎機(fluidizedbedjetmill))來尺寸化。在一些實施方案中,本文所述的制劑包含結晶顆粒和/或均質顆粒。在一些實施方案中,本文所述的制劑包含非晶形顆粒和/或非均質顆粒。在一些實施方案中,本文所述的制劑包含治療劑顆粒,其中該治療劑是治療劑的游離堿或鹽或前藥或其任意組合。在特定的實施方案中,本文所述的任何耳相容制劑包含一種或多種微粒化的藥劑(例如,耳用藥劑)。在一些這樣的實施方案中,微粒化的藥劑包含微粒化的顆粒。在一些這樣的實施方案中,微粒化的藥劑包含藥劑本身的微粒化顆粒,而沒有任何包衣或包封。在某些實施方案中,本文所述的藥物組合物包含作為微粒化粉末的耳用藥劑。在某些實施方案中,本文所述的藥物組合物包含微粒化的耳用藥劑粉末形式的耳用藥劑。在一些實施方案中,本文所述的多顆粒和/或微粒化的耳用藥劑通過耳可接受的凝膠基質遞送至耳結構(例如,eac)。可調的釋放特征活性劑從本文所述的任何制劑或組合物中的釋放任選地可調成所需的釋放特征。在一些實施方案中,本文所述的組合物是包含膠凝組分的溶液。在一些這樣的實施方案中,所述組合物提供了活性劑約1天至約14天、約1天至約12天、約2天至約10天或約3天至約8天的釋放。在一些實施方案中,本文所述的組合物包含膠凝劑(例如,泊洛沙姆407),并且提供了活性劑經約1天至約3天的時間段的釋放。在一些實施方案中,本文所述的組合物包含膠凝劑(例如,泊洛沙姆407),并且提供了活性劑經約1天至約5天的時間段的釋放。在一些實施方案中,本文所述的組合物包含膠凝劑(例如,泊洛沙姆407),并且提供了活性劑經約1天至約7天的時間段的釋放。在一些實施方案中,本文所述的組合物包含膠凝劑(例如,泊洛沙姆407),并且提供了活性劑經約2天至約7天的時間段的釋放。在一些實施方案中,本文所述的組合物包含膠凝劑(例如,泊洛沙姆407),并且提供了活性劑經約3天至約7天的時間段的釋放。在一些實施方案中,本文所述的組合物包含膠凝劑(例如,泊洛沙姆407),并且提供了活性劑經約1天至約10天的時間段的釋放。在一些實施方案中,本文所述的組合物包含膠凝劑(例如,泊洛沙姆407),并且提供了活性劑經約3天至約10天的時間段的釋放。在一些實施方案中,本文所述的組合物包含膠凝劑(例如,泊洛沙姆407),并且提供了活性劑經約1天至約14天的時間段的釋放。在一些實施方案中,本文所述的組合物包含與微粒化的耳用藥劑組合的膠凝劑(例如,泊洛沙姆407),并提供了經較長時間段的延長持續釋放。在一些實施方案中,本文所述的組合物包含約10-25%的膠凝劑(例如,泊洛沙姆407)和微粒化的耳用藥劑,并提供了經約1周至約10周的時間段的延長持續釋放。在一些實施方案中,本文所述的組合物包含約12-21%的膠凝劑(例如,泊洛沙姆407)和微粒化的耳用藥劑,并提供了經約1周至約6周的時間段的延長持續釋放。在一些實施方案中,本文所述的組合物包含約14-17%的膠凝劑(例如,泊洛沙姆407)和微粒化的耳用藥劑,并提供了經約1周至約3周的時間段的延長持續釋放。在一些實施方案中,本文所述的組合物包含約15-18%的膠凝劑(例如,泊洛沙姆407)和微粒化的耳用藥劑,并提供了經約1周至約3周的時間段的延長持續釋放。在一些實施方案中,本文所述的組合物包含約18-21%的膠凝劑(例如,泊洛沙姆407)和微粒化的耳用藥劑,并提供了經約3周至約6周的時間段的延長持續釋放。因此,組合物中膠凝劑的量和耳用藥劑的顆粒大小可調為達到耳用藥劑從該組合物中的所需釋放譜。如本文所述,相比于包含非微粒化的耳用藥劑的組合物,包含微粒化的耳用藥劑的組合物提供了經較長時間段的延長釋放。在一些情況下,微粒化的耳用藥劑通過緩慢降解提供了活性劑的穩定供給(例如,+/-20%),并充當活性劑的儲庫;這樣的儲庫效應延長了耳用藥劑在耳中的停留時間。在特定的實施方案中,與組合物中的膠凝劑的量組合的活性劑(例如,微粒化的活性劑)的合適的顆粒大小的選擇提供了可調的延長釋放特征,這允許活性劑經數小時、數天、數周或數月的時間段的釋放。在一些實施方案中,本文所述的任何制劑的粘度被設計為提供從耳相容凝膠中釋放的合適速率。在一些實施方案中,增稠劑(例如,膠凝組分,如聚氧乙烯-聚氧丙烯共聚物)的濃度允許可調的平均溶出時間(mdt)。mdt與活性劑從本文所述的組合物中的釋放速率成反比。實驗上,釋放的耳用藥劑任選地擬合至korsmeyer-peppas方程,其中q是在時間t時釋放的耳用藥劑的量,qα是耳用藥劑的總釋放量,k是第n階釋放常數,n是與溶出機制有關的無因次數,并且b是軸截距,描繪初始突釋機制的特征,其中n=1的特征為侵蝕控制機制。平均溶出時間(mdt)是藥物分子在釋放前在基質中停留的不同時間段的總和除以分子總數,并且任選地通過以下方程計算:例如,組合物的平均溶出時間(mdt)與膠凝劑(例如,泊洛沙姆)的濃度之間的線性關系表明耳用藥劑由于聚合物凝膠(例如,泊洛沙姆)的侵蝕而非經由擴散而釋放。在另一個實例中,非線性關系表明耳用藥劑經由擴散和/或聚合物凝膠降解的組合而釋放。在另一個實例中,組合物的更短的凝膠消除時程(活性劑的更快釋放)表明較低的平均溶出時間(mdt)。測定組合物中的膠凝組分和/或活性劑的濃度,以確定mdt的合適參數。在一些實施方案中,還測量注射體積,以確定臨床前和臨床研究的合適參數。凝膠強度和活性劑的濃度影響耳用藥劑從組合物釋放的動力學。在低泊洛沙姆濃度下,消除速率加速(mdt較低)。組合物中的耳用藥劑濃度的增加延長了耳用藥劑在耳中的停留時間和/或mdt。在一些實施方案中,泊洛沙姆從本文所述的組合物中溶出的mdt為至少6小時。在一些實施方案中,泊洛沙姆從本文所述的組合物中溶出的mdt為至少10小時。在一些實施方案中,活性劑從本文所述的組合物中溶出的mdt為約30小時至約48小時。在一些實施方案中,活性劑從本文所述的組合物中溶出的mdt為約30小時至約96小時。在一些實施方案中,活性劑從本文所述的組合物中溶出的mdt為約30小時至約1周。在一些實施方案中,本文所述的組合物的mdt為約1周至約6周。在一些實施方案中,活性劑在本文所述的組合物中的平均停留時間(mrt)為約20小時至約48小時。在一些實施方案中,活性劑在本文所述的組合物中的mrt為約20小時至約96小時。在一些實施方案中,活性劑在本文所述的組合物中的mrt為約20小時至約1周。在一些實施方案中,活性劑的mrt為約20小時。在一些實施方案中,活性劑的mrt為約30小時。在一些實施方案中,活性劑的mrt為約40小時。在一些實施方案中,活性劑的mrt為約50小時。在一些實施方案中,活性劑的mrt為約60小時。在一些實施方案中,活性劑的mrt為約70小時。在一些實施方案中,活性劑的mrt為約80小時。在一些實施方案中,活性劑的mrt為約90小時。在一些實施方案中,活性劑的mrt為約1周。在一些實施方案中,活性劑的mrt為約90小時。在一些實施方案中,本文所述的組合物的mrt為約1周至約6周。在一些實施方案中,活性劑的mrt為約1周。在一些實施方案中,活性劑的mrt為約2周。在一些實施方案中,活性劑的mrt為約3周。在一些實施方案中,活性劑的mrt為約4周。在一些實施方案中,活性劑的mrt為約5周。在一些實施方案中,活性劑的mrt為約4周。在一些實施方案中,活性劑的mrt為約6周。通過使用本文所述的程序測定eac中耳用藥劑的濃度,來確定每一種制劑的耳用藥劑的半衰期和耳用藥劑的平均停留時間。在某些實施方案中,與不是控制釋放耳用制劑的制劑相比,本文所述的任何控制釋放耳用制劑增加了耳用藥劑的暴露,并且使eac中的曲線下面積(auc)增加了約30%、約40%、約50%、約60%、約70%、約80%或約90%。在某些實施方案中,與不是控制釋放耳用制劑的制劑相比,本文所述的任何控制釋放耳用制劑增加了耳用藥劑的暴露時間,并且使eac中的cmax降低了約40%、約30%、約20%或約10%。在某些實施方案中,與不是控制釋放耳用制劑的制劑相比,本文所述的任何控制釋放耳用制劑改變(例如降低)了cmax與cmin之比。在某些實施方案中,與不是控制釋放耳用制劑的制劑相比,本文所述的任何控制釋放耳用制劑增加了耳用藥劑的暴露,并且使耳用藥劑的濃度在cmin以上的時間長度增加了約30%、約40%、約50%、約60%、約70%、約80%或約90%。在某些情況下,本文所述的控制釋放制劑延遲了到達cmax的時間。在某些情況下,藥物的受控穩定釋放延長了藥物的濃度將保持在cmin以上的時間。在一些實施方案中,本文所述的耳用組合物延長了藥物在耳中的停留時間,并且提供了穩定的藥物暴露分布。在一些情況下,組合物中活性劑濃度的增加使清除過程飽和,并允許達到更快速且穩定的穩態。在某些情況下,一旦藥物的藥物暴露(例如,eac)達到穩態,則eac中的藥物濃度就在治療劑量或大約治療劑量保持延長的一段時間(例如,至少1天、至少2天、至少3天、至少4天、至少5天、至少6天、至少1周、至少3周、至少6周或至少2個月)。在一些實施方案中,從本文所述的控制釋放制劑中釋放的活性劑的穩態濃度為從不是控制釋放制劑的制劑中釋放的活性劑的穩態濃度的約5至約20倍。在一些實施方案中,從本文所述的控制釋放制劑中釋放的活性劑的穩態濃度為從不是控制釋放制劑的制劑中釋放的活性劑的穩態濃度的約20至約50倍。圖3示出了活性劑從四種組合物中的預測的可調釋放。藥物制劑本文提供了包含至少一種耳用藥劑和藥學上可接受的稀釋劑、賦形劑或載體的藥物組合物。在一些實施方案中,該藥物組合物包含其他醫藥劑或藥劑、載體、佐劑(如防腐劑、穩定劑、潤濕劑或乳化劑)、溶液促進劑、用于調節滲透壓的鹽和/或緩沖劑。在其他的實施方案中,該藥物組合物還包含其他治療性物質。在一些實施方案中,本文所述組合物包含染料以幫助增強涂敷于eac時凝膠的可視化。在一些實施方案中,與本文所述的耳可接受的組合物相容的染料包括伊文思藍(例如,耳用制劑總重量的0.5%)、亞甲藍(例如,耳用制劑總重量的1%)、異硫藍(例如,耳用制劑總重量的1%)、臺盼藍(例如,耳用制劑總重量的0.15%)和/或吲哚菁綠(例如,25mg/小瓶)。其他常見染料,例如,fd&c紅40、fd&c紅3、fd&c黃5、fd&c黃6、fd&c藍1、fd&c藍2、fd&c綠3、熒光染料(例如,異硫氰酸熒光素、若丹明、alexafluor、dylightfluor)和/或結合非侵入性成像技術如mri、cat掃描、pet掃描等可視化的染料。還考慮將釓基mri染料、碘基染料、鋇基染料等用于本文所述的任何耳用制劑。與本文所述的任何制劑或組合物相容的其他染料在sigma-aldrich目錄中的染料下(其通過引用這樣的公開內容而包含在本文中)列出。在一些實施方案中,在本文所述的耳可接受的控制釋放耳用制劑中,耳用藥劑在凝膠基質中提供,其在本文也稱為“耳可接受的凝膠制劑”、“耳外部可接受的凝膠制劑”、“耳用凝膠制劑”或其變化形式。凝膠制劑的所有組分必須與目標耳結構相容。此外,該凝膠制劑提供耳用藥劑向目標耳結構內的所需部位的控制釋放;在一些實施方案中,該凝膠制劑還具有用于將耳用藥劑遞送至所需靶部位的立即或快速釋放組分。在其他的實施方案中,該凝膠制劑具有用于遞送耳用藥劑的持續釋放組分。在一些實施方案中,該凝膠制劑包含多顆粒(例如,微粒化的)耳用藥劑。在一些實施方案中,該耳用凝膠制劑是生物可降解的。在一些實施方案中,該耳用凝膠制劑是生物可蝕解的。在一些實施方案中,所述耳用凝膠制劑含有足以提供約500至1,000,000厘泊、約750至1,000,000厘泊、約1000至1,000,000厘泊、約1000至400,000厘泊、約2000至100,000厘泊、約3000至50,000厘泊、約4000至25,000厘泊、約5000至20,000厘泊、或約6000至15,000厘泊的粘度的粘度增強劑。在一些實施方案中,該耳用凝膠制劑含有足以提供約50,0000至1,000,000厘泊的粘度的粘度增強劑。在一些實施方案中,本文所述的組合物在體溫下為低粘度組合物。在一些實施方案中,低粘度組合物含有約1%至約10%的粘度增強劑(例如,膠凝組分,如聚氧乙烯-聚氧丙烯共聚物)。在一些實施方案中,低粘度組合物含有約2%至約10%的粘度增強劑(例如,膠凝組分,如聚氧乙烯-聚氧丙烯共聚物)。在一些實施方案中,低粘度組合物含有約5%至約10%的粘度增強劑(例如,膠凝組分,如聚氧乙烯-聚氧丙烯共聚物)。在一些實施方案中,低粘度組合物基本不含粘度增強劑(例如,膠凝組分,如聚氧乙烯-聚氧丙烯共聚物)。在一些實施方案中,本文所述的低粘度耳用藥劑組合物提供約100cp至約10,000cp的表觀粘度。在一些實施方案中,本文所述的低粘度耳用藥劑組合物提供約500cp至約10,000cp的表觀粘度。在一些實施方案中,本文所述的低粘度耳用藥劑組合物提供約1000cp至約10,000cp的表觀粘度。在一些實施方案中,本文所述的組合物在體溫下為高粘度組合物。在一些實施方案中,高粘度組合物含有約10%至約25%的粘度增強劑(例如,膠凝組分,如聚氧乙烯-聚氧丙烯共聚物)。在一些實施方案中,高粘度組合物含有約14%至約22%的粘度增強劑(例如,膠凝組分,如聚氧乙烯-聚氧丙烯共聚物)。在一些實施方案中,高粘度組合物含有約15%至約21%的粘度增強劑(例如,膠凝組分,如聚氧乙烯-聚氧丙烯共聚物)。在一些實施方案中,本文所述的高粘度耳用藥劑組合物提供約100,000cp至約1,000,000cp的表觀粘度。在一些實施方案中,本文所述的高粘度耳用藥劑組合物提供約150,000cp至約500,000cp的表觀粘度。在一些實施方案中,本文所述的高粘度耳用藥劑組合物提供約250,000cp至約500,000cp的表觀粘度。在一些這樣的實施方案中,高粘度組合物在室溫下為液體,而大約在室溫與體溫(包括嚴重發熱,例如高達約42℃的個體)之間的溫度下為凝膠。在一些實施方案中,耳用藥劑高粘度組合物作為用于治療本文所述耳部疾病或病況的單一療法施用。在一些實施方案中,本文所述的耳用藥物制劑進一步提供耳可接受的水凝膠;在進一步的實施方案中,該耳用藥物制劑提供耳可接受的原位成形水凝膠材料。在一些實施方案中,該耳用藥物制劑提供耳可接受的溶劑釋放凝膠。在一些實施方案中,該耳用藥物制劑提供光化輻射可固化凝膠。其他實施方案包括耳用藥物制劑中的熱可逆性凝膠,使得在室溫或更低溫度下制備凝膠時,該制劑為流體,但在將凝膠涂敷于eac靶部位內或eac靶部位附近(包括鼓膜的外表面)時,該耳用藥物制劑變硬或硬化為凝膠樣物質。在一些實施方案中,所述耳用凝膠制劑能夠通過注射器和針頭施用于鼓膜的外表面上或附近。在一些實施方案中,該耳用凝膠制劑能夠通過注射器施用于鼓膜的外表面上或附近。在一些實施方案中,該耳用凝膠制劑能夠通過滴管施用于鼓膜的外表面上或附近。在其他的實施方案中,該耳用凝膠制劑施用于外聽道上。在一些實施方案中,該制劑通過泵裝置或能夠將制劑遞送至鼓膜的外表面上或附近、外聽道上或其組合的另一種裝置來施用。在一些實施方案中,本文所述的任何藥物組合物包含在液體基質中的多顆粒耳用藥劑(例如,用于注射的液體組合物,或滴耳劑)。在某些實施方案中,本文所述的任何藥物組合物包含在固體基質中的多顆粒耳用藥劑。控制釋放制劑通常,控制釋放藥物制劑提供對藥物在釋放部位的釋放和體內釋放時間的控制。如本文中所討論的,控制釋放是指立即釋放、延遲釋放、持續釋放、延長釋放、可變釋放、脈沖釋放和雙模式釋放。控制釋放提供了許多優點。第一,藥劑的控制釋放允許頻率更低的給藥,并由此使重復治療最小化。第二,控制釋放治療導致更有效的藥物利用并使較少的化合物留作殘留物。第三,通過在病變部位處放置遞送裝置或制劑,控制釋放提供了局部藥物遞送的可能性。此外,借助于單一劑量單位,控制釋放為施用和釋放兩種或更多種不同的藥物(各自具有獨特的釋放曲線),或為相同藥物以不同的速率釋放或釋放不同的持續時間提供了機會。因此,本文公開的實施方案的一個方面是提供用于調節耵聹的產生以及治療耵聹分泌過多和耵聹分泌過多相關疾病的耳可接受的控制釋放組合物。本文公開的組合物和/或制劑和/或裝置的控制釋放特性通過多種試劑給予,該試劑包括但不限于對于在eac中使用來說可接受的賦形劑、試劑或材料。僅舉例而言,這樣的賦形劑、試劑或材料包括耳可接受的聚合物、耳可接受的粘度增強劑、耳可接受的凝膠、耳可接受的水凝膠、耳可接受的原位成形水凝膠材料、耳可接受的光化輻射可固化凝膠、耳可接受的溶劑釋放凝膠、耳可接受的納米囊或納米球、耳可接受的熱可逆性凝膠或其組合。耳可接受的凝膠凝膠,有時稱為膠凍,已經以各種方式被定義。例如,美國藥典將凝膠定義為或者由小無機顆粒構成的懸浮液組成的或者由被液體滲透的大有機分子組成的半固體體系。凝膠包括單相或兩相體系。單相凝膠由以分散的大分子與液體之間不存在明顯邊界的這樣一種方式均勻地分布在整個液體中的有機大分子組成。一些單相凝膠由合成大分子(例如,卡波姆)或由天然樹膠(例如,黃蓍膠)制備。在一些實施方案中,單相凝膠通常是水性的,但也可采用醇和油制備。兩相凝膠由離散小顆粒的網絡組成。凝膠還可分類為疏水性的或親水性的。在某些實施方案中,疏水性凝膠的基體由具有聚乙烯的液體石蠟或采用膠態二氧化硅或鋁或鋅皂膠凝的脂肪油組成。相比之下,疏水性凝膠的基體通常由采用合適的膠凝劑(例如,黃蓍膠、淀粉、纖維素衍生物、羧基乙烯基聚合物和硅酸鎂鋁)膠凝的水、甘油或丙二醇組成。在某些實施方案中,本文公開的組合物的流變學是假塑性的、塑性的、觸變性的或膨脹性的。在一個實施方案中,本文所述的粘度增強的耳可接受的制劑在室溫下不是液體。在某些實施方案中,該粘度增強的制劑的特征在于在室溫與體溫(包括具有嚴重發熱的個體,例如,高至約42℃)之間的相變。在一些實施方案中,在低于體溫1℃、低于體溫2℃、低于體溫3℃、低于體溫4℃、低于體溫6℃、低于體溫8℃或低于體溫10℃時發生相變。在一些實施方案中,在低于體溫約15℃、低于體溫約20℃或低于體溫約25℃時發生相變。在特定的實施方案中,本文所述的制劑的膠凝溫度(t膠凝)為約20℃、約25℃或約30℃。在某些實施方案中,本文所述的制劑的膠凝溫度(t膠凝)為約35℃或約40℃。在體溫的定義內包括健康個體或不健康個體的體溫,包括發熱(高至約42℃)個體的體溫。在一些實施方案中,本文所述的藥物組合物在大約室溫下是液體并在室溫下或大約室溫下施用。由聚氧丙烯和聚氧乙烯組成的聚合物在摻入到水溶液中時形成熱可逆性凝膠。這些聚合物具有在接近體溫的溫度下從液態變成凝膠態的能力,由此成為施用至目標耳結構的有用制劑。液態向凝膠態的相變取決于聚合物濃度和溶液中的成分。在一些實施方案中,本文所述的任何制劑中的熱可逆性聚合物的量為該制劑總重量的約10%、約15%、約20%、約25%、約30%、約35%或約40%。在一些實施方案中,本文所述的任何制劑中的熱可逆性聚合物的量為該制劑總重量的約10%、約11%、約12%、約13%、約14%、約15%、約16%、約17%、約18%、約19%、約20%、約21%、約22%、約23%、約24%或約25%。在一些實施方案中,本文所述的任何制劑中的熱可逆性聚合物(例如,泊洛沙姆407)的量為該制劑總重量的約7.5%。在一些實施方案中,本文所述的任何制劑中的熱可逆性聚合物(例如,泊洛沙姆407)的量為該制劑總重量的約10%。在一些實施方案中,本文所述的任何制劑中的熱可逆性聚合物(例如,泊洛沙姆407)的量為該制劑總重量的約11%。在一些實施方案中,本文所述的任何制劑中的熱可逆性聚合物(例如,泊洛沙姆407)的量為該制劑總重量的約12%。在一些實施方案中,本文所述的任何制劑中的熱可逆性聚合物(例如,泊洛沙姆407)的量為該制劑總重量的約13%。在一些實施方案中,本文所述的任何制劑中的熱可逆性聚合物(例如,泊洛沙姆407)的量為該制劑總重量的約14%。在一些實施方案中,本文所述的任何制劑中的熱可逆性聚合物(例如,泊洛沙姆407)的量為該制劑總重量的約15%。在一些實施方案中,本文所述的任何制劑中的熱可逆性聚合物(例如,泊洛沙姆407)的量為該制劑總重量的約16%。在一些實施方案中,本文所述的任何制劑中的熱可逆性聚合物(例如,泊洛沙姆407)的量為該制劑總重量的約17%。在一些實施方案中,本文所述的任何制劑中的熱可逆性聚合物(例如,泊洛沙姆407)的量為該制劑總重量的約18%。在一些實施方案中,本文所述的任何制劑中的熱可逆性聚合物(例如,泊洛沙姆407)的量為該制劑總重量的約19%。在一些實施方案中,本文所述的任何制劑中的熱可逆性聚合物(例如,泊洛沙姆407)的量為該制劑總重量的約20%。在一些實施方案中,本文所述的任何制劑中的熱可逆性聚合物(例如,泊洛沙姆407)的量為該制劑總重量的約21%。在一些實施方案中,本文所述的任何制劑中的熱可逆性聚合物(例如,泊洛沙姆407)的量為該制劑總重量的約23%。在一些實施方案中,本文所述的任何制劑中的熱可逆性聚合物(例如,泊洛沙姆407)的量為該制劑總重量的約25%。在一些實施方案中,本文所述的任何制劑中的增稠劑(例如,膠凝劑)的量為該制劑總重量的約1%、約5%、約10%或約15%。在一些實施方案中,本文所述的任何制劑中的增稠劑(例如,膠凝劑)的量為該制劑總重量的約0.5%、約1%、約1.5%、約2%、約2.5%、約3%、約3.5%、約4%、約4.5%或約5%。在替代的實施方案中,所述熱凝膠是peg-plga-peg三嵌段共聚物(jeong等人,nature(1997),388:860-2;jeong等人,j.control.release(2000),63:155-63;jeong等人,adv.drugdeliveryrev.(2002),54:37-51)。該聚合物在約5%w/w到約40%w/w的濃度內表現出溶膠-凝膠性質。根據期望的性質,plga共聚物中的丙交酯/乙交酯摩爾比在約1:1到約20:1的范圍內。所得共聚物在室溫下可溶于水并形成自由流動的液體,但在體溫下形成水凝膠。一種可商購的peg-plga-peg三嵌段共聚物是由boehringeringelheim生產的resomerrgpt50106。該材料由50:50聚(dl-丙交酯-共-乙交酯)的plga共聚物和10%w/w的peg組成,并具有約6000的分子量。其他生物可降解的熱塑性聚酯包括(由atrixlaboratories,inc.提供)和/或在例如美國專利號5,324,519、4,938,763、5,702,716、5,744,153和5,990,194中公開的那些;其中合適的生物可降解的熱塑性聚酯作為熱塑性聚合物公開。合適的生物可降解的熱塑性聚酯的實例包括聚丙交酯、聚乙交酯、聚己內酯,其共聚物、其三元共聚物及其任何組合。在一些這樣的實施方案中,合適的生物可降解的熱塑性聚酯是聚丙交酯、聚乙交酯,其共聚物、其三元共聚物或其組合。在一個實施方案中,生物可降解的熱塑性聚酯是具有羧基端基的50/50聚(dl-丙交酯-共-乙交酯);以該組合物的約30wt.%到約40wt.%存在;并具有約23,000到約45,000的平均分子量。或者,在另一個實施方案中,生物可降解的熱塑性聚酯是沒有羧基端基的75/25聚(dl-丙交酯-共-乙交酯);以該組合物的約40wt.%到約50wt.%存在;并具有約15,000到約24,000的平均分子量。在其他或替代的實施方案中,聚(dl-丙交酯-共-乙交酯)的端基是羥基、羧基或酯,這取決于聚合的方法。乳酸或乙醇酸的縮聚提供了具有末端羥基和羧基基團的聚合物。環狀丙交酯或乙交酯單體與水、乳酸或乙醇酸的開環聚合提供了具有相同端基的聚合物。然而,環狀單體與單官能醇如甲醇、乙醇或1-十二烷醇的開環提供了具有一個羥基基團和一個酯端基的聚合物。環狀單體與二醇如1,6-己二醇或聚乙二醇的開環聚合提供了僅具有羥基端基的聚合物。由于熱可逆性凝膠的聚合物體系在降低的溫度下更完全地溶解,因此溶解方法包括向將在降低的溫度下使用的量的水中添加所需量的聚合物。通常,在通過振搖使聚合物潤濕后,將混合物加蓋并放置在冷室中或放置在約0-10℃的恒溫容器中,以便使聚合物溶解。將該混合物攪拌或振搖,以使該熱可逆性凝膠聚合物更快溶解。隨后添加耳用藥劑和多種添加劑如緩沖液、鹽和防腐劑并使其溶解。在一些情況下,耳用藥劑和/或其他藥學活性劑如果不溶于水,則是懸浮的。通過添加合適的緩沖劑調節ph。。在一個實施方案中是不需要使用添加的粘度增強劑的耳可接受的藥用凝膠制劑。此類凝膠制劑中引入了至少一種藥學上可接受的緩沖液。在一個方面是包含耳用藥劑和藥學上可接受的緩沖液的凝膠制劑。在另一個實施方案中,藥學上可接受的賦形劑或載體是膠凝劑。在其他實施方案中,有用的耳用藥劑耳可接受的藥物制劑還包含一種或多種ph調節劑或緩沖劑,以提供適合eac的ph。合適的ph調節劑或緩沖液包括但不限于乙酸鹽、碳酸氫鹽、氯化銨、檸檬酸鹽、磷酸鹽、其藥學上可接受的鹽和組合或混合物。以使組合物的ph維持在約5到約9的ph(在一個實施方案中,ph為約6.5到約7.5,而在又一實施方案中,ph為約6.5、6.6、6.7、6.8、6.9、7.0、7.1、7.2、7.3、7.4、7.5)所需要的量包含此類ph調節劑和緩沖液。在一個實施方案中,當在本發明的制劑中使用一種或多種緩沖液時,它們與例如藥學上可接受的媒介物組合,并且以例如約0.1%到約20%、約0.5%到約10%范圍的量存在于最終制劑中。在本發明的某些實施方案中,包含在凝膠制劑中的緩沖液的量是使得凝膠制劑的ph不干擾eac的天然緩沖體系的量。在一些實施方案中,在凝膠制劑中存在約10μm到約200mm濃度的緩沖液。在某些實施方案中,存在約5mm到約200mm濃度的緩沖液。在某些實施方案中,存在約20mm到約100mm濃度的緩沖液。在一個實施方案中是微酸性ph的緩沖液,如乙酸鹽或檸檬酸鹽。在一個實施方案中,該緩沖液是ph為約4.5到約6.5的乙酸鈉緩沖液。在一個實施方案中,該緩沖液是ph為約5.0到約8.0或約5.5到約7.0的檸檬酸鈉緩沖液。在替代的實施方案中,所用的緩沖液是微堿性ph的三(羥甲基)氨基甲烷、碳酸氫鹽、碳酸鹽或磷酸鹽。在一個實施方案中,該緩沖液是ph為約6.5到約8.5或約7.0到約8.0的碳酸氫鈉緩沖液。在另一個實施方案中,該緩沖液是ph為約6.0到約9.0的磷酸氫二鈉緩沖液。本文中還描述了包含耳用藥劑和粘度增強劑的控制釋放制劑。僅舉例而言,合適的粘度增強劑包括膠凝劑和懸浮劑。在一個實施方案中,該粘度增強的制劑不包含緩沖液。在其他實施方案中,該粘度增強的制劑包含藥學上可接受的緩沖液。必要時,任選地使用氯化鈉或其他張度劑來調節張度。僅舉例而言,所述耳可接受的粘度劑包括羥丙基甲基纖維素、羥乙基纖維素、聚乙烯吡咯烷酮、羧甲基纖維素、聚乙烯醇、硫酸軟骨素鈉、透明質酸鈉。其他與目標耳結構相容的粘度增強劑包括但不限于阿拉伯膠(阿拉伯樹膠)、瓊脂、硅酸鎂鋁、藻酸鈉、硬脂酸鈉、墨角藻、膨潤土、卡波姆(carbomer)、角叉菜膠、卡波普(carbopol)、黃原膠、纖維素、微晶纖維素(mcc)、長角豆膠(ceratonia)、甲殼質、羧甲基殼聚糖、角叉菜(chondrus)、右旋糖、紅藻膠、明膠、印度樹膠(ghattigum)、瓜爾膠、鋰蒙脫石、乳糖、蔗糖、麥芽糊精、甘露醇、山梨醇、蜂蜜、玉米淀粉、小麥淀粉、米淀粉、馬鈴薯淀粉、明膠、梧桐膠、黃多糖膠、黃蓍膠、乙基纖維素、乙基羥乙基纖維素、乙基甲基纖維素、甲基纖維素、羥乙基纖維素、羥乙基甲基纖維素、羥丙基纖維素、聚(甲基丙烯酸羥乙酯)、氧化聚明膠、果膠、聚明膠肽、聚維酮、碳酸丙烯酯、甲基乙烯基醚/馬來酸酐共聚物(pvm/ma)、聚(甲基丙烯酸甲氧乙酯)、聚(甲基丙烯酸甲氧基乙氧基乙酯)、羥丙基纖維素、羥丙基甲基纖維素(hpmc)、羧甲基纖維素鈉(cmc)、二氧化硅、聚乙烯吡咯烷酮(pvp:聚維酮)、(右旋糖、麥芽糊精和三氯蔗糖)或其組合。在特定的實施方案中,該粘度增強賦形劑是mcc和cmc的組合。在另一個實施方案中,該粘度增強劑是羧甲基殼聚糖或甲殼質和藻酸鹽的組合。甲殼質和藻酸鹽與本文公開的耳用藥劑的組合充當控制釋放制劑,從而限制耳用藥劑從該制劑的擴散。此外,任選地使用羧甲基殼聚糖和藻酸鹽的組合來幫助增加耳用藥劑通過eac的皮膚的滲透性。在一些實施方案中是一種粘度增強的制劑,其包含約0.1mm到約100mm的耳用藥劑、藥學上可接受的粘度劑和注射用水,該粘度劑在水中的濃度足以提供最終粘度為約100cp到約100,000cp的粘度增強的制劑。在某些實施方案中,凝膠的粘度在約100cp到約50,000cp、約100cp到約1,000cp、約500cp到約1500cp、約1000cp到約3000cp、約2000cp到約8,000cp、約4,000cp到約50,000cp、約10,000cp到約500,000cp、約15,000cp到約1,000,000cp的范圍內。在其他實施方案中,當需要更粘的介質時,該生物相容的凝膠包含至少約35重量%、至少約45重量%、至少約55重量%、至少約65重量%、至少約70重量%、至少約75重量%或甚至至少約80重量%左右的耳用藥劑。在高度濃縮的樣品中,該生物相容的粘度增強的制劑包含至少約25重量%、至少約35重量%、至少約45重量%、至少約55重量%、至少約65重量%、至少約75重量%、至少約85重量%、至少約90重量%或至少約95重量%或更多的耳用藥劑。在一些實施方案中,本文中提出的凝膠制劑的粘度通過所描述的任何手段來測量。例如,在一些實施方案中,使用lvdv-ii+cp錐板粘度計和conespindlecpe-40來計算本文所述的凝膠制劑的粘度。在其他實施方案中,使用brookfield(軸和杯)粘度計來計算本文所述的凝膠制劑的粘度。在一些實施方案中,在室溫下測量本文提及的粘度范圍。在其他實施方案中,在體溫下(例如,在健康人的平均體溫下)測量本文所提及的粘度范圍。在一個實施方案中,所述藥學上可接受的粘度增強的耳可接受的制劑包含至少一種耳用藥劑和至少一種膠凝劑。用于制備凝膠制劑的合適的膠凝劑包括但不限于纖維素、纖維素衍生物、纖維素醚(例如,羧甲基纖維素、乙基纖維素、羥乙基纖維素、羥甲基纖維素、羥丙基甲基纖維素、羥丙基纖維素、甲基纖維素)、瓜爾膠、黃原膠、刺槐豆膠、藻酸鹽(例如,藻酸)、硅酸鹽、淀粉、黃蓍膠、羧基乙烯基聚合物、角叉菜膠、石蠟、礦脂及其任意組合或混合物。在一些其他實施方案中,使用羥丙基甲基纖維素作為膠凝劑。在某些實施方案中,還使用本文所述的粘度增強劑作為本文提出的凝膠制劑的膠凝劑。在一些實施方案中,根據所用的特定耳用藥劑、其他藥劑或賦形劑/添加劑,其他凝膠制劑是有用的,并且因此被認為落入本公開內容的范圍內。例如,其他可商購的基于甘油的凝膠、甘油衍生的化合物、綴合或交聯凝膠、基質、水凝膠和聚合物,以及明膠及其衍生物、藻酸鹽和基于藻酸鹽的凝膠,和甚至各種天然和合成的水凝膠和水凝膠衍生的化合物,預計在本文所述的耳用藥劑制劑中都是有用的。在一些實施方案中,耳可接受的凝膠包括但不限于藻酸鹽水凝膠(convatec,princeton,n.j.)、hydroactivegel(convatec)、(johnson&johnsonmedical,arlington,tex.);(v)acemannanhydrogel(carringtonlaboratories,inc.,irving,tex.);甘油凝膠hydrogel(swiss-americanproducts,inc.,dallas,tex.)和sterile(johnson&johnson)。在進一步的實施方案中,生物可降解、生物相容的凝膠也代表存在于本文公開和描述的耳可接受的制劑中的化合物。在一些為了施用于哺乳動物而開發的制劑中,以及對于配制用于人類施用的組合物,耳可接受的凝膠占據該組合物的基本上全部重量。在其他實施方案中,該耳可接受的凝膠占該組合物的多達約98重量%或約99重量%。當需要基本非流動性或基本粘性的制劑時,這是期望的。在進一步的實施方案中,當需要粘度略低或流動性略大的耳可接受的藥物凝膠制劑時,該制劑的生物相容的凝膠部分占該化合物的至少約50重量%、至少約60重量%、至少約70重量%或甚至至少約80重量%或90重量%。這些范圍內的所有中間的整數被認為均落入本公開內容的范圍內,并且在一些替代的實施方案中,配制了流動性甚至更大(從而粘度更低)的耳可接受的凝膠組合物,例如,在其中混合物的凝膠或基質組分占組合物的不超過約50重量%、不超過約40重量%、不超過約30重量%的那些組合物,或者甚至占組合物的不超過約15重量%或約20重量%的那些組合物。耳可接受的懸浮劑在一個實施方案中,至少一種耳用藥劑被包含在藥學上可接受的粘度增強的制劑中,其中該制劑進一步包含至少一種懸浮劑,其中該懸浮劑有助于賦予該制劑控制釋放特性。在一些實施方案中,懸浮劑還用于增加耳可接受的制劑和組合物的粘度。僅舉例而言,懸浮劑包括化合物,如聚乙烯吡咯烷酮,例如聚乙烯吡咯烷酮k12、聚乙烯吡咯烷酮k17、聚乙烯吡咯烷酮k25或聚乙烯吡咯烷酮k30,乙烯基吡咯烷酮/乙酸乙烯酯共聚物(s630),羧甲基纖維素鈉,甲基纖維素,羥丙基甲基纖維素(羥丙甲纖維素),羥甲基纖維素乙酸硬脂酸酯,聚山梨酯-80,羥乙基纖維素,藻酸鈉,樹膠,例如黃蓍膠和阿拉伯膠、瓜爾膠、黃原膠(包括黃原膠樹膠),糖,纖維素材料,例如羧甲基纖維素鈉、甲基纖維素、羧甲基纖維素鈉、羥丙基甲基纖維素、羥乙基纖維素,聚山梨酯-80,藻酸鈉,聚乙氧基化失水山梨醇單月桂酸酯,聚乙氧基化失水山梨醇單月桂酸酯,聚維酮,等等。在一些實施方案中,有用的水性懸浮液還包含作為懸浮劑的一種或多種聚合物。有用的聚合物包括水溶性聚合物,如纖維素聚合物,例如,羥丙基甲基纖維素,以及水不溶性聚合物,如交聯的含羧基聚合物。在一個實施方案中,本發明提供了耳可接受的凝膠組合物,其包含在羥乙基纖維素凝膠中的治療有效量的耳用藥劑。獲得呈干燥粉末的羥乙基纖維素(hec),其在水或水性緩沖溶液中重建以得到所需粘度(通常為約200cps至約30,000cps,對應于約0.2%至約10%hec)。在一個實施方案中,hec的濃度為約1%至約15%,約1%至約2%,或約1.5%至約2%。在其他的實施方案中,包括凝膠制劑和粘度增強的制劑在內的耳可接受的制劑進一步包含賦形劑、其他醫藥劑或藥劑、載體、佐劑(如防腐劑、穩定劑、潤濕劑或乳化劑)、溶液促進劑、鹽、增溶劑、消泡劑、抗氧化劑、分散劑、潤濕劑、表面活性劑及其組合。耳可接受的光化輻射可固化凝膠在其他的實施方案中,所述凝膠為光化輻射可固化凝膠,使得在施用于目標耳結構或其附近之后,使用光化輻射(或光,包括紫外線、可見光或紅外線),形成所需的凝膠性質。僅舉例而言,光纖用于提供光化輻射,以便形成所需的凝膠性質。在一些實施方案中,光纖和凝膠施用裝置構成單一單元。在其他的實施方案中,分開提供光纖和凝膠施用裝置。耳可接受的溶劑釋放凝膠在一些實施方案中,所述凝膠為溶劑釋放凝膠,使得在施用于目標耳結構或其附近之后形成所需凝膠性質,即,隨著注射的凝膠制劑中的溶劑從凝膠中擴散出,形成具有所需凝膠性質的凝膠。例如,將包含乙酸異丁酸蔗糖酯、藥學上可接受的溶劑、一種或多種添加劑以及耳用藥劑的制劑施用于eac內:溶劑從注射的制劑中的擴散提供了具有所需凝膠性質的儲庫(depot)。例如,當溶劑從注射的制劑中迅速擴散出時,水溶性溶劑的使用提供了高粘度的儲庫。另一方面,疏水性溶劑(例如,苯甲酸芐酯)的使用提供了粘性較低的儲庫。耳可接受的溶劑釋放凝膠制劑的一個實例是由durectcorporation銷售的sabertm遞送系統。耳可接受的環糊精和其他穩定制劑在具體的實施方案中,所述耳可接受的制劑備選地包含環糊精。環糊精為含有6、7或8個吡喃葡萄糖單元的環狀寡糖,分別被稱為α-環糊精、β-環糊精或γ-環糊精。環糊精具有增強水溶性的親水性外部和形成空腔的疏水性內部。在水性環境中,其他分子的疏水性部分通常進入環糊精的疏水腔中以形成包合物。此外,環糊精還能夠與不在疏水腔內部的分子發生其他類型的非鍵合相互作用。環糊精的每個吡喃葡萄糖單元均具有三個游離羥基,或在α-環糊精上具有18個羥基,在β-環糊精上具有21個羥基,而在γ-環糊精上具有24個羥基。這些羥基中的一個或多個可以與許多試劑中的任一種反應以形成很多種環糊精衍生物,包括羥丙基醚、磺酸酯和磺基烷基醚。以下示出了β-環糊精和羥丙基-β-環糊精(hpβcd)的結構。在一些實施方案中,在本文所述的藥物組合物中使用環糊精改善了藥物的溶解度。包合物與許多提高溶解度的情況有關;然而,環糊精與不溶性化合物之間的其他相互作用也改善了溶解度。羥丙基-β-環糊精(hpβcd)作為無熱原產品是可商購獲得的。它是易溶于水的非吸濕性白色粉末。hpβcd是熱穩定的,并且在中性ph下不降解。因此,環糊精改善了治療劑在組合物或制劑中的溶解度。因此,在一些實施方案中,包含環糊精以提高本文所述制劑內的耳可接受的耳用藥劑的溶解度。在其他的實施方案中,環糊精另外用作本文所述制劑內的控制釋放賦形劑。僅舉例而言,使用的環糊精衍生物包括α-環糊精、β-環糊精、γ-環糊精、羥乙基β-環糊精、羥丙基γ-環糊精、硫酸化β-環糊精、硫酸化α-環糊精、磺丁基醚β-環糊精。在本文公開的組合物和方法中使用的環糊精的濃度根據理化性質、藥代動力學性質、副作用或不良事件、配制考慮因素或與治療活性劑或其鹽或前藥相關的其他因素而變化,或隨著組合物中其他賦形劑的性質而變化。因此,在某些情況下,在根據本文公開的組合物和方法中使用的環糊精的濃度或量將根據需要而變化。在使用時,利用本文所述的原理、實例和教導來選擇提高耳用藥劑的溶解度和/或在本文所述的任何制劑中起到控制釋放賦形劑的作用所需的環糊精的量。在本文公開的耳可接受的制劑中有用的其他穩定劑包括,例如,脂肪酸、脂肪醇、醇、長鏈脂肪酸酯、長鏈醚、脂肪酸的親水性衍生物、聚乙烯吡咯烷酮、聚乙烯醚、聚乙烯醇、烴、疏水性聚合物、吸濕性聚合物及其組合。在一些實施方案中,還使用穩定劑的酰胺類似物。在進一步的實施方案中,所選擇的穩定劑改變制劑的疏水性(例如油酸、蠟),或改善制劑中各種組分的混合(例如乙醇),控制配方中的水分含量(例如,pvp或聚乙烯吡咯烷酮),控制相的流動性(具有高于室溫的熔點的物質,如長鏈脂肪酸、醇、酯、醚、酰胺等或其混合物;蠟)。在另一個實施方案中,這些穩定劑中的一些用作溶劑/共溶劑(例如,乙醇)。在其他的實施方案中,穩定劑以足以抑制耳用藥劑的降解的量存在。這樣的穩定劑的實例包括但不限于:(a)約0.5%至約2%w/v的甘油,(b)約0.1%至約1%w/v的甲硫氨酸,(c)約0.1%至約2%w/v的一硫代甘油,(d)約1mm至約10mm的edta,(e)約0.01%至約2%w/v的抗壞血酸,(f)0.003%至約0.02%w/v的聚山梨酯80,(g)0.001%至約0.05%w/v的聚山梨酯20,(h)精氨酸,(i)肝素,(j)硫酸葡聚糖,(k)環糊精,(l)戊聚糖多硫酸酯和其他類肝素,(m)二價陽離子,如鎂和鋅;或(n)其組合。另外的有用的耳可接受的耳用藥劑制劑包含一種或多種抗聚集添加劑,以通過降低蛋白質聚集速率提高耳用藥劑制劑的穩定性。所選擇的抗聚集添加劑取決于耳用藥劑例如耳用藥劑抗體所暴露的條件的性質。例如,某些經歷攪拌和熱應力的制劑需要與經歷凍干和重建的制劑不同的抗聚集添加劑。僅舉例而言,有用的抗聚集添加劑包括尿素、氯化胍、簡單氨基酸如甘氨酸或精氨酸、糖、多元醇、聚山梨酯、聚合物如聚乙二醇和葡聚糖、烷基糖如烷基糖苷以及表面活性劑。在需要的情況下,其他有用的制劑任選地包含一種或多種耳可接受的抗氧化劑以增強化學穩定性。僅舉例而言,合適的抗氧化劑包括抗壞血酸、甲硫氨酸、硫代硫酸鈉和焦亞硫酸鈉。在一個實施方案中,抗氧化劑選自金屬螯合劑、含巰基化合物和其他一般穩定劑。其他有用的組合物包含一種或多種耳可接受的表面活性劑以增強物理穩定性或用于其他目的。合適的非離子型表面活性劑包括但不限于聚氧乙烯脂肪酸甘油酯和植物油,例如聚氧乙烯(60)氫化蓖麻油;以及聚氧乙烯烷基醚和烷基苯基醚,例如辛苯聚醇10、辛苯聚醇40。在一些實施方案中,本文所述的耳可接受的藥物制劑經以下的任一個時間段在化合物降解方面是穩定的:至少約1天、至少約2天、至少約3天、至少約4天、至少約5天、至少約6天、至少約1周、至少約2周、至少約3周、至少約4周、至少約5周、至少約6周、至少約7周、至少約8周、至少約3個月、至少約4個月、至少約5個月或至少約6個月。在其他的實施方案中,本文所述的制劑經至少約1周的時間段在化合物降解方面是穩定的。本文還描述了經至少約1個月的時間段在化合物降解方面穩定的制劑。在其他實施方案中,另外的表面活性劑(助表面活性劑)和/或緩沖劑與本文先前所述的一種或多種藥學上可接受的媒介物組合,使得該表面活性劑和/或緩沖劑將產品維持在關于穩定性的最佳ph下。合適的助表面活性劑包括但不限于:a)天然和合成的親脂性試劑,例如磷脂、膽固醇和膽固醇脂肪酸酯及其衍生物;b)非離子型表面活性劑,其包括例如聚氧乙烯脂肪醇酯,失水山梨醇脂肪酸酯(spans),聚氧乙烯失水山梨醇脂肪酸酯(例如,聚氧乙烯(20)失水山梨醇單油酸酯(吐溫80)、聚氧乙烯(20)失水山梨醇單硬脂酸酯(吐溫60)、聚氧乙烯(20)失水山梨醇單月桂酸酯(吐溫20)以及其他吐溫),失水山梨醇酯,甘油酯(例如myrj和三乙酸甘油酯(三醋精)),聚乙二醇,鯨蠟醇,十六十八醇(cetostearylalcohol),硬脂醇,聚山梨酯80,泊洛沙姆(poloxamer),泊洛沙胺(poloxamine),聚氧乙烯蓖麻油衍生物(例如,rh40、cremphora25、cremphora20、el)及其他cremophor,磺基琥珀酸酯,烷基硫酸酯(sls);peg甘油脂肪酸酯,如peg-8甘油辛酸酯/癸酸酯(labrasol)、peg-4甘油辛酸酯/癸酸酯(labrafachydrowl1219)、peg-32甘油月桂酸酯(gelucire444/14)、peg-6甘油單油酸酯(labrafilm1944cs)、peg-6甘油亞油酸酯(labrafilm2125cs);丙二醇單脂肪酸酯和丙二醇二脂肪酸酯,如丙二醇月桂酸酯、丙二醇辛酸酯/癸酸酯;700,抗壞血酸基-6-棕櫚酸酯,硬脂胺,十二烷基硫酸鈉,聚氧乙烯甘油三蓖麻油酸酯及其任何組合或混合物;c)陰離子型表面活性劑,包括但不限于羧甲基纖維素鈣、羧甲基纖維素鈉、磺基琥珀酸鈉、二辛基、藻酸鈉、烷基聚氧乙烯硫酸酯、十二烷基硫酸鈉、三乙醇胺硬脂酸酯、月桂酸鉀、膽汁鹽及其任何組合或混合物;以及d)陽離子型表面活性劑,如十六烷基三甲基溴化銨和月桂基二甲基芐基氯化銨。在進一步的實施方案中,當一種或多種助表面活性劑在本發明的耳可接受的制劑中使用時,它們例如與藥學上可接受的媒介物組合,并以例如在約0.1%至約20%、約0.5%至約10%范圍內的量存在于最終制劑中。在一個實施方案中,所述表面活性劑具有0至20的hlb值。在其他的實施方案中,所述表面活性劑具有0至3、4至6、7至9、8至18、13至15、10至18的hlb值。在一個實施方案中,稀釋劑由于提供更穩定的環境也用于穩定耳用藥劑或其他藥物化合物。溶解于緩沖溶液中的鹽(其還可以提供ph控制或維持)用作稀釋劑,包括但不限于磷酸鹽緩沖鹽水溶液。在其他的實施方案中,凝膠制劑與eac等滲。通過添加張度劑提供等滲制劑。合適的張度劑包括但不限于任何藥學上可接受的糖、鹽或其任何組合或混合物,例如但不限于右旋糖和氯化鈉。在進一步的實施方案中,張度劑以約100mosm/kg至約500mosm/kg的量存在。在一些實施方案中,張度劑以約200mosm/kg至約400mosm/kg、約280mosm/kg至約320mosm/kg的量存在。如本文所述,張度劑的量將取決于藥物制劑的靶結構。有用的張度組合物還包含使組合物的重量摩爾滲透壓濃度處于涂敷于eac的可接受的范圍內所需的量的一種或多種鹽。這樣的鹽包括具有鈉、鉀或銨陽離子以及氯離子、檸檬酸根、抗壞血酸根、硼酸根、磷酸根、碳酸氫根、硫酸根、硫代硫酸根或亞硫酸氫根陰離子的那些鹽;合適的鹽包括氯化鈉、氯化鉀、硫代硫酸鈉、亞硫酸氫鈉和硫酸銨。在一些實施方案中,本文公開的耳可接受的凝膠制劑備選地或附加地包含防腐劑以防止微生物生長。用于本文所述的粘度增強的制劑的合適的耳可接受的防腐劑包括但不限于苯甲酸、硼酸、對羥基苯甲酸酯、醇、季化合物(quarternarycompound)、穩定的二氧化氯、汞劑如硼酸苯汞(merfen)和硫柳汞、前述的混合物等。在進一步的實施方案中,僅舉例而言,防腐劑是在本文提供的耳可接受的制劑內的耳用藥劑。在一個實施方案中,該制劑包含防腐劑,僅舉例而言,如對羥基苯甲酸甲酯、亞硫酸氫鈉、硫代硫酸鈉、抗壞血酸鹽、氯丁醇、硫柳汞、對羥基苯甲酸酯、苯甲醇、苯乙醇等。在另一個實施方案中,對羥基苯甲酸甲酯為約0.05%至約1.0%、約0.1%至約0.2%的濃度。在進一步的實施方案中,通過將水、對羥基苯甲酸甲酯、羥乙基纖維素和檸檬酸鈉混合來制備凝膠。在進一步的實施方案中,通過將水、對羥基苯甲酸甲酯、羥乙基纖維素和乙酸鈉混合來制備凝膠。在進一步的實施方案中,通過在120℃下高壓滅菌約20分鐘對混合物進行滅菌,并測試混合物的ph、對羥基苯甲酸甲酯濃度和粘度,然后將混合物與適量的本文公開的耳用藥劑混合。在藥物遞送媒介物中使用的合適的耳可接受的水溶性防腐劑包括亞硫酸氫鈉、硫代硫酸鈉、抗壞血酸鹽、氯丁醇、硫柳汞、對羥基苯甲酸酯、苯甲醇、丁羥甲苯(bht)、苯乙醇等。這些試劑通常以約0.001重量%至約5重量%的量,或以約0.01重量%至約2重量%的量存在。在一些實施方案中,本文所述的耳相容性制劑不含防腐劑。賦形劑在一些實施方案中,包括凝膠制劑和粘度增強的制劑在內的耳可接受的制劑進一步包含賦形劑、其他醫藥劑或藥劑、載體、佐劑(如防腐劑、穩定劑、潤濕劑或乳化劑)、溶液促進劑、鹽、增溶劑、抗氧化劑、分散劑、潤濕劑、表面活性劑及其組合。在本文所述的耳可接受的制劑中使用的合適的載體包括但不限于與目標耳結構的生理環境相容的任何藥學上可接受的溶劑。在其他的實施方案中,基質為藥學上可接受的表面活性劑和溶劑的組合。在一些實施方案中,其他賦形劑包括硬脂酰富馬酸鈉、二乙醇胺硫酸鯨蠟酯、異硬脂酸酯、聚乙氧基化蓖麻油、壬氧基10(nonoxyl10)、辛苯聚醇9、十二烷基硫酸鈉、失水山梨醇酯(失水山梨醇單月桂酸酯、失水山梨醇單油酸酯、失水山梨醇單棕櫚酸酯、失水山梨醇單硬脂酸酯、失水山梨醇倍半油酸酯、失水山梨醇三油酸酯、失水山梨醇三硬脂酸酯、失水山梨醇月桂酸酯、失水山梨醇油酸酯、失水山梨醇棕櫚酸酯、失水山梨醇硬脂酸酯、失水山梨醇二油酸酯、失水山梨醇倍半異硬脂酸酯、失水山梨醇倍半硬脂酸酯、失水山梨醇三異硬脂酸酯)、卵磷脂、其藥學上可接受的鹽及其組合或混合物。在其他的實施方案中,載體為聚山梨酯。聚山梨酯為非離子型表面活性劑失水山梨醇酯。在本發明中有用的聚山梨酯包括但不限于聚山梨酯20、聚山梨酯40、聚山梨酯60、聚山梨酯80(吐溫80)及其任何組合或混合物。在進一步的實施方案中,聚山梨酯80用作藥學上可接受的載體。在一個實施方案中,在制備藥物遞送媒介物中使用的水溶性甘油基耳可接受的粘度增強的制劑包含至少一種含有至少約0.1%或更多的水溶性甘油化合物的耳用藥劑。在一些實施方案中,耳用藥劑的百分比在總藥物制劑的重量或體積的約1%至約95%、約5%至約80%、約10%至約60%或更高百分比之間變化。在一些實施方案中,每種治療上有用的耳用藥劑制劑中的化合物的量以在任何給定的化合物單位劑量中獲得合適的劑量的方式進行制備。本文考慮了諸如溶解度、生物利用度、生物半衰期、給藥途徑、產品保質期以及其他藥理學考慮因素墻因素。如需要,所述耳可接受的藥用凝膠除了緩沖劑之外還含有助溶劑、防腐劑、共溶劑、離子強度和重量摩爾滲透壓濃度調節劑和其他賦形劑。合適的耳可接受的水溶性緩沖劑是堿或堿土金屬的碳酸鹽、磷酸鹽、碳酸氫鹽、檸檬酸鹽、硼酸鹽、乙酸鹽、琥珀酸鹽等,如磷酸鈉、檸檬酸鈉、硼酸鈉、乙酸鈉、碳酸氫鈉、碳酸鈉和氨丁三醇(tris)。這些試劑均以足以使系統的ph維持在7.4±0.2且優選7.4的量存在。因此,按總組合物的重量計,緩沖劑為多達5%。共溶劑用于提高耳用藥劑的溶解度,然而,一些耳用藥劑或其他藥物化合物是不溶性的。這些通常在合適的懸浮劑或粘度增強劑的幫助下懸浮于聚合物媒介物中。此外,一些藥物賦形劑、稀釋劑或載體是潛在耳毒性的。例如,苯扎氯銨(一種常見防腐劑)是耳毒性的,因此在引入耳中時是潛在有害的。在配制控制釋放耳用藥劑制劑時,建議避免或組合適當的賦形劑、稀釋劑或載體以減少或消除來自制劑的潛在耳毒性組分,或減少這樣的賦形劑、稀釋劑或載體的量。任選地,控制釋放耳用藥劑制劑包括耳保護劑,如抗氧化劑、α硫辛酸、鈣、磷霉素或鐵螯合劑,以抵消可能由特定的治療劑或賦形劑、稀釋劑或載體的使用而引起的潛在耳毒性作用。治療方式給藥方法和時間表遞送至eac的藥物通常通過注射來施用。在一些實施方案中,遞送系統為能夠將本文公開的耳用組合物或制劑釋放到鼓膜的表面上或外聽道中的注射器和針頭裝置。在一些實施方案中,在注射器上的針頭比18號針頭更粗。在另一個實施方案中,針頭規格為18號到31號。在進一步的實施方案中,針頭規格為25號到30號。根據耳用藥劑組合物或制劑的稠度或粘度,注射器或皮下注射針頭的規格水平可相應地變化。在另一個實施方案中,針頭的內徑可通過減少針頭的壁厚(常稱為薄壁或超薄壁針頭)而增加,以降低針頭堵塞的可能性,同時保持足夠的針頭規格。在一些實施方案中,所述針頭是用于即時遞送凝膠制劑的針頭。該針頭可以是單次使用針頭或一次性針頭。在一些實施方案中,可使用注射器遞送如本文公開的藥學上可接受的基于凝膠的含有耳用藥劑的組合物,其中該注射器具有壓配式(魯爾(luer))或旋緊張式(魯爾鎖(luer-lock))接頭。在一個實施方案中,該注射器是皮下注射器。在另一個實施方案中,該注射器由塑料或玻璃制成。在又一個實施方案中,該皮下注射器是一次性使用的注射器。在進一步的實施方案中,玻璃注射器能夠進行滅菌。在進一步的實施方案中,通過高壓滅菌器進行滅菌。在另一個實施方案中,該注射器包括圓柱形注射器主體,在使用前凝膠制劑儲存于其中。在其他實施方案中,該注射器包括圓柱形注射器主體,在使用前如本文公開的藥學上可接受的基于凝膠的耳用藥劑組合物儲存于其中,這方便地允許與合適的藥學上可接受的緩沖液混合。在其他實施方案中,該注射器可含有其他賦形劑、穩定劑、懸浮劑、稀釋劑或其組合,以使其中所含的耳用藥劑或其他藥物化合物穩定或穩定地儲存。在一些實施方案中,所述注射器含有圓柱形注射器主體,其中該主體被區室化,使得每個區室能夠儲存耳可接受的耳用藥劑凝膠制劑的至少一種組分。在進一步的實施方案中,具有區室化的主體的注射器允許組分在注射至eac之前混合。在其他實施方案中,遞送系統包括多個注射器,所述多個注射器中的每個注射器均含有凝膠制劑的至少一種組分,使得各組分在注射之前預混合或在注射后混合。在進一步的實施方案中,本文公開的注射器包含至少一個儲室,其中所述至少一個儲室包含耳用藥劑或藥學上可接受的緩沖液或粘度增強劑(如膠凝劑)或其組合。可商購的注射裝置任選地以其最簡形式使用,作為具有注射筒、帶有針頭的針頭組裝體、帶有柱塞桿的柱塞以及固持凸緣的即用型塑料注射器,以進行注射。在一些實施方案中,在不使用針頭的情況下將本文公開的耳可接受的組合物或制劑遞送或注射至鼓膜的表面上或外聽道中。在一些實施方案中,使用注射器將本文公開的耳可接受的組合物或制劑遞送或注射至鼓膜的表面上或外聽道中。在一些實施方案中,使用滴管或能夠將所公開的耳可接受的組合物遞送至目標區域的任何遞送裝置,將本文公開的耳可接受的組合物或制劑遞送或注射至鼓膜的表面上或外聽道中。施用本文所述的含有耳用藥劑化合物的耳可接受的組合物或制劑以用于預防性和/或治療性治療。在治療性應用中,將耳用藥劑組合物以足以治愈或至少部分阻止疾病、病癥或病況的癥狀的量施用至已經患有病況或病癥的患者。對于該應用有效的量將取決于疾病、病癥或病況的嚴重程度和進程、既往治療、患者的健康狀況和對藥物的反應以及治療醫師的判斷。施用頻率在一些實施方案中,將本文公開的組合物施用至有需要的個體一次。在一些實施方案中,將本文公開的組合物施用至有需要的個體超過一次。在一些實施方案中,本文公開的組合物的第一次施用后接著是本文公開的組合物的第二次施用。在一些實施方案中,本文公開的組合物的第一次施用后接著是本文公開的組合物的第二次和第三次施用。在一些實施方案中,本文公開的組合物的第一次施用后接著是本文公開的組合物的第二次、第三次和第四次施用。在一些實施方案中,本文公開的組合物的第一次施用后接著是本文公開的組合物的第二次、第三次、第四次和第五次施用。在一些實施方案中,本文公開的組合物的第一次施用后接著是休藥期。向有需要的個體施用組合物的次數取決于醫務人員的判斷、病癥、病癥的嚴重程度和個體對制劑的反應。在一些實施方案中,將本文公開的組合物施用至患有輕度急性病況的有需要的個體一次。在一些實施方案中,將本文公開的組合物施用至患有中度或重度急性病況的有需要的個體超過一次。在患者的病況沒有改善的情況下,根據醫生的判斷,可長期地進行耳用藥劑的施用,即,持續延長的時間段,包括貫穿患者的整個生命期,以便改善或另外控制或限制患者的疾病或病況的癥狀。在患者的病況沒有改善的情況下,根據醫生的判斷,可長期地進行耳用藥劑化合物的施用,即,持續延長的時間段,包括貫穿患者的整個生命期,以便改善或另外控制或限制患者的疾病或病況的癥狀。在患者的狀況確實得到改善的情況下,根據醫生的判斷,可繼續給予耳用藥劑化合物的施用;或者,可將所施用的藥物的劑量暫時減少或暫時暫停某一時間長度(即“休藥期”)。休藥期的長度在2天與1年之間不等,僅舉例而言,包括2天、3天、4天、5天、6天、7天、10天、12天、15天、20天、28天、35天、50天、70天、100天、120天、150天、180天、200天、250天、280天、300天、320天、350天和365天。休藥期期間的劑量減少可為10%-100%,僅舉例而言,包括10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%和100%。一旦患者的耳部病況發生改善,則必要時施用耳用藥劑的維持劑量。隨后,任選地根據癥狀將施用的劑量或頻率或兩者降低至保持疾病、病癥或病況改善的水平。在某些實施方案中,一旦有任何癥狀復發,則患者需要長期的間歇治療。對應于這樣的量的耳用藥劑的量將根據諸如具體化合物、疾病病況及其嚴重程度等因素,根據關于該病例的具體情況而變化,這些具體情況包括例如所施用的具體耳用藥劑、給藥途徑、所治療的病況、所治療的目標區域和所治療的受試者或主體。然而,一般而言,用于成人治療的劑量通常將會在每次施用0.02-50mg的范圍內,優選每次施用1-15mg。所需劑量以單一劑量或作為同時(或在短時間段內)或以適當間隔施用的分開的劑量提供。在一些實施方案中,初始施用特定的耳用藥劑,隨后施用不同的制劑或耳用藥劑。控制釋放制劑的藥代動力學在一些實施方案中,本文公開的制劑另外提供了耳用藥劑從組合物中的立即釋放,或在1分鐘內,或在5分鐘內,或在10分鐘內,或在15分鐘內,或在30分鐘內,或在60分鐘內,或在90分鐘內釋放。在其他實施方案中,治療有效量的至少一種耳用藥劑從組合物中立即釋放,或在1分鐘內,或在5分鐘內,或在10分鐘內,或在15分鐘內,或在30分鐘內,或在60分鐘內,或在90分鐘內釋放。在某些實施方案中,該組合物包含提供至少一種耳用藥劑的立即釋放的耳藥物學上可接受的凝膠制劑。該制劑的其他實施方案還可包含增強本文包括的制劑的粘度的試劑。在其他或進一步的實施方案中,所述制劑提供了至少一種耳用藥劑的延長釋放制劑。在某些實施方案中,至少一種耳用藥劑從該制劑中的擴散發生持續超過5分鐘、或15分鐘、或30分鐘、或1小時、或4小時、或6小時、或12小時、或18小時、或1天、或2天、或3天、或4天、或5天、或6天、或7天、或10天、或12天、或14天、或18天、或21天、或25天、或30天、或45天、或2個月、或3個月、或4個月、或5個月、或6個月、或9個月或1年的時間段。在其他實施方案中,治療有效量的至少一種耳用藥劑從該制劑中釋放持續超過5分鐘、或15分鐘、或30分鐘、或1小時、或4小時、或6小時、或12小時、或18小時、或1天、或2天、或3天、或4天、或5天、或6天、或7天、或10天、或12天、或14天、或18天、或21天、或25天、或30天、或45天、或2個月、或3個月、或4個月、或5個月、或6個月、或9個月或1年的時間段。在其他實施方案中,所述制劑提供了耳用藥劑的立即釋放和延長釋放制劑。在其他實施方案中,該制劑含有0.25:1比例、或0.5:1比例、或1:1比例、或1:2比例、或1:3比例、或1:4比例、或1:5比例、或1:7比例、或1:10比例、或1:15比例或1:20比例的立即釋放和延長釋放制劑。在進一步的實施方案中,該制劑提供了第一耳用藥劑的立即釋放和第二耳用藥劑或其他治療劑的延長釋放。在其他實施方案中,該制劑提供了至少一種耳用藥劑和至少一種治療劑的立即釋放和延長釋放制劑。在一些實施方案中,該制劑分別提供了第一耳用藥劑和第二治療劑的0.25:1比例、或0.5:1比例、或1:1比例、或1:2比例、或1:3比例、或1:4比例、或1:5比例、或1:7比例、或1:10比例、或1:15比例或1:20比例的立即釋放和延長釋放制劑。在特定的實施方案中,所述制劑在治療部位(例如eac)提供治療有效量的至少一種耳用藥劑而基本沒有全身暴露。在另外的實施方案中,該制劑在治療部位提供治療有效量的至少一種耳用藥劑而基本沒有可檢測到的全身暴露。在其他實施方案中,該制劑在治療部位提供治療有效量的至少一種耳用藥劑而沒有或幾乎沒有可檢測到的全身暴露。可將立即釋放、延遲釋放和/或延長釋放耳用藥劑組合物或制劑的組合與其他藥劑以及本文公開的賦形劑、稀釋劑、穩定劑、張度劑和其他組分組合。這樣,根據所用的耳用藥劑、所需的稠度或粘度或者所選的遞送模式,相應地將本文公開的實施方案的替代方面與立即釋放、延遲釋放和/或延長釋放實施方案組合。在某些實施方案中,本文所述的耳用藥劑制劑的藥代動力學通過將該制劑注射至試驗動物(舉例而言,其包括豚鼠或毛絲鼠)的eac中或鼓膜表面上或鼓膜表面附近來確定。在確定的時間段(例如,6小時、12小時、1天、2天、3天、4天、5天、6天和7天,經1周的時間測試制劑的藥代動力學),對試驗動物施以安樂死并測量耳中或其他器官中的耳用藥劑的水平。此外,通過從試驗動物中抽取血樣來測量耳用藥劑的全身水平。為了確定該制劑是否妨礙聽力,任選地測試試驗動物的聽力。藥劑盒/制品本發明還提供了用于在哺乳動物中調節耵聹的產生以及治療耵聹分泌過多和耵聹分泌過多相關疾病的藥劑盒。此類藥劑盒通常將包含一種或多種本文公開的耳用藥劑控制釋放組合物,以及藥劑盒的使用說明。本發明還涉及一種或多種耳用藥劑控制釋放組合物在制備藥物中的用途,該藥物用于治療、緩和、減輕或改善患有、疑似患有耵聹分泌過多或處于發生耵聹分泌過多的風險下的哺乳動物(如人)的疾病、功能障礙或病癥的癥狀。在一些實施方案中,藥劑盒包含載體、包裝或容器,該容器被區室化以接納一個或多個容器如小瓶、管等等,每個容器包括一種將在本文所述的方法中使用的單獨的要素。合適的容器包括例如瓶子、小瓶、注射器和試管。在其他實施方案中,容器由多種材料如玻璃或塑料形成。本文提供的制品含有包裝材料。本文中還提出了用于包裝藥物產品的包裝材料。參見,例如,美國專利號5,323,907、5,052,558和5,033,252。藥物包裝材料的實例包括但不限于泡罩包裝、瓶子、管、吸入器、泵、袋、小瓶、容器、注射器、瓶子以及適于所選制劑和預期施用模式和治療的任何包裝材料。本文提供的很多種耳用藥劑制劑組合物預期作為多種針對將從耳用藥劑向eac的控制釋放施用獲益的任何疾病、病癥或病況的治療。在一些實施方案中,藥劑盒包含一個或多個附加容器,每個均具有從商業和用戶角度來看期望用于本文所述制劑的一種或多種不同的材料(如任選地為濃縮的形式的試劑和/或裝置)。此類材料的非限制性實例包括但不限于緩沖液、稀釋劑、過濾器、針頭、注射器;載體、包裝、容器、小瓶和/或列出內容物的管標簽和/或使用說明以及具有使用說明的包裝插頁。任選地包括一套說明書。在進一步的實施方案中,標簽位于容器上或與容器相關聯。在進一步的實施方案中,當構成標簽的字母、數字或其他字符附于、模塑于或刻蝕于容器自身中時,標簽位于容器上;當標簽存在于同樣容納容器的器皿或載體內時(例如,作為包裝插頁),標簽與容器相關聯。在其他實施方案中,標簽用于說明針對特定的治療應用要使用的內容物。在又一個實施方案中,標簽還說明該內容物例如在本文所述的方法中的使用指導。在某些實施方案中,藥物組合物存在于含有一個或多個單位劑型的包裝或分配器裝置中,該單位劑型含有本文提供的化合物。在另一個實施方案中,包裝例如含有金屬或塑料箔,如泡罩包裝。在進一步的實施方案中,包裝或分配器裝置伴隨有施用說明。在進一步的實施方案中,包裝或分配器還伴隨有與容器關聯的、由管控藥物的制造、使用或銷售的政府機構規定的形式的通知,該通知反映了藥物用于人類或獸醫施用的形式的機構批準。在另一個實施方案中,這樣的通知例如是由美國食品和藥品管理局針對處方藥批準的標簽,或批準的產品插頁。在又一個實施方案中,還制備了配制在相容的藥物載體中的、含有本文提供的化合物的組合物,該組合物放置在合適的容器中并貼有針對所示病況的治療的標簽。實施例實施例1用于制備熱可逆性凝膠耳用制劑的示例性組合物描述于表1-12中。表1.熱可逆性凝膠膽堿酯或氨基甲酸酯制劑表2.含有另外的活性劑的熱可逆性凝膠膽堿酯或氨基甲酸酯制劑表3.熱可逆性凝膠植物生物堿制劑表4.含有另外的活性劑的熱可逆性凝膠植物生物堿制劑表5.熱可逆性凝膠可逆性膽堿酯酶抑制劑制劑表6.含有另外的活性劑的熱可逆性凝膠可逆性膽堿酯酶抑制劑制劑表7.熱可逆性凝膠乙酰膽堿釋放促進劑制劑表8.含有另外的活性劑的熱可逆性凝膠乙酰膽堿釋放促進劑制劑表9.熱可逆性凝膠抗腎上腺素能藥制劑表10.含有另外的活性劑的熱可逆性凝膠抗腎上腺素能藥制劑表11.熱可逆性凝膠擬交感神經藥制劑表12.含有另外的活性劑的熱可逆性凝膠擬交感神經藥制劑實施例2-含有膽堿酯或氨基甲酸酯的熱可逆性凝膠制劑的制備成分量(mg/g制劑)膽堿酯或氨基甲酸酯60.0nacl100.0泊洛沙姆407160.0trishcl緩沖液(0.1m)680.0通過將1.60g泊洛沙姆407(basfcorp.)懸浮于5.00gtrishcl緩沖液(0.1m)中制備含有6.0%膽堿酯或氨基甲酸酯(例如乙酰膽堿或卡巴膽堿)的10-g批凝膠制劑,并在4℃下攪拌過夜的情況下將組分混合以確保完全溶解。添加膽堿酯或氨基甲酸酯(例如乙酰膽堿或卡巴膽堿)(600.0mg)、nacl(1g)和另外的trishcl緩沖液(0.1m)(1.80g),并將其進一步攪拌直至觀察到完全溶解。將混合物保持在低于室溫的溫度下直至使用。含有膽堿酯或氨基甲酸酯的熱可逆性凝膠制劑的制備成分量(mg/g制劑)膽堿酯或氨基甲酸酯60.0角鯊烯60.0羊毛甾醇60.0膽固醇60.0nacl100.0泊洛沙姆407160.0trishcl緩沖液(0.1m)500.0通過將1.60g泊洛沙姆407(basfcorp.)懸浮于4.00gtrishcl緩沖液(0.1m)中制備含有6.0%膽堿酯或氨基甲酸酯(例如乙酰膽堿或卡巴膽堿)的10-g批凝膠制劑,并在4℃下攪拌過夜的情況下將組分混合以確保完全溶解。添加膽堿酯或氨基甲酸酯(例如乙酰膽堿或卡巴膽堿)(600.0mg)、角鯊烯(600.0mg)、羊毛甾醇(600.0mg)、膽固醇(600.0mg)、nacl(1g)和另外的trishcl緩沖液(0.1m)(100mg),并將其進一步攪拌直至觀察到完全溶解。將混合物保持在低于室溫的溫度下直至使用。實施例3-含有植物生物堿的熱可逆性凝膠制劑的制備成分量(mg/g制劑)植物生物堿60.0nacl100.0泊洛沙姆407160.0trishcl緩沖液(0.1m)680.0通過將1.60g泊洛沙姆407(basfcorp.)懸浮于5.00gtrishcl緩沖液(0.1m)中制備含有6.0%植物生物堿(例如毛果蕓香堿)的10-g批凝膠制劑,并在4℃下攪拌過夜的情況下將組分混合以確保完全溶解。添加植物生物堿(例如毛果蕓香堿)(600.0mg)、nacl(1g)和另外的trishcl緩沖液(0.1m)(1.80g),并將其進一步攪拌直至觀察到完全溶解。將混合物保持在低于室溫的溫度下直至使用。含有植物生物堿的熱可逆性凝膠制劑的制備成分量(mg/g制劑)植物生物堿60.0角鯊烯60.0羊毛甾醇60.0膽固醇60.0nacl100.0泊洛沙姆407160.0trishcl緩沖液(0.1m)500.0通過將1.60g泊洛沙姆407(basfcorp.)懸浮于4.00gtrishcl緩沖液(0.1m)中制備含有6.0%植物生物堿(例如毛果蕓香堿)的10-g批凝膠制劑,并在4℃下攪拌過夜的情況下將組分混合以確保完全溶解。添加植物生物堿(例如毛果蕓香堿)(600.0mg)、角鯊烯(600.0mg)、羊毛甾醇(600.0mg)、膽固醇(600.0mg)、nacl(1g)和另外的trishcl緩沖液(0.1m)(100mg),并將其進一步攪拌直至觀察到完全溶解。將混合物保持在低于室溫的溫度下直至使用。實施例4-含有膽堿酯酶抑制劑的熱可逆性凝膠制劑的制備成分量(mg/g制劑)可逆性膽堿酯酶抑制劑60.0nacl100.0泊洛沙姆407160.0trishcl緩沖液(0.1m)680.0通過將1.60g泊洛沙姆407(basfcorp.)懸浮于5.00gtrishcl緩沖液(0.1m)中制備含有6.0%可逆性膽堿酯酶抑制劑(例如新斯的明或毒扁豆堿)的10-g批凝膠制劑,并在4℃下攪拌過夜的情況下將組分混合以確保完全溶解。添加可逆性膽堿酯酶抑制劑(例如新斯的明或毒扁豆堿)(600.0mg)、nacl(1g)和另外的trishcl緩沖液(0.1m)(1.80g),并將其進一步攪拌直至觀察到完全溶解。將混合物保持在低于室溫的溫度下直至使用。含有膽堿酯酶抑制劑的熱可逆性凝膠制劑的制備成分量(mg/g制劑)可逆性膽堿酯酶抑制劑60.0角鯊烯60.0羊毛甾醇60.0膽固醇60.0nacl100.0泊洛沙姆407160.0trishcl緩沖液(0.1m)500.0通過將1.60g泊洛沙姆407(basfcorp.)懸浮于4.00gtrishcl緩沖液(0.1m)中制備含有6.0%可逆性膽堿酯酶抑制劑(例如新斯的明或毒扁豆堿)的10-g批凝膠制劑,并在4℃下攪拌過夜的情況下將組分混合以確保完全溶解。添加可逆性膽堿酯酶抑制劑(例如新斯的明或毒扁豆堿)(600.0mg)、角鯊烯(600.0mg)、羊毛甾醇(600.0mg)、膽固醇(600.0mg)、nacl(1g)和另外的trishcl緩沖液(0.1m)(100mg),并將其進一步攪拌直至觀察到完全溶解。將混合物保持在低于室溫的溫度下直至使用。實施例5-含有乙酰膽堿釋放促進劑的熱可逆性凝膠制劑的制備成分量(mg/g制劑)乙酰膽堿釋放促進劑60.0nacl100.0泊洛沙姆407160.0trishcl緩沖液(0.1m)680.0通過將1.60g泊洛沙姆407(basfcorp.)懸浮于5.00gtrishcl緩沖液(0.1m)中制備含有6.0%乙酰膽堿釋放促進劑(例如氟哌利多、利培酮或曲唑酮)的10-g批凝膠制劑,并在4℃下攪拌過夜的情況下將組分混合以確保完全溶解。添加乙酰膽堿釋放促進劑(例如氟哌利多、利培酮或曲唑酮)(600.0mg)、nacl(1g)和另外的trishcl緩沖液(0.1m)(1.80g),并將其進一步攪拌直至觀察到完全溶解。將混合物保持在低于室溫的溫度下直至使用。含有乙酰膽堿釋放促進劑的熱可逆性凝膠制劑的制備通過將1.60g泊洛沙姆407(basfcorp.)懸浮于4.00gtrishcl緩沖液(0.1m)中制備含有6.0%乙酰膽堿釋放促進劑(例如氟哌利多、利培酮或曲唑酮)的10-g批凝膠制劑,并在4℃下攪拌過夜的情況下將組分混合以確保完全溶解。添加乙酰膽堿釋放促進劑(例如氟哌利多、利培酮或曲唑酮)(600.0mg)、角鯊烯(600.0mg)、羊毛甾醇(600.0mg)、膽固醇(600.0mg)、nacl(1g)和另外的trishcl緩沖液(0.1m)(100mg),并將其進一步攪拌直至觀察到完全溶解。將混合物保持在低于室溫的溫度下直至使用。實施例6-含有抗腎上腺素能藥的熱可逆性凝膠制劑的制備成分量(mg/g制劑)抗腎上腺素能藥60.0nacl100.0泊洛沙姆407160.0trishcl緩沖液(0.1m)680.0通過將1.60g泊洛沙姆407(basfcorp.)懸浮于5.00gtrishcl緩沖液(0.1m)中制備含有6.0%抗腎上腺素能藥(例如可樂定、普萘洛爾、阿替洛爾或哌唑嗪)的10-g批凝膠制劑,并在4℃下攪拌過夜的情況下將組分混合以確保完全溶解。添加抗腎上腺素能藥(例如可樂定、普萘洛爾、阿替洛爾或哌唑嗪)(600.0mg)、nacl(1g)和另外的trishcl緩沖液(0.1m)(1.80g),并將其進一步攪拌直至觀察到完全溶解。將混合物保持在低于室溫的溫度下直至使用。含有抗腎上腺素能藥的熱可逆性凝膠制劑的制備成分量(mg/g制劑)抗腎上腺素能藥60.0角鯊烯60.0羊毛甾醇60.0膽固醇60.0nacl100.0泊洛沙姆407160.0trishcl緩沖液(0.1m)500.0通過將1.60g泊洛沙姆407(basfcorp.)懸浮于4.00gtrishcl緩沖液(0.1m)中制備含有6.0%抗腎上腺素能藥(例如可樂定、普萘洛爾、阿替洛爾或哌唑嗪)的10-g批凝膠制劑,并在4℃下攪拌過夜的情況下將組分混合以確保完全溶解。添加抗腎上腺素能藥(例如可樂定、普萘洛爾、阿替洛爾或哌唑嗪)(600.0mg)、角鯊烯(600.0mg)、羊毛甾醇(600.0mg)、膽固醇(600.0mg)、nacl(1g)和另外的trishcl緩沖液(0.1m)(100mg),并將其進一步攪拌直至觀察到完全溶解。將混合物保持在低于室溫的溫度下直至使用。實施例7-含有擬交感神經藥的熱可逆性凝膠制劑的制備成分量(mg/g制劑)擬交感神經藥60.0nacl100.0泊洛沙姆407160.0trishcl緩沖液(0.1m)680.0通過將1.60g泊洛沙姆407(basfcorp.)懸浮于5.00gtrishcl緩沖液(0.1m)中制備含有6.0%擬交感神經藥(例如去甲腎上腺素或多巴胺)的10-g批凝膠制劑,并在4℃下攪拌過夜的情況下將組分混合以確保完全溶解。添加擬交感神經藥(例如去甲腎上腺素或多巴胺)(600.0mg)、nacl(1g)和另外的trishcl緩沖液(0.1m)(1.80g),并將其進一步攪拌直至觀察到完全溶解。將混合物保持在低于室溫的溫度下直至使用。含有擬交感神經藥的熱可逆性凝膠制劑的制備成分量(mg/g制劑)擬交感神經藥60.0角鯊烯60.0羊毛甾醇60.0膽固醇60.0nacl100.0泊洛沙姆407160.0trishcl緩沖液(0.1m)500.0通過將1.60g泊洛沙姆407(basfcorp.)懸浮于4.00gtrishcl緩沖液(0.1m)中制備含有6.0%擬交感神經藥(例如去甲腎上腺素或多巴胺)的10-g批凝膠制劑,并在4℃下攪拌過夜的情況下將組分混合以確保完全溶解。添加擬交感神經藥(例如去甲腎上腺素或多巴胺)(600.0mg)、角鯊烯(600.0mg)、羊毛甾醇(600.0mg)、膽固醇(600.0mg)、nacl(1g)和另外的trishcl緩沖液(0.1m)(100mg),并將其進一步攪拌直至觀察到完全溶解。將混合物保持在低于室溫的溫度下直至使用。實施例8-包含微粒化膽堿酯或氨基甲酸酯粉末和微粒化地塞米松粉末的熱可逆性凝膠組合物的制備制備含有2.0%微粒化膽堿酯或氨基甲酸酯(例如乙酰膽堿或卡巴膽堿)和微粒化地塞米松的10-g批凝膠制劑。用8.2g無菌過濾的去離子水溶解微粒化膽堿酯或氨基甲酸酯(例如乙酰膽堿或卡巴膽堿)、微粒化地塞米松、13.8mg磷酸氫二鈉二水合物usp(fisherscientific.)+3.1mg磷酸二氫鈉一水合物usp(fisherscientific.)+74mg氯化鈉usp(fisherscientific.),并用1mnaoh將ph調節至7.4。將緩沖溶液冷卻,并在混合的同時將1.6g泊洛沙姆407(basfcorp.,含有約100ppm的bht)灑到冷卻的pbs溶液中。將溶液混合直至全部泊洛沙姆均溶解。使用33mmpvdf0.22μm無菌注射器過濾器(milliporecorp.)將泊洛沙姆無菌過濾并在無菌環境中遞送至2ml無菌玻璃小瓶(wheaton),用無菌丁基橡膠塞(kimble)將小瓶封閉,并用13mm鋁封(kimble)卷曲密封。將20mg微粒化膽堿酯或氨基甲酸酯(例如乙酰膽堿或卡巴膽堿)和地塞米松置于單獨的干凈的去熱原小瓶中,將小瓶用無菌丁基橡膠塞(kimble)封閉并用13mm鋁封(kimble)卷曲密封,將小瓶在140℃下干熱滅菌(fisherscientificisotemp烘箱)7小時。在對于本文所述的實驗施用之前,使用附接至1ml無菌注射器(bectondickinson)的21g針頭(bectondickinson)將1ml的冷泊洛沙姆溶液遞送至含有20mg無菌微粒化膽堿酯或氨基甲酸酯(例如乙酰膽堿或卡巴膽堿)和地塞米松的小瓶中,通過搖動將懸浮液充分混合以確保懸浮液的均勻性。隨后用21g注射器抽取懸浮液,并將針頭轉換為用于施用的27g針頭。包含微粒化膽堿酯或氨基甲酸酯粉末、微粒化地塞米松粉末和另外的活性劑粉末的熱可逆性凝膠組合物的制備制備含有2.0%微粒化膽堿酯或氨基甲酸酯(例如乙酰膽堿或卡巴膽堿)、微粒化地塞米松、微粒化角鯊烯、微粒化羊毛甾醇、微粒化膽固醇的10-g批凝膠制劑。用8.2g無菌過濾的去離子水溶解微粒化膽堿酯或氨基甲酸酯(例如乙酰膽堿或卡巴膽堿)、微粒化地塞米松、微粒化角鯊烯、微粒化羊毛甾醇、微粒化膽固醇、13.8mg磷酸氫二鈉二水合物usp(fisherscientific.)+3.1mg磷酸二氫鈉一水合物usp(fisherscientific.)+74mg氯化鈉usp(fisherscientific.),并用1mnaoh將ph調節至7.4。將緩沖溶液冷卻,并在混合的同時將1.6g泊洛沙姆407(basfcorp.,含有約100ppm的bht)灑到冷卻的pbs溶液中。將溶液混合直至全部泊洛沙姆均溶解。使用33mmpvdf0.22μm無菌注射器過濾器(milliporecorp.)將泊洛沙姆無菌過濾并在無菌環境中遞送至2ml無菌玻璃小瓶(wheaton),用無菌丁基橡膠塞(kimble)將小瓶封閉,并用13mm鋁封(kimble)卷曲密封。將20mg微粒化膽堿酯或氨基甲酸酯(例如乙酰膽堿或卡巴膽堿)、地塞米松、角鯊烯、羊毛甾醇和膽固醇置于單獨的干凈的去熱原小瓶中,將小瓶用無菌丁基橡膠塞(kimble)封閉并用13mm鋁封(kimble)卷曲密封,將小瓶在140℃下干熱滅菌(fisherscientificisotemp烘箱)7小時。在對于本文所述的實驗施用之前,使用附接至1ml無菌注射器(bectondickinson)的21g針頭(bectondickinson)將1ml的冷泊洛沙姆溶液遞送至含有20mg無菌微粒化膽堿酯或氨基甲酸酯(例如乙酰膽堿或卡巴膽堿)、地塞米松、角鯊烯、羊毛甾醇和膽固醇的小瓶中,通過搖動將懸浮液充分混合以確保懸浮液的均勻性。隨后用21g注射器抽取懸浮液,并將針頭轉換為用于施用的27g針頭。實施例17-ph對高壓滅菌的pbs緩沖液中16%泊洛沙姆407/2%耳用藥劑的降解產物的影響通過用79.3g無菌過濾的去離子水溶解351.4mg氯化鈉(fisherscientific)、302.1mg無水磷酸氫二鈉(fisherscientific)、122.1mg無水磷酸二氫鈉(fisherscientific)和適量的耳用藥劑來制備16%泊洛沙姆407/2%耳用藥劑的儲備溶液。將溶液在冰冷水浴中冷卻,隨后在混合的同時將16.05g泊洛沙姆407灑到該冷溶液中。將混合物進一步混合直至泊洛沙姆完全溶解。測量該溶液的ph。ph為5.3的pbs中的16%泊洛沙姆407/2%耳用藥劑。取上述溶液的等分試樣(約30ml),并通過添加1mhcl調節ph至5.3。ph為8.0的pbs中的16%泊洛沙姆407/2%耳用藥劑。取上述儲備溶液的等分試樣(約30ml),并通過添加1mnaoh調節ph至8.0。通過用無菌過濾的去離子水溶解805.5mg氯化鈉(fisherscientific)、606mg無水磷酸氫二鈉(fisherscientific)、247mg無水磷酸二氫鈉(fisherscientific),隨后適量(qs)加至200g來制備pbs緩沖液(ph7.3)。通過將適量的耳用藥劑溶解于pbs緩沖液中并用適量pbs緩沖液加至10g來制備pbs(ph7.3)中的2%耳用藥劑溶液。將1ml樣品單獨地置于3ml螺旋蓋玻璃小瓶(帶有橡膠襯里)中并緊閉。將小瓶置于marketforge-sterilmatic高壓滅菌器(設置,緩慢液體)中,并在250°f下滅菌15分鐘。高壓滅菌后,使樣品冷卻至室溫并隨后置于冰箱中。通過在冷卻的同時混合小瓶來使樣品均勻化。觀察并記錄外觀(例如,變色和/或沉淀)。利用裝備有lunac18(2)3μm,250x4.6mm柱的agilent1200,使用30-80乙腈梯度(1-10min)(含有0.05%tfa的水-乙腈混合物)進行hplc分析,總共運行15分鐘。通過取30μl樣品并用1.5ml的1:1乙腈水混合物溶解來稀釋樣品。記錄高壓滅菌的樣品中耳用藥劑的純度。使用上述程序測試根據上述程序制備的包含耳用藥劑和/或eac保護劑的制劑,以確定ph對高壓滅菌步驟中降解的影響。實施例18-緩沖液類型對含有泊洛沙姆407的制劑在熱滅菌(高壓滅菌)之后的降解產物的影響。通過用無菌過濾的去離子水溶解377.8mg氯化鈉(fisherscientific)和602.9mg氨丁三醇(sigmachemicalco.),隨后適量加至100g來制備tris緩沖液,用1mhcl將ph調節至7.4。含有在tris緩沖液中的25%泊洛沙姆407溶液的儲備溶液:稱取45gtris緩沖液,在冰冷的浴中冷卻,隨后在混合的同時將15g泊洛沙姆407(spectrumchemicals)灑入該緩沖液中。將該混合物進一步混合直至全部泊洛沙姆完全溶解。用上述儲備溶液制備一系列制劑。將適量的耳用藥劑(或其鹽或前藥)和/或呈微粒化/包覆/脂質體顆粒的耳用藥劑(或其鹽或前藥)用于所有實驗。含有在pbs緩沖液中的25%泊洛沙姆407溶液的儲備溶液(ph7.3):使用上述pbs緩沖液。用140.4g無菌過濾的去離子水溶解704mg氯化鈉(fisherscientific)、601.2mg無水磷酸氫二鈉(fisherscientific)、242.7mg無水磷酸二氫鈉(fisherscientific)。將溶液在冰冷的水浴中冷卻,隨后在混合的同時將50g泊洛沙姆407灑入該冷溶液中。將混合物進一步混合直至泊洛沙姆完全溶解。用上述儲備溶液制備一系列制劑。將適量的耳用藥劑(或其鹽或前藥)和/或呈微粒化/包覆/脂質體顆粒的耳用藥劑(或其鹽或前藥)用于所有實驗。表13和表14列出了使用上述程序制備的樣品。將適量的耳用藥劑添加至各樣品中,以提供樣品中2%耳用藥劑的最終濃度。表13.含有tris緩沖液的樣品的制備表14.含有pbs緩沖液(ph7.3)的樣品的制備將1ml樣品單獨地置于3ml螺旋蓋玻璃小瓶(帶有橡膠襯里)中并緊閉。將小瓶置于marketforge-sterilmatic高壓滅菌器(設置,緩慢液體)中,并在250°f下滅菌25分鐘。高壓滅菌后,使樣品冷卻至室溫。將小瓶置于冰箱中并在冷卻的同時進行混合以使樣品均勻化。利用裝備有lunac18(2)3μm,250x4.6mm柱的agilent1200,使用30-80乙腈梯度(1-10min)(含有0.05%tfa的水-乙腈混合物)進行hplc分析,總共運行15分鐘。通過取30μl樣品并用1.5ml的1:1乙腈水混合物溶解來稀釋樣品。記錄高壓滅菌的樣品中耳用藥劑的純度。比較tris和pbs緩沖液中制劑的穩定性。使用具有以0.08rpm(剪切速率為0.31s-1)旋轉的cpe-51主軸、裝備有水夾套溫度控制單元(溫度以1.6℃/min從15℃上升至34℃)的brookfield粘度計rvdv-ii+p進行粘度測量。t膠凝被定義為由于溶膠-凝膠轉變而發生粘度增加時曲線的拐點。僅分析在高壓滅菌后沒有顯示變化的制劑。使用以上程序測試根據本文所述程序制備的包含耳用藥劑和/或eac保護劑的制劑,以確定二級聚合物的添加對含有2%活性劑和17%泊洛沙姆407的制劑在熱滅菌(高壓滅菌)后的降解產物和粘度的影響。將含有微粒化耳用藥劑的制劑的穩定性與非微粒化耳用藥劑制劑的對應物進行比較。實施例19-釋放曲線的體外比較。在37℃下在snapwell(孔徑為0.4μm的6.5mm直徑的聚碳酸酯膜)中進行溶出,將0.2ml本文所述的凝膠制劑置于snapwell中并使之硬化,隨后將0.5ml緩沖液置于儲器中并使用labline軌道搖床在70rpm下搖動。每小時采集樣品(抽取0.1ml并用溫緩沖液代替)。根據外部校準標準曲線,通過245nm處的uv來分析樣品的耳用藥劑濃度。使用硫氰酸鈷方法在624nm下分析普朗尼克(pluronic)濃度。測定作為%p407的函數的平均溶出時間(mdt)的相對排序。制劑平均溶出時間(mdt)與p407濃度之間的線性關系表明耳用藥劑由于聚合物凝膠(泊洛沙姆)的蝕解而釋放,而不是通過擴散來釋放。非線性關系表明耳用藥劑通過擴散和/或聚合物凝膠降解的組合而釋放。或者,使用lixin-yu的論文[actapharmaceuticasinica2008,43(2):208-203]描述的方法來分析樣品,并且測定作為%p407的函數的平均溶出時間(mdt)的排序。使用以上程序測試根據本文所述程序制備的包含耳用藥劑和/或eac保護劑的制劑,以測定耳用藥劑的釋放曲線。實施例20-關于無菌過濾的溫度范圍的確定測量低溫下的粘度以幫助認識到需要進行無菌過濾以降低堵塞的可能性的溫度范圍。使用具有以1、5和10rpm(剪切速率為7.5、37.5和75s-1)旋轉的cpe-40主軸、裝備有水夾套溫度控制單元(溫度以1.6℃/min從10℃上升至25℃)的brookfield粘度計rvdv-ii+p進行粘度測量。隨著耳用藥劑濃度的增加測定16%普朗尼克p407的t膠凝。16%普朗尼克制劑的t膠凝的增加由下式估算:δt膠凝=0.93[耳用藥劑%]使用以上程序測試根據本文所述程序制備的包含耳用藥劑和/或eac保護劑的制劑,以確定關于無菌過濾的溫度范圍。記錄增加量的耳用藥劑的添加對制劑的t膠凝以及表觀粘度的影響。實施例21-制備條件的確定表17.制備/過濾條件下可能的制劑的粘度a:37.5s-1的剪切速率下測得的粘度制備8升批的16%p407安慰劑以評價制備/過濾條件。通過將6.4升去離子水置于3加侖ss壓力容器中來制備安慰劑,并使安慰劑在冰箱中冷卻過夜。第二天早上取出罐(水溫5℃,室溫18℃),并添加48g氯化鈉、29.6g脫水磷酸氫二鈉和10g磷酸二氫鈉一水合物,并用頂置式混合器(ikarw20,在1720rpm下)溶解。半小時后,一旦緩沖液溶解(溶液溫度8℃,室溫18℃),將1.36kg泊洛沙姆407以15分鐘的間隔緩慢地灑到緩沖溶液中(溶液溫度12℃,室溫18℃),隨后將速度增加至2430rpm。混合另一個小時后,將混合速度降至1062rpm(完全溶解)。將室溫維持在低于25℃以保持溶液的溫度低于19℃。將溶液的溫度維持在低于19℃直至制備開始后的3小時,而不需要冷凍/冷卻其容器。以20psi和14℃的溶液評價具有17.3cm2表面積的三種不同sartoscale(sartoriusstedim)過濾器1)sartopore2,0.2μm5445307hs-ff(pes),流速為16ml/min2)sartobranp,0.2μm5235307hs-ff(纖維素酯),流速為12ml/min3)sartopore2xli,0.2μm5445307is-ff(pes),流速為15ml/min使用sartopore2過濾器5441307h4-ss,在16psi的壓力下使用具有0.015m2表面積的0.45、0.2μmsartopore2150無菌膠囊(sartoriusstedim)在溶液溫度下進行過濾。在16psi下測量流速大約100ml/min,在溫度維持在6.5-14℃范圍內時流速沒有變化。壓力減小和溶液溫度升高導致流速由于溶液粘度的增加而降低。在該過程中監測溶液的變色。表18.在16psi的壓力下使用sartopore2,0.2μm過濾器在6.5-14℃的溶液溫度范圍下16%泊洛沙姆407安慰劑的預測過濾時間在過濾評價前檢查粘度、t膠凝和uv/vis吸收。通過evolution160uv/vis(thermoscientific)獲得普朗尼克uv/vis光譜。250-300nm范圍內的峰歸因于存在于原料(泊洛沙姆)中的bht穩定劑。表19列出了過濾前后上述溶液的物理化學性質。表19.過濾前后16%泊洛沙姆407安慰劑溶液的物理化學性質樣品t膠凝(℃)19℃時的粘度a(cp)274nm處的吸光度過濾前221000.3181過濾后221000.3081a在37.5s-1的剪切速率下測得的粘度上述過程適用于16%的p407制劑的制備,并且包括室內條件的溫度分析。優選地,19℃的最大溫度降低了制備期間冷卻容器的成本。在一些情況下,使用夾套容器進一步控制溶液的溫度以緩解制備問題。實施例22-耳用藥劑從高壓滅菌的微粒化樣品中的體外釋放tris緩沖液中的16%泊洛沙姆407/1.5%耳用藥劑:將250.8mg氯化鈉(fisherscientific)和302.4mg氨丁三醇(sigmachemicalco.)溶解于39.3g無菌過濾的去離子水中,用1mhcl將ph調節至7.4。使用4.9g的上述溶液,并使適量的微粒化耳用藥劑懸浮且分散良好。將2ml制劑轉移到2ml玻璃小瓶(wheaton血清玻璃小瓶)中,并用13mm丁基苯乙烯(kimble塞子)密封并用13mm鋁封卷曲密封。將小瓶置于marketforge-sterilmatic高壓滅菌器(設置,緩慢液體)中,并在250°f下滅菌25分鐘。高壓滅菌后,使樣品冷卻至室溫。將小瓶置于冰箱中并在冷卻的同時進行混合以使樣品均勻化。記錄高壓滅菌后的樣品變色或沉淀。在37℃下在snapwell(孔徑為0.4μm的6.5mm直徑的聚碳酸酯膜)中進行溶出,將0.2ml凝膠置于snapwell中并使之硬化,隨后將0.5mlpbs緩沖液置于儲器中并使用labline軌道搖床在70rpm下搖動。每小時采集樣品[抽取0.1ml并用含有2%peg-40氫化蓖麻油(basf)的溫pbs緩沖液代替,以提高耳用藥劑溶解度]。根據外部校準標準曲線,通過245nm處的uv來分析樣品的耳用藥劑濃度。將釋放速率與本文公開的其他制劑進行比較。計算各樣品的mdt時間。通過在使用eppendorf離心機5424將樣品在15,000rpm下離心10分鐘后測量上清液中耳用藥劑的濃度來評估耳用藥劑在16%泊洛沙姆體系中的溶出。根據外部校準標準曲線,通過245nm處的uv來測量上清液中的耳用藥劑濃度。使用上述程序測試根據本文所述程序制備的包含耳用藥劑和/或eac保護劑的制劑,以測定耳用藥劑從每種制劑中的釋放速率。實施例23-泊洛沙姆濃度和耳用藥劑濃度對釋放動力學的影響使用上述程序制備一系列包含不同濃度的膠凝劑和微粒化耳用藥劑的組合物。使用上述程序測定表20中各組合物的平均溶出時間(mdt)。表20.泊洛沙姆/耳用藥劑組合物的制備樣品ph15.5%p407/1.5%耳用藥劑/pbs7.416%p407/1.5%耳用藥劑/pbs7.417%p407/1.5%耳用藥劑/pbs7.415.5%p407/4.5%耳用藥劑/pbs7.416%p407/4.5%耳用藥劑/pbs7.417%p407/4.5%耳用藥劑/pbs7.4通過測量泊洛沙姆的mdt和測量耳用藥劑的mdt來確定凝膠強度和耳用藥劑濃度對耳用藥劑從組合物中的釋放動力學的影響。如上所述測量各組合物的表觀粘度。上述組合物中約15.5%的熱可逆性聚合物凝膠濃度提供了約270,000cp的表觀粘度。上述組合物中約16%的熱可逆性聚合物凝膠濃度提供了約360,000cp的表觀粘度。上述組合物中約16%的熱可逆性聚合物凝膠濃度提供了約480,000cp的表觀粘度。使用上述程序測試根據上述程序制備的包含耳用藥劑和/或eac保護劑的組合物,以測定耳用藥劑從各組合物中的釋放速率。實施例24-耳用藥劑制劑在豚鼠中的體內測試向一組豚鼠(charlesriver,體重為200-300g的雌性)注射含有0至50%耳用藥劑的50μl本文所述的不同p407-耳用藥劑制劑。測定每種制劑的凝膠消除時程。制劑的凝膠消除時程越短表明平均停留時間(mrt)越短。因此,測試制劑中耳用藥劑的注射體積和濃度以確定臨床前和臨床研究的最優參數。實施例25-體內延長釋放動力學向一組21只豚鼠(charlesriver,體重為200-300g的雌性)注射以280mosm/kg緩沖且按制劑的重量計含有0.1%至35%耳用藥劑的50μl16%p407制劑。在第1天對動物給藥。基于eac的分析來確定制劑的釋放曲線。實施例26-耳用制劑在耵聹分泌過多患者中的臨床試驗研究目的此研究的主要目的將是評估本文公開的耳用制劑與安慰劑相比,在改善患病患者的耵聹分泌過多癥狀中的安全性和功效。方法研究設計這將是一項3期、多中心、雙盲、隨機化、具有安慰劑對照的三組研究,在耵聹分泌過多癥狀的治療方面比較本文公開的耳用制劑(100mg和200mg)和安慰劑。約150名受試者將參加此研究,并且基于主辦方準備的隨機化序列將他們隨機分配(1:1)至三個治療組之一。每個組將接受200mg控制釋放耳用制劑、400mg控制釋放耳用制劑或控制釋放安慰劑制劑。在1周的基線期后,將來自每組的患者隨機分配至16周的雙治療期(8周治療,隨后8周維持期)。采用與基線測量值相比,治療后的耵聹分泌過多癥狀(包括眩暈、聽力損失、耳鳴和耳痛發生率)的頻率和強度的變化百分比來衡量主要功效。此外,每次測量都伴隨著使用標準檢查程序對eac的目視檢查。雖然本文已示出并描述了本發明的優選實施方案,但這些實施方案僅以示例的方式提供。在實施本發明時,可任選地采用本文所述的實施方案的各種替代方案。意在以下述權利要求限定本發明的范圍,并由此涵蓋這些權利要求范圍內的方法和結構及其等同項。當前第1頁12
相關技術
網友詢問留言
已有0條留言
- 還沒有人留言評論。精彩留言會獲得點贊!
1