鼠李糖乳桿菌促進生態失調后腸道菌群多樣性恢復的應用的制作方法
本發明涉及益生菌領域。具體地,本發明與鼠李糖乳桿菌(Lactobacillus rhamnosus)在受試者中維持和增加腸道菌群多樣性中的應用有關。
背景技術:
根據聯合國糧食及農業組織/世界衛生組織(FAO/WHO)中對具有活乳酸菌的奶粉的健康和營養特性的專家評議會在2001年批準的定義,益生菌是“活的微生物,該活的微生物當以恰當的量施用時,賦予了宿主健康益處”。已在屬于乳品工業中常用的乳桿菌屬(Lactobacillus)、雙歧桿菌屬(Bifidobacterium)、鏈球菌屬(Streptococcus)和乳球菌屬(Lactococcus)的物種中,描述了益生菌。據認為,益生菌通過阻礙致病微生物的生長和/或通過更直接地作用于免疫系統,在腸道菌群的水平上進行干預。
導致醫療保健相關感染(HAI)的機會細菌感染對患者死亡率和發病率,以及發達國家和發展中國家的醫療保健成本造成了深遠影響(WHO,2008)。胃腸道(GIT)是機會致病菌的貯主,其中機會致病菌受益于腸道菌群平衡的破壞或生態失調而侵入和感染易感患者。具體地,抗生素治療對腸道菌群的多樣性產生有害影響,并且抗生素治療促進了人的細菌性機會致病菌(包括糞腸球菌(Enterococcus faecalis),屎腸球菌(Enterococcus faecium)或艱難梭菌(Clostridium difficile))的擴增。
在獲得抗生素耐性和其他致病性狀后,植入和/或侵入的多重耐藥性糞腸球菌(E.faecalis)菌系(其導致嚴重的院內感染)被分類為7種醫院適應(hospital-adapted)的復合體,這7種醫院適應的復合體被命名為高風險腸道球菌克隆復合體(HiRECC)。HiRECC在GIT內的增殖和持久生存是產生耐萬古霉素性腸球菌(VRE)感染的主要風險,從而非常需要更好地了解糞腸球菌(E.faecalis)定植在GIT中所涉及的生物因素和生化因素。在美國和幾個歐洲國家中,屬于HiRECC-2的菌系是糞腸球菌(E.faecalis)感染的最常見病因之一。
從上文清楚的是,需要用于治療或預防糞腸球菌(E.faecalis)感染的抗生素的替代物或補充物。
“腸道菌群”是指居于隸屬動物界的任何生物體(人、動物、昆蟲等)的腸內的微生物群落。雖然每個個體具有獨特的菌群組成(來自總共400至500個不同細菌種類/個體的50%以上的取樣群落中,60至80種的細菌是相同的),但是它總是實現類似的主要生理功能,并且對個體健康具有直接影響:
·有助于消化胃和小腸不能消化的某些食物(主要是非消化性纖維);
·有助于產生一些維生素(B和K);
·保護免受其他微生物的侵襲,維持腸粘膜的完整性;
·在適當免疫系統的發育中發揮重要作用;
·健康、多樣且平衡的腸道菌群是確保適當腸道功能的關鍵。
考慮到腸道菌群在身體正常功能中發揮的主要作用及其所完成的不同功能,有時認為腸道菌群是“器官”。然而它是“獲得性”器官,因為嬰兒出生時是無菌的;也即,腸道定植始于出生,之后逐漸形成。
腸道菌群在擾動(諸如,飲食變化、抗生素治療和外源微生物的侵入)之后出現紊亂的幅度,以及恢復到擾動前狀態的速度和程度被限定為“菌群的恢復力”。菌群的恢復力在個體間以及個體內不同擾動之間是有差異的。
從上文可知,還非常需要用于提高菌群恢復力的治療。
越來越多的證據表明,益生菌或糞菌移植預防或治療包括腸道感染的許多疾病。這樣的方法也與小鼠中的腸道VRE的較高清除率相關。
令人驚奇地是,本發明人已經發現,細菌菌種鼠李糖乳桿菌(Lactobacillus rhamnosus)能夠在體內促進腸道菌群多樣性的恢復。
因此,本發明的主題是鼠李糖乳桿菌(Lactobacillus rhamnosus)在提高腸道菌群的恢復力中的應用。特別地,本發明與鼠李糖乳桿菌(Lactobacillus rhamnosus)在維持或提高受試者的腸道菌群多樣性中的應用有關。在具體的實施方式中,使用鼠李糖乳桿菌(Lactobacillus rhamnosus)能夠在患有由抗生素引起的腸道生態失調的受試者中,維持或提高腸道菌群的多樣性。
本發明的其它方面提供了鼠李糖乳桿菌(Lactobacillus rhamnosus)在以下方面中的應用:預防、緩解或治療腸道生態失調;和/或預防由存在于胃腸道中的致病菌引起的疾病;和/或在增加受試者中短鏈脂肪酸的水平。
本發明還提供了組合物,該組合物包括用于本發明的應用的鼠李糖乳桿菌(Lactobacillus rhamnosus)。
技術實現要素:
在本文中,短語“維持菌群多樣性”用于表示:尤其是在生態失調的情況下,不會顯著地改變或影響個體中菌群的物種多樣性(物種豐富度和/或物種均勻性)。特別地,維持菌群多樣性可以幫助受試者在有生態失調風險的情況下更快地恢復,或者可以避免生態失調惡化。短語“增加菌群多樣性”、“促進菌群多樣性的恢復”、“生態失調的治療/緩解/降低”等用于表示:個體中菌群的物種多樣性(物種豐富度和/或物種均勻性)的增加。用于計算物種多樣性、物種豐富度和物種均勻度的方法是本領域已知的,包括但不限于辛普森指數,辛普森多樣性指數和辛普森相互指數,曹指數(Chao Index)和香農指數。
此外,“加速腸道菌群多樣性的增加”、“促進腸道菌群多樣性的恢復”、“有利于恢復至基線/正常/健康的腸道菌群多樣性”、“加速生態失調的緩解/降低/消失”等用于表示:在抗生素治療后患有腸道生態失調的個體內的菌群多樣性(豐富度和/或均勻性)在服用益生菌菌株的受試者中比未服用益生菌菌株的對照受試者在統計學上增加更快,從而抗生素治療后三周的菌群的結構在服用益生菌菌株的受試者中比未服用益生菌菌株的受試者在統計學上更接近于治療前的結構。
如本文中所使用的,術語“生態失調”應當被理解為與健康或普通群體相比,菌群共生物種多樣性的改變,并且應包括有益微生物的減少和/或致病菌(致病性微生物或潛在致病性微生物)的增加和/或總體菌群物種多樣性的減少。許多因素可能傷害腸道菌群的有益成員,從而導致生態失調,這些因素包括抗生素的使用、心理和生理壓力、輻射和飲食變化。抗生素的使用是導致正常菌群中發生重大改變的最常見且不可忽略的原因。因此,如本文所使用的,術語“抗生素誘導的生態失調”是指由抗生素所引起的生態失調,包括促進細菌性機會致病菌的過度生長,其中細菌性機會致病菌包括糞腸球菌(Enterococcus faecalis)、屎腸球菌(Enterococcus faecium)或艱難梭菌(Clostridium difficile)。
如本文所使用的,術語“乳品組合物“應當被理解為適于動物食用,特別是人類食用的奶類組合物。
如本文所使用的,術語“奶”應理解為包括蔬菜奶或動物奶,例如但不限于大豆奶、杏仁奶、斯佩爾特小麥奶(spelt milk)、燕麥奶、麻籽奶(hemp milk)、椰奶、米奶、山羊奶、綿羊奶或牛奶。
如本文所使用的,術語“x%(w/w)”被認為等于“x g/100g”。
如本文所使用的,所提及的細菌菌株或物種應當被理解為包括由此衍生的保留緩解受試者(優選患有抗生素誘導的生態失調的受試者)的腸道生態失調的能力的細菌。為了評估該能力,可使用與下文實施例中所述相同的模型。源自于可以根據本發明使用的親本菌株的菌株包括突變菌株和遺傳轉化菌株。這些突變菌株或遺傳轉化菌株可以是其中親本菌株中的一個或多個內源基因已經發生突變的菌株,例如改變它們的一些代謝性質(例如它們發酵糖的能力,它們對酸度的耐性,它們在胃腸道中運輸的存活能力,它們的后酸化性質或它們的代謝產物)。它們還可以是由親本菌株經遺傳轉化以增加一個或多個感興趣的基因而產生的菌株,其中增加一個或多個感興趣的基因例如是為了給予所述遺傳轉化菌株額外的生理特征,或允許它們表達希望通過施用該菌株來表達的感興趣的治療性蛋白質或疫苗。這些突變體或遺傳轉化菌株可以利用細菌的隨機或定點誘變和遺傳轉化的常規技術,或利用被稱為“基因組重排”的技術由親本菌株來獲得。在本文中,當提及親本物種或菌株時,應理解其涵蓋衍生自所述親本物種或菌株并且保留在患有抗生素誘導的生態失調的受試者中維持或增加腸道菌群多樣性的能力的菌株、突變體和變體,例如,短語“鼠李糖乳桿菌(Lactobacillus rhamnosus)”和“菌株CNCM I-3690”應被理解為包括衍生自它們的菌株、突變體和變體。
如本文所使用的,術語“食物補充劑”應被理解為由食品中常用的化合物制成的產品,但其為片劑、粉末、膠囊、飲劑的形式或通常不與營養物相關的任何其它形式,并且對個體健康具有有益的影響。
如本文所使用的,術語“功能性食物”應被理解為除了提供營養之外,還對個體的健康具有有益效果的營養物。特別地,食物補充劑和功能性食物可以具有生理效應-用于疾病(例如慢性疾病)的預防、改善或治療疾病。
如本文所使用的,術語“發酵乳”或“發酵奶”是指分別通過至少一種乳酸菌的酸化作用從乳品組合物或奶品組合物得到的組合物,所述乳酸菌可包含在發酵物、培養物或引酵物中。
如本文所使用的,術語“可勺取的”應被理解為可利用勺子或其他器具食用的固體或半固體。
鼠李糖乳桿菌(L.RHAMNOSUS)的應用
本發明提供了鼠李糖乳桿菌(L.rhamnosus),優選菌株CNCM I-3690在受試者(優選患有腸道生態失調的受試者)中維持或增加腸道菌群多樣性中的應用。
因此,一個實施方式中,本發明提供了鼠李糖乳桿菌(L.rhamnosus),優選菌株CNCM I-3690在預防或緩解受試者腸道生態失調中的應用。根據布達佩斯條約,將菌株CNCM I-3690于2006年11月9日保藏在CNCM(Collection Nationale de Cultures de Microorganismes,25rue du Docteur Roux,巴黎)。該菌株公開在國際申請WO 2009/122042中。
在優選的實施方式中,腸道生態失調由受試者的抗生素治療引起或在受試者的抗生素治療后引起。
在又一實施方式中,本發明提供了鼠李糖乳桿菌(L.rhamnosus),優選菌株CNCM I-3690在預防胃腸細菌感染中的應用和/或預防由胃腸道中存在的致病菌(優選共生和/或機會致病菌)所引起的疾病的發展中的應用。這些疾病可位于GIT中,或在機會致病菌穿過腸道屏蔽(顯著和/或長期的生態失調有助于所述穿過)的情況中,擴散至腹腔、血液等。因此,本發明進一步提供了用于預防胃腸細菌感染的方法和/或預防由受試者胃腸道中存在的致病菌引起的疾病的發展的方法,所述方法包括:將有效量的組合物施用予受試者,所述組合物包括鼠李糖乳桿菌(L.rhamnosus),優選菌株CNCM I-3690。優選地,所述受試者患有腸道生態失調。在優選的實施方式中,所述腸道失衡由受試者的抗生素治療所引起,或在受試者的抗生素治療后引起。在進一步優選的實施方式中,所述致病菌為糞腸球菌(Enterococcus faecalis)。
短鏈脂肪酸的增加
本發明人已證明:鼠李糖乳桿菌(L.rhamnosus),優選菌株CNCM I-3690的施用在維持或增加菌群多樣性的同時,還使受試者中短鏈脂肪酸的水平增加。如先前在本領域中所述,菌群的廣泛多樣性和菌群中的SCFA(特別是丁酸鹽/酯)的高水平單獨或組合地對健康是有利的。因此,在生態失調的情況下,鼠李糖乳桿菌(Lactobacillus rhamnosus)允許菌群多樣性增加和SCFA的增加這一事實,表明鼠李糖乳桿菌(Lactobacillus rhamnosus)尤其可以是健康有益的。
因此,在又一實施方式中,本發明提供了鼠李糖乳桿菌(L.rhamnosus),優選菌株CNCM I-3690在增加受試者中的短鏈脂肪酸的應用。在一個實施方式中,所述短鏈脂肪酸是腸道的,典型地為結腸、遠端結腸、盲腸或排泄物。在優選的實施方式中,所述短鏈脂肪酸為丁酸鹽/酯。在替代性實施方式中,本發明提供了鼠李糖乳桿菌(L.rhamnosus),優選菌株CNCM I-3690在增加丁酸鹽/酯與乙酸鹽/酯的比例中的應用。優選地,上述受試者患有腸道生態失調。在又一優選的實施方式中,腸道生態失調由受試者的抗生素治療所引起或在受試者的抗生素治療后引起。
組合物
本發明的另一方面提供了包括鼠李糖乳桿菌(L.rhamnosus),優選菌株CNCM I-3690的組合物,用于本發明的應用中。因此,本發明提供了包括鼠李糖乳桿菌(L.rhamnosus),優選菌株CNCM I-3690的組合物,用于:維持或增加腸道菌群多樣性;和/或在預防或治療腸道生態失調;和/或預防由胃腸道內存在的致病菌(優選共生和/或機會致病菌)所引起的疾病;和/或增加受試者中的短鏈脂肪酸水平。優選地,所述受試者患有腸道生態失調,進一步優選地,所述生態失調由受試者的抗生素治療所引起或在受試者的抗生素治療后引起。
因此,在本發明優選的實施方式中,菌株鼠李糖乳桿菌(L.rhamnosus),優選菌株CNCM I-3690以可口服施用組合物的形式提供。在這樣的組合物中,所述菌株可以以活的或死的全菌形式使用。可替代地,所述菌株可以細菌裂解物的形式來使用。優選地,細菌細胞以活的且可存活的細胞形式存在。
根據本發明,所述組合物可以是適合于口服施用的任何形式。這包括例如固體、半固體、液體和粉末。半固體組合物(諸如酸奶)和液體組合物(例如飲料)是優選的。
優選地,所述組合物包括每克重量至少1.106菌落形成單位(cfu)、至少1.107菌落形成單位(cfu)或優選至少1.108cfu的鼠李糖乳桿菌(L.rhamnosus),優選菌株CNCM I-3690。優選地,基于本發明的每克(g)組合物,根據本發明的組合物包括至多約1011菌落形成單位,更優選至少1010菌落形成單位并且最優選至少109菌落形成單位(CFU)的根據本發明的鼠李糖乳桿菌(L.rhamnosus),優選菌株CNCM I-3690。
所述組合物可進一步包括:除上述菌株之外的乳桿菌屬(Lactobacillus)的其它菌株和/或細菌的其它菌株,特別是益生菌菌株,例如嗜熱鏈球菌(Streptococcus thermophilus)、雙歧桿菌(Bifidobacterium)和乳球菌(Lactococcus)菌株。
所述組合物可為藥物組合物或營養組合物。根據優選的實施方式,所述組合物是營養組合物,諸如食品(包括功能性食物)或食物補充劑。
可根據本發明使用的營養組合物包括乳品組合物,優選發酵乳品組合物。發酵組合物可以是液體形式,或者是通過干燥發酵液體而獲得的干粉形式。乳品組合物的實例包括乳酪、酸奶,和凝固、攪拌(stirred)或可飲用形式的發酵奶和/或發酵乳清。發酵產品還可以是凝固、攪拌或可飲用形式的發酵植物,例如發酵的大豆、谷物和/或果實。可根據本發明使用的營養組合物還包括幼兒食物、嬰兒配方奶粉和嬰兒后續(follow-on)配方奶粉。在優選的實施方式中,發酵產品是新鮮產品。未經過嚴格熱處理步驟的新鮮產品具有細菌菌株以存活形式存在的優點。
特別優選的是,根據本發明的組合物是乳品組合物,特別是發酵乳品組合物。
優選地,根據本發明的乳品組合物包含或衍生自(特別是通過發酵):含有30%至100%(w/w)的奶、更優選50%至100%(w/w)的奶和甚至更優選70%至100%(w/w)的奶的組合物。還優選地,根據本發明的乳品組合物包括或衍生自(特別是通過發酵):基本上由奶(優選牛奶)組成的組合物,或僅由奶(優選牛奶)組成的組合物。
優選地,根據本發明的乳品組合物包括或衍生自(特別是通過發酵):含脫脂奶或非脫脂奶之一或兩者的組合物。優選地,所述奶或多種奶可以是液體、粉末和/或濃縮形式。在一個實施方式中,所述奶或多種奶可以富含或強化了用另外的奶組分或其它營養物,諸如但不限于維生素、礦物質、微量元素或其它微量營養物。
所述發酵乳品組合物通過至少一種乳酸菌的酸化作用衍生自本發明的乳品組合物,該至少一種乳酸菌可以包含在發酵物、培養物或引酵物中。更優選地,根據本發明所述的發酵乳品組合物通過至少一種、兩種、三種、四種、五種、六種、七種或更多種乳酸菌菌株的酸化作用獲得。因此,“發酵乳品組合物”包括至少一種、兩種、三種、四種、五種、六種、七種或更多種乳酸菌菌株。
用于制備發酵乳品(諸如酸奶或其等同物)的方法是本領域公知的。典型地,通過與合適的微生物一起培養熱處理(例如巴氏殺菌的)脫脂奶和/或非脫脂奶以使pH降低,來制備發酵奶制品。合適的微生物(例如嗜熱乳酸菌)的選擇在本領域技術人員的范圍內。
根據本發明的乳品組合物,特別是發酵乳品組合物可選地進一步包含輔助成分,諸如果實、蔬菜、營養性和非營養性甜味劑、谷物、調味劑、淀粉、增稠劑、防腐劑或穩定劑。優選地,根據本發明的乳品組合物,特別是發酵乳品組合物應包含至多約30%(w/w)的所述輔助成分,例如,至多約10%、15%、20%、25%(w/w)的輔助成分。
優選地,根據本發明的乳品組合物是發酵乳品組合物、更優選發酵奶品組合物,包括或基本上包括經過至少相當于巴氏殺菌的熱處理的奶,或由經過至少相當于巴氏殺菌的熱處理的奶組成,優選所述熱處理在制備所述乳品組合物或發酵乳品組合物之前進行。
優選地,根據本發明的乳品組合物是發酵乳品組合物,更優選每100g重量包含約0.3g以上游離乳酸的發酵奶品組合物,更優選地,本發明提供了每100g包括約0.7g或0.6g以上游離乳酸的發酵奶品組合物。優選地,根據本發明的乳品組合物是發酵乳品組合物,更優選地是包括至少與奶或其來源的奶的蛋白含量相等的發酵奶品組合物。
優選地,根據本發明的乳品組合物是發酵乳品組合物,更優選地是pH等于或低于5、更優選約3.5至約4.5的發酵奶品組合物。
優選地,根據本發明的乳品組合物是發酵乳品組合物,更優選地是在10℃下,64/s的剪切速率時,粘度低于200mPa.s、更優選低于100mPa.s并且最優選低于60mPa.s的發酵奶品組合物。在一個實施方式中,根據本發明的乳品組合物是可飲用的發酵乳品組合物,更優選地是飲料發酵奶飲料,諸如但不限于酸奶飲料、克非爾(kefir)等。在替代性實施方式中,根據本發明的乳品組合物是發酵乳品組合物,更優選地是可勺取的發酵乳品組合物。
還優選地,根據本發明的乳品組合物,特別是發酵乳品組合物或根據本發明的產品可以在1℃至10℃的溫度下儲存。
根據本發明的乳品組合物,特別是發酵乳品組合物,更優選根據本發明的發酵奶品組合物或者產品的單份量以重量計,優選為約50g、60g、70g、75g、80g、85g、90g、95g、100g、105g、110g、115g、120g、125g、130g、135g、140g、145g、150g、200g、300g或320g,或者可替代地為約1盎司、2盎司、3盎司、4盎司、5盎司、6盎司或12盎司。
優選地,根據本發明的乳品組合物、特別是發酵乳品組合物,更優選根據本發明的發酵奶品組合物包括:每克(g)根據本發明的組合物,至少106、更優選至少107、并且最優選至少108菌落形成單位(CFU)的根據本發明的鼠李糖乳桿菌(L.rhamnosus),優選菌株CNCM I-3690。
治療用途
本發明的主題還在于鼠李糖乳桿菌(L.rhamnosus),優選菌株CNCM I-3690或如上定義的組合物,在制備用于以下方面的藥物中的應用:用于維持或增加腸道菌群多樣性;和/或用于預防或治療腸道生態失調;和/或用于預防由胃腸道內存在的致病菌(優選共生和/或機會致病菌)所引起的疾病;和/或用于增加受試者中短鏈脂肪酸的水平。優選地,所述受試者患有腸道生態失調,進一步優選地,所述生態失調由受試者的抗生素治療所引起或在受試者的抗生素治療后引起。
本發明的主題還在于如上所限定的鼠李糖乳桿菌(L.rhamnosus)菌株,優選菌株CNCM I-3690或如上所限定的組合物在用于以下方面的應用:維持或增加腸道菌群多樣性;和/或預防或治療腸道生態失調;和/或預防由胃腸道內存在的致病菌(優選地,共生和/或機會致病菌)所引起的疾病;和/或增加受試者中短鏈脂肪酸的水平。優選地,所述受試者患有腸道生態失調,進一步優選地,所述生態失調由受試者的抗生素治療所引起或在受試者的抗生素治療后引起。
本發明的主題還在于用于維持或增加胃腸菌群多樣性的方法;和/或預防或治療腸道生態失調的方法;和/或預防由胃腸到中存在的致病菌(優選地,共生和/或機會致病菌)所引起的疾病的方法;和/或增加在需要的受試者中短鏈脂肪酸的水平的方法,所述方法包括將治療有效量的如上所限定的鼠李糖乳桿菌(L.rhamnosus)菌株,優選菌株CNCM I-3690或如上所限定的組合物施用予所述受試者。優選地,所述受試者患有腸道生態失調,進一步優選地,所述生態失調由受試者的抗生素治療所引起或在受試者的抗生素治療后引起。
特別是在考慮到本文提供的詳細公開內容下,治療有效量的確定是本領域技術人員熟知的。
本發明的主題還在于用于制備藥物的方法,所述藥物用于:維持或增加胃腸菌群多樣性;和/或預防或治療腸道生態失調;和/或預防由胃腸道中存在的致病菌(優選地,共生和/或機會致病菌)所引起的疾病;和/或增加受試者中短鏈脂肪酸的水平,所述方法包括將如上所限定的鼠李糖乳桿菌(L.rhamnosus)菌株,優選菌株CNCM I-3690并入到至少一種藥學上可接受的稀釋劑、載劑或賦形劑中。
服用量(dosage)
在一個實施方式中,本發明提供了食用或施用劑量約108至約1011菌落形成單位(CFU)的鼠李糖乳桿菌(L.rhamnosus),優選約108至約109菌落形成單位、更優選約109至約1010菌落形成單位(CFU),并且在一替代性實施方案中,約1010至1011菌落形成單位(CFU)的鼠李糖乳桿菌(L.rhamnosus),更優選菌株CNCM I-3690,用于本文所公開的應用和方法。在另一實施方式中,在24小時時段內提供至少1、2、3或4劑。進一步優選地,日劑量方案保持至少約1天、2天、3天、4天、5天、6天或7天;或在替代性實施方式中,該日劑量方案保持至少約1周、2周、3周、4周、5周、6周或7周。
因此,在一個實施方式中,本發明提供每日食用或施用至少1份、2份、3份或4份根據本發明的乳品組合物、特別是發酵乳品組合物,更優選根據本發明的發酵奶品組合物。每份可以單獨地被食用或施用,或者在單次中可食用或施用多份。上述多份中的每一份可在進餐時或在進餐之間食用(例如作為零食,在體育活動等之后)。
根據本發明的乳品組合物,特別是發酵乳品組合物,更優選根據本發明的發酵奶品組合物的單份量以重量計,優選為約50g、60g、70g、75g、80g、85g、90g、95g、100g、105g、110g、115g、120g、125g、130g、135g、140g、145g、150g、200g、300g或320g,或者約1盎司、2盎司、3盎司、4盎司、5盎司、6盎司或12盎司。
優選地,根據本發明的組合物包含:每克(g)根據本發明的組合物,至少106菌落形成單位、更優選至少107菌落形成單位并且最優選至少108菌落形成單位(CFU)的根據本發明的鼠李糖乳桿菌(L.rhamnosus),更優選菌株CNCM I-3690。還優選地,根據本發明的組合物包括:每克(g)根據本發明的組合物的細菌為至少1011菌落形成單位,更優選至少1010菌落形成單位,最優選至少109菌落形成單位(CFU)的鼠李糖乳桿菌(L.rhamnosus),更優選菌株CNCM I-3690。
例如,在一個實施方式中,本發明提供了至少2份或至少3份的100g或125g份的發酵奶品的日食用量,所述發酵奶品包括每g制品約至少107至至少108菌落形成單位(CFU)的鼠李糖乳桿菌(L.rhamnosus)I-3690。在另一實施方式中,維持所述日食用水平至少1周、2周、3周、4周或更多周的時段。
從以下進一步描述和附圖中將更清楚地理解本發明,其中,該進一步描述涉及闡述鼠李糖乳桿菌(L.rhamnosus),例如菌株CNCM I-3690緩解體內生態失調以及增加短鏈脂肪酸的能力的實施例。
附圖說明
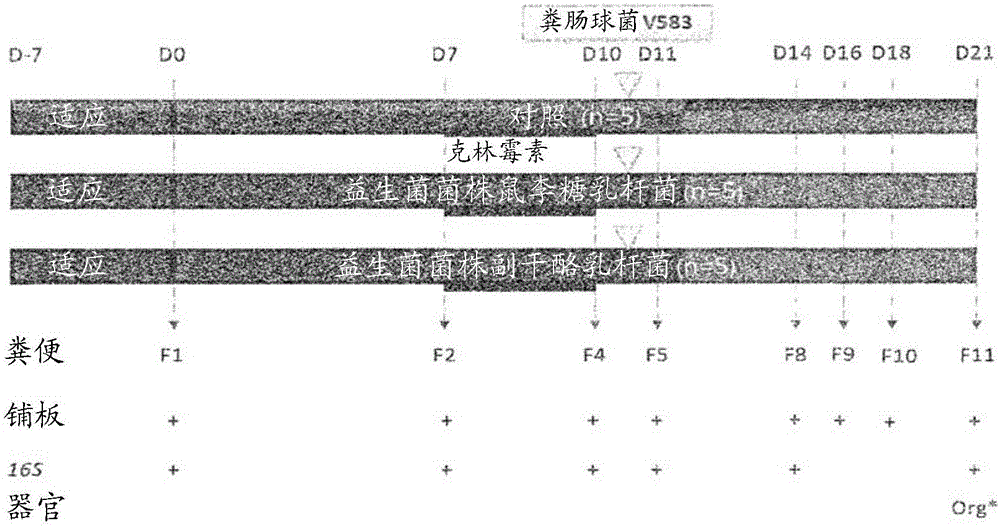
圖1:表示實驗順序的圖示。
圖2:通過Chao指數測量的菌群的豐富度。C:對照,Lr:鼠李糖乳桿菌(L.rhamnosus。
圖3:克林霉素治療和恢復后,腸球菌和腸桿菌相對于基線的相對豐度。
圖4:在D0、D7、D10、D11和D21時,從對照組和鼠李糖乳桿菌(L.Rhamnosus)組(每組和每個時間點n=3)收集的樣品的加權Unifrac距離的主坐標分析。
具體實施方式
實施例
本發明人開發了基于由克林霉素誘導的菌群生態失調以模擬腸球菌過度生長和VRE建立的腸道定植小鼠模型。小鼠皮下接受克林霉素3天,之后口胃接種糞腸球菌(Enterococcus faecalis)VRE菌株(V583)。小鼠的天然菌群中幾乎或完全沒有糞腸球菌(Enterococcus faecalis);此外,在小鼠中不會發生共生至致病菌的轉變。使用該模型,在抗生素治療前一周開始,直到停止抗生素治療和接種VRE之后兩周,每天將益生菌菌株口服施用予小鼠。通過選擇性鋪板,監測建立的動力學和VER清除率以及固有腸球菌群落水平。同時,收集糞便樣品,用于全菌群的16S rRNA基因調查分析。在該模型中誘導的生態失調模擬在人中觀察到的抗生素誘導的生態失調。因此,該模型構成了良好模型,以研究相對腸球菌過度生長的腸道定植屏蔽的機制。菌株V583屬于CC2,并且是美國報道的第一個耐萬古霉素的菌系(Sahm等,1989)。該菌株在下面報道的實驗中作為CC2分離株,并且更常見的致病菌糞腸球菌(E.faecalis)的模型菌株中。
方法
細菌生長
糞腸球菌(E.faecalis V583菌株在補充有0.5%葡萄糖的M17(GM17)中生長,并在達到穩定期后通過離心1小時來收集。細菌細胞用0.9%鹽水溶液洗滌兩次,并于-80℃下以干燥冷凍塊狀物的形式儲存。該菌株屬于CC2,并且是在美國報道的第一個耐萬古霉素的分離株(Sahm等人,1989)。
使益生菌菌株在MRS培養基中生長,并如上所述進行收集。
在接種前至少兩天,將冷凍的細菌懸浮在鹽水溶液中,并將連續稀釋液鋪板在GM17或MRS瓊脂平板上,以測定該塊狀物的細菌計數。
小鼠糞腸球菌(E.faecalis)模型定植化
使用特定的無致病菌的雄性CF-1小鼠(Harlan,USA)進行小鼠實驗6~8周。每個籠中飼養總共5只小鼠,并用高壓滅菌的食物和水自由飼喂。
利用鋼飼喂管(Ecimed)通過口胃接種,小鼠接受含109CFU的益生菌菌株的0.1ml的0.9%鹽水溶液的日劑量。將鼠李糖乳桿菌(Lactobacillus rhamnosus)CNCM I-3690施用予Lr組,并且將鼠李糖乳桿菌(Lactobacillus rhamnosus)I-3689施用予Lp組。對照組的動物以相同的方式接受0.1ml的0.9%鹽水溶液。在益生菌治療一周后,每天皮下施用劑量為1.4mg/天的克林霉素,持續三天。一天后,利用鋼飼喂管(Ecimed)通過口胃接種,施用含1010菌落形成單位(CFU)的糞腸球菌(E.faecalis)(耐萬古霉素性腸球菌,稱為“VRE”)菌株V583的0.1ml的0.9%鹽水溶液。
如下面的實驗設計中所述,收集糞便樣品。將糞便(50~100mg/小鼠)或盲腸保持在4℃,并且在取樣后3小時內處理,且在室溫下加工。從該階段開始,所有的工作在PSMII的無菌條件下進行。稱重樣品并使該樣品以10-1的稀釋度懸浮。根據重量,加入調節體積的蛋白胨水(例如,對于100mg,為900μl;對于50mg,為450μl)。使用100μl體積的懸浮液(稀釋-1),在蛋白胨水中進行數十倍稀釋直到10-8。通過將稀釋的糞便樣品鋪板到BEA上并且將總乳酸菌鋪板到MRS培養基上,然后在37℃厭氧條件(Gaz包裝)下孵育48小時,來監測總腸球菌群落。為了使用糞腸球菌(E.faecalis)V583施用來進行研究,隨后將V583鋪板到補充有6μg/mL萬古霉素的BEA上來示蹤V583的群落水平。還收集了糞便樣品用于全菌群的16S rRNA基因調查分析。在實驗結束時,處死動物。收集盲腸內容物以通過測量短鏈脂肪酸的濃度來評估發酵模式。回收結腸并立即用于RNA提取(在液氮中冷凍)或組織學(多聚甲醛溶液4%)。
菌群分析
在第0天(基線)、第7天(益生菌治療1周)、第10天(抗生素攝取3天)、第11天(糞腸球菌(E.faecalis)V583接種后1天)和第21天(處死)收集糞便樣品。使用Godon等人方法提取DNA(Godon,1997)。對于焦磷酸測序,基于Sim等人(2012)的設計,使用密鑰(key)標記的真細菌引物(Lifesquencing SL,Valencia,西班牙)擴增16S rRNA基因的V3-V5區域。使用20ng宏基因組DNA,每種200μM的四種脫氧核苷三磷酸,每種400nM的引物,2.5U的FastStart HiFi聚合酶以及由制造商(Roche,Mannheim,德國)提供的含有MgCl2的合適緩沖液,4%的20μg/mLBSA(Sigma,Dorset,英國)和0.5M甜菜堿(Sigma),來進行PCR反應。熱循環由以下組成:在94℃下初始變性2分鐘,接著進行94℃下變性20秒、50℃下退火30秒以及72℃下延伸5分鐘的35次循環。將擴增子以等摩爾濃度合并在單管中。將合并的擴增子混合物純化兩次(AMPure XP試劑盒,Agencourt,Takeley,英國),并使用PicoGreen測定(Quant-iT,PicoGreen DNA測定,Invitrogen)再次量化無污染的合并物。隨后,擴增子提交給由Life Sequencing S.L.(Valencia,西班牙)提供的焦磷酸測序服務,其中進行EmPCR,隨后按照Roche Amplicon Lib-L方案,在454Life Sciences GS FLX+儀器(Roche)上進行單向焦磷酸測序。使用QIIME v.1.6(Caporaso,2010)進行生物信息學分析。根據以下質量標準過濾后,將數據分為50個樣本:大小在500nt和1000nt之間,50個堿基對窗口上的質量在25以上,引物和條形碼序列中經核定沒有錯配,以及不存在大于6nt的聚合物。使用cd-hit(Li,2006),將剩余的解讀信息聚類成定義為97%一致性下的運算分類單位(OTU),并且利用Greengenes v_13_08數據庫,對每個OTU的代表性序列進行比對和分類學上的分配。對于α多樣性和β多樣性,將樣品稀釋到每個樣品3000個序列。使用豐度(Chao1)和均勻度(Shannon指數)和觀察的OUT的數目的稀疏曲線,來評估α-多樣性(其測量樣品內的多樣性)。使用3500個解讀信息,對加權和未加權Unifrac距離進行β多樣性(其測量樣品間的多樣性)。
盲腸發酵終產物的測量
如前所述,使用500mg盲腸內容物上清液,在水提取酸化樣品后,通過氣相色譜法來測定短鏈脂肪酸(SCFA)的濃度,其中,所述短鏈脂肪酸包括乙酸鹽/酯、丙酸鹽/酯和丁酸鹽/酯的濃度(Nelson 1020,Perkin-Elmer,St Quentin en Yvelines,法國)(Lan et al,2008)。使用D-L乳酸試劑盒(BioSenTeck)來測定乳酸鹽/酯。
統計學分析
通過曼-惠特尼(Mann-Whitney)檢驗(GraphPad)來分析細菌計數的差異、菌群多樣性(豐度和均勻性)以及短鏈脂肪酸數據。當P<0.05時,認為差異是顯著的。
結果:菌株鼠李糖乳桿菌(L.rhamnosus)I-3690在糞腸球菌(E.faecalis)V583的存在下的生態失調后,促進菌群多樣性的恢復,并增加糞便中的丁酸鹽/酯與/乙酸鹽/酯的比例
在糞腸球菌(E.faecalis)定植模型中,在克林霉素治療時,伴隨固有腸球菌的瞬時增加。在抗生素治療停止后一天,腸球菌群落達到最高水平,然后在4至5天后逐漸降至初始水平。在接種后,糞腸球菌(Enterococcus faecalis)VRE菌株與固有腸球菌并存,并且在管飼后至少長達11天內以可檢測的水平持續存在(Rigottier-Gois等人提交)。在本項目中,使用細菌16S rRNA基因的454焦磷酸測序的菌群分析表明,固有腸球菌的過度生長與由抗生素治療導致的菌群多樣性降低相關。益生菌菌株的施用對腸球菌過度生長沒有影響(圖2)。
為了描述克林霉素治療+VRE接種,以及鼠李糖乳桿菌(L.rhamnosus)CNCM I-3690食用對菌群結構的影響,對在第0天(基線)、第7天(益生菌食用1周)、第10天(克林霉素治療3天)、第11天(糞腸球菌E.faecalis V583接種)和第21天(“恢復”)從小鼠收集的糞便樣品進行細菌16S rRNA基因V3-V5可變區的454焦磷酸測序。在第10天和第14天收集的糞便樣品的菌群分析顯示,克林霉素治療導致微菌群組成的劇烈變化,同時喪失多樣性(豐度(Chao指數)和均勻性(Shannon指數))(圖2)。
此外,腸球菌(Enterococcus)屬以及屬于變形菌(Proteobacteria)的種系(特別是腸桿菌科(Enterobacteriaceae))的相對豐度急劇增加(圖3)。
對第21天收集的樣品的分析表明:每日食用鼠李糖乳桿菌(L.rhamnosus)CNCM I-3690使得菌群多樣性的損失程度較低(圖2)。
此外,基于加權和未加權的Unifrac距離矩陣的多變量分析(主分量分析)表明,來自第0天至第7天的樣品(基線+/-益生菌)和來自第10天至第21天的樣品(克林霉素誘導的生態失調)之間存在明顯的區別。值得注意的是,在第21天,與對照組相比,接受鼠李糖乳桿菌(L.rhamnosus)的小鼠組與基線的區別較小(圖4)。
對第21天的盲腸內容物的SCFA和乳酸鹽/酯分析表明:與對照組相比,鼠李糖乳桿菌(L.rhamnosus)CNCM I-3690影響SCFA。在三次獨立實驗(運行)中,與對照相比,并且同時與等同物副干酪乳桿菌(L.paracasei)治療組(下表)相比,在接受鼠李糖乳桿菌(L.rhamnosus)菌株的小鼠中,盲腸丁酸鹽/酯與乙酸鹽/酯的比例顯著增加。在兩次運行中,丁酸鹽/酯的絕對量顯著增加。
運行1
運行2
運行3
- 還沒有人留言評論。精彩留言會獲得點贊!